Der endogene Fructosestoffwechsel könnte den Warburg-Effekt und den Schutz von SGLT2-Inhibitoren bei chronischer Nierenerkrankung erklären
Feb 22, 2022
Chronische leichte Entzündung liegt der Pathogenese von nicht übertragbaren Krankheiten zugrunde, einschließlich chronischerNierenerkrankungen(CNI). Entzündung ist ein biologisch aktiver Prozess, der von biochemischen Veränderungen begleitet wird, die Energie, Aminosäuren, Lipide und Nukleotide beinhalten. In letzter Zeit wurde beobachtet, dass die Glykolyse bei mehreren entzündlichen Erkrankungen, einschließlich mehrerer Arten von, erhöht istNierenerkrankung. Die Faktoren, die die Glykolyse auslösen, bleiben jedoch unklar. Fructosehaltige Zuckerzusätze sind in fast 70 Prozent der verarbeiteten Lebensmittel enthalten und wurden mit der Ätiologie vieler nicht übertragbarer Krankheiten in Verbindung gebracht. In demNierewird Fructose über mehrere Transporter in die proximalen Tubuli transportiert, um pathophysiologische Prozesse zu vermitteln. Fructose kann in der erzeugt werdenNierewährend der Glukose-Reabsorption (z. B. bei Diabetes) sowie vonintrarenalHypoxie, die bei CNE auftritt. Der Fruktosestoffwechsel stellt auch biosynthetische Vorläufer für Entzündungen bereit, indem er trotz der Verfügbarkeit von Sauerstoff das intrazelluläre Stoffwechselprofil von mitochondrialer oxidativer Phosphorylierung auf Glykolyse umschaltet, was dem Warburg-Effekt bei Krebs ähnelt. Wichtig ist, dass Harnsäure, ein Nebenprodukt des Fructosestoffwechsels, wahrscheinlich eine Schlüsselrolle bei der Begünstigung der Glykolyse spielt, indem sie Entzündungen stimuliert und Aconitase im Tricarbonsäurezyklus unterdrückt. Eine konsequente Akkumulation von glykolytischen Zwischenprodukten ist mit der Produktion von biosynthetischen Vorläufern, Proteinen, Lipiden und Nukleinsäuren verbunden, um den erhöhten Energiebedarf für die lokale Entzündung zu decken. Hier diskutieren wir die Möglichkeit, dass Fructose und Harnsäure bei CNE eine metabolische Umstellung auf Glykolyse vermitteln können. Wir schlagen auch vor, dass Natrium-Glucose-Cotransporter 2 (SGLT2)-Inhibitoren das Fortschreiten der CKD verlangsamen können, indem sie sie reduzierenintrarenalGlukose- und anschließend Fruktosespiegel.
Schlüsselwörter:Fructose, Der Warburg-Effekt, CKD - chronische Nierenerkrankung, Entzündung, Fifibrose, Renal
EINLEITUNGChronischNierenerkrankung(CKD) hat in den letzten Jahrzehnten zugenommen und ist eine der Hauptursachen für Morbidität und Mortalität. Von zentraler Bedeutung für sowohl diabetische als auch nicht-diabetische CNE istintrarenalEntzündung und Fibrose. Hier stellen wir eine neue Hypothese vor, dass Fructose, entweder in der Nahrung enthalten oder endogen produziert, eine Schlüsselrolle bei der Entstehung von Krankheiten spielen könnte, da sie durch einen Warburg-Effekt Entzündungen hervorrufen kann. Wir postulieren auch, dass dies den schützenden Nutzen der Natrium-Glucose-Cotransporter-2 (SGLT2)-Inhibitoren erklären könnte. Während andere vorgeschlagen haben, dass SGLT2-Hemmer zur Verfügung stehen könntenNieren-Schutz durch Umkehrung des Warburg-Effekts (1), hier schlagen wir vor, dass der endogene Fructose-Stoffwechsel der Mediator des Warburg-Effekts in diesem Manuskript sein könnte, und wir schlagen einen Mechanismus vor, durch den SGLT2-Inhibitoren den Fructose-Stoffwechsel in reduzieren könntenNiere.Da Fructose auch bei nicht-diabetischen Erkrankungen endogen produziert wird, könnte unsere Hypothese darauf angewendet werden, wie SGLT2-Inhibitoren sowohl diabetische als auch nicht-diabetische CKD verbessern.

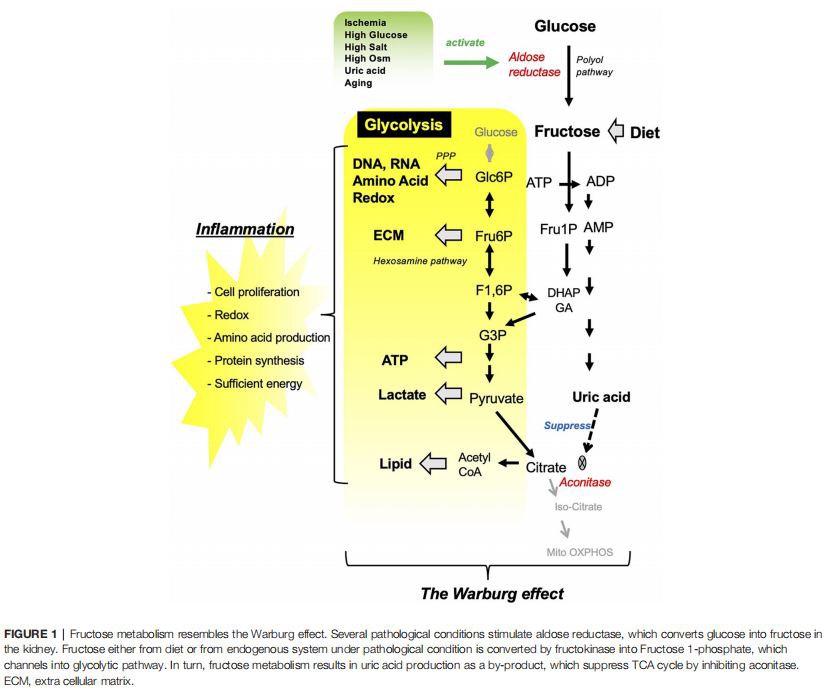
FRUCTOSE, DAS METABOLISCHE SYNDROM UND CNEFructose ist ein einfacher Zucker, der in Obst und Honig vorkommt, und ist auch ein Hauptbestandteil von zugesetzten Zuckern wie Saccharose (ein Disaccharid aus Fructose und Glucose) und Maissirup mit hohem Fructosegehalt (HFCS, eine Kombination aus Monosaccharid aus Fructose und Glucose). Die Aufnahme von Fruktose ist im letzten Jahrhundert in Verbindung mit der insgesamt erhöhten Aufnahme von zugesetztem Zucker sprunghaft angestiegen. Fruktose kann auch im Körper durch Aktivierung der Aldose-Reduktase (AR) im Polyolweg hergestellt werden (Abbildung 1). Es ist bekannt, dass eine Vielzahl von Stimuli die AR-Expression erhöhen, einschließlich Ischämie, Hypoxie, Hyperglykämie, Hyperosmolalität und Harnsäure (2–5). Während die endogene Fructoseproduktion normalerweise niedrig ist, gibt es zunehmend Hinweise darauf, dass die endogene Fructoseproduktion nicht nur bei Diabetes (6, 7), sondern auch durch eine kohlenhydratreiche Ernährung, salzige Speisen und Alkohol, die in der westlichen Ernährung üblich sind, erhöht wird (8–11 ).
Die Forschung hat eine Rolle von Fructose bei vielen nichtübertragbaren Krankheiten, einschließlich Fettleibigkeit, Diabetes, nichtalkoholischer Fettlebererkrankung und Herzerkrankungen (12, 13) und sowohl akuten als auch chronischen, impliziertNierenerkrankung(5, 6, 14, 15). Klassischerweise wurde dies der Wirkung von Fructose zur Stimulierung von oxidativem Stress, Endotheldysfunktion, Stimulierung von Vasopressin und Harnsäurebildung zugeschrieben (12, 13, 16).
Kürzlich haben wir Beweise dafür überprüft, dass Fruktose auch das Krebswachstum unterstützen kann, indem sie einen metabolischen Schalter einschaltet, der die mitochondriale Atmung gegenüber der Glykolyse begünstigt, was dem Warburg-Effekt ähnelt (17, 18). Der Warburg-Effekt ist wahrscheinlich auch am Fortschreiten von Nicht-Tumorerkrankungen beteiligt, einschließlich pulmonaler Hypertonie, Herz-Kreislauf-Erkrankungen, neuronalen Störungen undNierenerkrankungen(19). Hier schlagen wir vor, dass der Warburg-Effekt aufgrund von Fructose eine Rolle bei chronischen Erkrankungen spielen könnteNierenerkrankung(CNI).
FRUCTOSE-STOFFWECHSEL UND DER WARBURG-EFFEKTGlykolyse ist der Stoffwechselweg, der Glukose in Pyruvat umwandelt, das in den Tricarbonsäure (TCA)-Zyklus in Mitochondrien eintreten kann, wo ATP durch oxidative Phosphorylierung erzeugt wird. Fructose unterscheidet sich von Glucose dadurch, dass sie ausschließlich zu Fructose 1--phosphat (Fru1P) metabolisiert wird. Fru1P kann anschließend metabolisiert werden, um sich mit dem glykolytischen Weg zu verbinden (Abbildung 1). Während des Fructosestoffwechsels reduziert die Aktivierung der C-Isoform Offructokinase (Ketohexokinase-C; KHK-C) sowohl Phosphat als auch Adenosintriphosphat (ATP) in der Zelle und löst den Abbau von Adenosinmonophosphat (AMP) durch AMP-Deaminase zur Harnsäureproduktion aus . Harnsäure ist ein intrazelluläres Prooxidans und kann Aconitase unterdrücken, das Enzym, das im TCA-Zyklus Citrat zu Isocitrat katalysiert. Infolgedessen kann Fruktose als metabolischer Schalter fungieren, der trotz der Verfügbarkeit von Sauerstoff eine schnellere Energieerzeugung aus der Glykolyse im Vergleich zu der durch mitochondriale Atmung erzeugten Energie begünstigt. Ähnlich wie beim Warburg-Effekt beim Krebswachstum liefert die aktivierte Glykolyse mehrere Zwischenprodukte, die mit nachfolgenden Stoffwechselwegen verbunden sind, darunter der Pentosephosphatweg, der Hexosaminweg und die Lipidsynthese, und diese biosynthetischen Vorläufer tragen zur Entzündungsreaktion bei (17).
MECHANISMEN, DURCH DIE FRUCTOSE EINE NIERENENTZÜNDUNG STIMULIERTIn demNierewird Nahrungsfructose vollständig durch den Glomerulus filtriert und in den proximalen tubulären Epithelzellen durch Fructosetransporter reabsorbiert, die in der apikalen Membran exprimiert werden. Die Fruktose wird physiologisch im Cytosol als Substrat für die Glukoneogenese verwendet, um die systemische Glukosekonzentration aufrechtzuerhalten (18). DasNiereist in der Lage, Fructose endogen zu produzieren, um mit mehreren pathologischen Zuständen fertig zu werden. Beispielsweise stimulieren Ischämie, hohe Glukose und hohe Osmolarität, die alle Schlüsselkomponenten von CKD sind, die Aldosereduktase und aktivieren den Polyolweg (Abbildung 2).
Eine übermäßige Menge an Fructose in der Nahrung ist schädlich für dieNiere. Tatsächlich entwickeln normale Ratten eine milde tubulointerstitielle Entzündung und Fifibrose bei einer Diät mit hohem Fructosegehalt. Die tubuläre epitheliale Vimentin-Expression, die Kollagen-III-Ablagerung und die Infifiltration von Immunzellen wurden durch diätetische Fructose bei Nagetieren induziert (15, 20). Im VorhandenenNierenverletzung, Fructose beschleunigt das Fortschreiten vonNierenverletzungenmit auffälligen entzündlichen Veränderungen sowohl in den Glomeruli als auch im Tubulointerstitium (14). Es wurde festgestellt, dass kultivierte proximale Tubuluszellen entzündliche Zytokine freisetzen, einschließlich Monozyten-Chemoattractant-Protein -1 (MCP-1) als Reaktion auf Fruktose, eine durch Harnsäure vermittelte Stoffwechselreaktion (21).
Die Entzündungsreaktion auf Fructose wird nicht nur durch Fructose aus der Nahrung, sondern auch durch die endogene Produktion von Fructose in den tubulären Epithelzellen induziert. Tatsächlich zeigten Studien an Mäusen, dass Diabetes oder Hypoxie das ausmachenNieren-tubuläre Epithelzellen zur Freisetzung mehrerer entzündlicher Zytokine, einschließlich NFkB-Aktivierung, IL6- und CCL2-Expression, die alle in Fructokinase-defizienten Mäusen abgestumpft waren (5, 6). Endothelzellen werden auch stimuliert, interzelluläre Adhäsionsmoleküle-1 (ICAM-1) als Reaktion auf Fructose freizusetzen (22). Ein wahrscheinlicher Mechanismus ist die Fähigkeit von Offructose, die Verfügbarkeit von Stickoxid (NO) in den Endothelzellen zu reduzieren, da NO-Donoren die Fructose-induzierte ICAM-1-Expression abschwächten. Es wurde gezeigt, dass dieser Effekt auf die Entkopplung der endothelialen NO-Synthase (eNOS) zurückzuführen ist, die aus fructoseinduziertem oxidativem Stress resultiert (23–25). An diesem Prozess könnte auch die durch Fructose induzierte Bildung von Harnsäure beteiligt sein, da Harnsäure direkt die Endothelfunktion beeinträchtigt (16, 26, 27).
CNE IST MIT VERSCHLECHTERNDER NIERENHYPOXIE VERBUNDENUnter normalen physiologischen Bedingungen ist dieNiereDie Medulla befindet sich in einem sauerstoffarmen Zustand mit einem Sauerstoffpartialdruck im Bereich von 10 bis 20 mmHg, im Gegensatz zu dem im Kortex, der etwa 50 mmHg beträgt (28). Die physiologische Hypoxie hängt weitgehend vom hohen Sauerstoffbedarf abNieren-Röhrenzellen zur Aufrechterhaltung des Elektrolyttransports. Auch die Sauerstoffversorgung ist in diesem Bereich eingeschränkt, da das Gefäßsystem mit einem Gegenstromsystem betrieben wird, bei dem Sauerstoff von arteriellen zu venösen Vasa recta diffundiert und das Außenmark sauerstoffarm verlässt (28). Unter pathologischen Bedingungen wird ein niedriger Sauerstoffgehalt weiter beschleunigt. Beispielsweise verringert der Verlust glomerulärer Kapillaren bei Glomerulärer Sklerose den Blutfluss zu den distalen peritubulären Kapillaren mit einer weiteren Verringerung der Sauerstoffversorgung. In ähnlicher Weise kann eine CKD-assoziierte Anämie die Sauerstoffversorgung verringern und gleichzeitig eine Verengung der abführenden Arteriole nach sich ziehenintrarenalDie Aktivierung des Renin-Angiotensin-Aldosteron-Systems reduziert den Blutfluss zum tubulointerstitiellen Bereich mit ähnlichen Auswirkungen auf die Sauerstoffversorgung (28). Da dies wahrscheinlich gemeinsame Mechanismen im Fortschreiten von sindNierenerkrankungenwird Hypoxie als verbindender Weg zum Endstadium angesehenNierenerkrankung (28, 29).

DasNierensind physiologisch mit kompensatorischen Reaktionen auf Hypoxie ausgestattet. Zu den Schutzsystemen gehören die Aktivierung des Hypoxie-induzierten Faktors -1a (HIF-1a), der die Expression von Erythropoietin zur Erhöhung der Erythrozytenzahl stimulieren kann, und die Induktion des vaskulären endothelialen Wachstumsfaktors (VEGF). zur Induktion von Angiogenese (30), die beide helfen, Sauerstoff an hypoxische periphere Gewebe abzugeben. Diese kompensatorischen Reaktionen können sich jedoch unter verschiedenen pathologischen Bedingungen als schädlich erweisen. Insbesondere könnte HIF unter anhaltender Hypoxie bei CKD profibrotisch werden (31). Der Mechanismus ist wahrscheinlich an der Fähigkeit von HIF beteiligt, die Glykolyse gegenüber der mitochondrialen Atmung zu begünstigen und die zu induzieren
Produktion von endogenem Fruchtzucker (32, 33). Dennoch ist es im Rahmen einer chronischen Hypoxie wahrscheinlich, dass die Mitochondrienfunktion zunehmend reduziert wird, so dass ein Wechsel zur Glykolyse erforderlich ist.
DER WARBURG-EFFEKT IST AN CNE BETEILIGTDie Mitochondrien sind seit langem als Ort erhöhten oxidativen Stresses bei Diabetes anerkannt, und eine abweichende Aktivierung von Mitochondrien könnte auch eine Schlüsselrolle bei diabetischen Komplikationen spielen (34–36), obwohl einige Kontroversen bestehen bleiben (37). Jüngste Erkenntnisse haben jedoch gezeigt, dass die mitochondriale Funktion bei Diabetes eher unterdrückt ist und die Wiederherstellung der normalen mitochondrialen Gesundheit verbessert wirdNieren-, kardiovaskuläre und neuronale Ergebnisse (38–42). Übereinstimmend mit diesen Erkenntnissen haben experimentelle Studien gezeigt, dass glykolytische Zwischenprodukte und Enzyme hochreguliert sindNiereKortex bei Typ-2-Diabetes (42). In ähnlicher Weise waren Metaboliten im mitochondrialen Citratzyklus bei Patienten mit diabetischer Nephropathie im Vergleich zu gesunden Kontrollpersonen signifikant reduziert (43). Diese Daten legen nahe, dass die aktivierte Glykolyse die mitochondriale Funktion dominiert und eine pathologische Rolle bei der diabetischen Nephropathie spielt.
Es gibt auch Hinweise darauf, dass es bei anderen Arten von CNI zu einer Verschiebung von oxidativem Stress zur Glykolyse kommen kann. Ein Beispiel ist die autosomal-dominante polyzystischeNierenerkrankung(ADPKD), die durch Loss-of-Function-Mutationen in PDK1 oder PKD2 verursacht wird (44). Rowe et al. fanden heraus, dass kultivierte embryonale Maus-Fifibroblasten (MEFs), die von den Pkd-/--Mäusen stammten, vorzugsweise eine höhere Menge an Glucose verwerteten, aber eine höhere Menge an Lactat in das Kulturmedium ausschieden als Zellen von Wildtyp-Mäusen (45). Darüber hinaus produzierten Pkd-/-MEFs einen höheren ATP-Gehalt, der mit der Hochregulierung von Glykolyseenzymen verbunden war und nur eine geringe Wirkung durch Oligomycin, einen Inhibitor der mitochondrialen ATP-Synthese, hatte, was darauf hindeutet, dass ATP durch Glykolyse, aber nicht durch Mitochondrien produziert wird Atmung. Ebenso fehlt der Maus Pkd in derNieren-Tubuli zeigten als Mausmodell für ADPKD eine Aktivierung der Glykolyse, während die Blockierung der Glykolyse mit 2DG, einem Glukoseanalog, erfolgreich die tubuläre Zellproliferation dämpfte, was zu einer Verringerung von führteNiereGröße und Zystenbildung (45, 46).
Eine Verschiebung zur Glykolyse wurde auch in einem Modell mit einseitiger Harnleiterobstruktion und bei einer mit TGF-b1- behandelten Person beobachtetNieren-Fifibrose-Modell. Insbesondere haben Ding et al. fanden heraus, dass die Aktivierung von Myofifibroblasten in derNierenwurde mit einer erhöhten Glukoseaufnahme und Laktatproduktion in Verbindung gebrachtNierendie durch Blockieren der Glykolyse durch 2-Desoxy-Glucose-Behandlung abgeschwächt werden könnte. Es wurde dann gezeigt, dass dies einen TGF b1--abhängigen Stoffwechselschalter darstellt, der die Glykolyse gegenüber der mitochondrialen Atmung begünstigt. Diese Daten deuten darauf hin, dass der Warburg-Effekt bei diesem Prozess eine Schlüsselrolle spielen könnteNieren-Fifibrose (47).

FRUCTOSE ALS MECHANISMUS ZUR INDUZIERUNG DES WARBURG-EFFEKTS BEI CNEDie Beobachtung, dass CKD mit einer Verschlechterung einhergehtintrarenalIschämie und Hypoxie könnten große Auswirkungen auf habenintrarenalStoffwechsel. Wie bereits erwähnt, stimuliert Hypoxie-assoziiertes HIF-1a die endogene Fruktoseproduktion und den Stoffwechsel. Parket al. untersuchten die Rolle von Fructose bei Nacktmullen, die längere Zeit unter hypoxischen Bedingungen überleben können, und fanden heraus, dass ein Mechanismus für die Toleranz gegenüber Hypoxie ihrer Fähigkeit zugeschrieben wird, endogen Fructose zu produzieren (32). Fruktose kann sogar unter Bedingungen mit wenig Sauerstoff metabolisiert werden, während sie mehrere biosynthetische Zwischenprodukte über mehrere Wege bereitstellen kann, um den Bedarf an Zellschutz zu decken (wie im obigen Abschnitt diskutiert).
Während Fructose jedoch wahrscheinlich vor Ischämie schützend wirken sollte, kann Fructose unter pathologischen Bedingungen schädliche Folgen haben. Mirtschink et al. fanden heraus, dass Fructokinase unter einer niedrigen Sauerstoffbedingung als HIF-Zielgen hochreguliert wurde, aber es trug zur Entwicklung des hypertrophen Herzens bei Mäusen bei, während die Herzhypertrophie bei Mäusen mit Fructokinase-Mangel blockiert wurde (33). In demNieren,Endogene Fructose könnte bei mehreren pathologischen Zuständen schädlich sein. Andres-Hernando et al. zeigten, dass eine transiente Ischämie in der Lage war, endogene Fruktose im Blut zu induzierenNieren-Tubuli, und es wurde erneut festgestellt, dass es schädlich ist, da das Blockieren des Fructosestoffwechsels den Fructosestoffwechsel verbessertNierenverletzungin einem Ischämie-Reperfusions-Mausmodell (5).
Eine weitere Einstellung, bei der die endogene Fruktoseproduktion in derNierehoch ist bei diabetischer Nephropathie. Bei der diabetischen Nephropathie gibt es nicht nurintrarenalIschämie und Hypoxie, aber hoher Glukosetransport in den proximalen Tubuli. Die lokalen Erhöhungen der Glukose sind ein weiterer wichtiger Stimulus für die Fruktoseproduktion. Da Fructokinase in den proximalen Tubuli (S1 bis S3) vorhanden ist, ist es wahrscheinlich, dass die endogene Fructoseproduktion hoch ist (7). Tatsächlich wurde festgestellt, dass die Blockierung von Fructokinase bei experimenteller diabetischer Nephropathie (6) schützt.
Die proximalen tubulären Zellen bevorzugen normalerweise Lipide gegenüber Glukose zur Energieerzeugung, daher wurde bei diesem Zelltyp keine Glykolyse durchgeführt. Dies würde durch ein Ungleichgewicht der enzymatischen Aktivierungen für die Glykolyse gegenüber denen für die Glukoneogenese erklärt (18). Da die proximalen Tubuluszellen der Hauptort des Fruktosestoffwechsels in der sindNiereDa dort überwiegend Fructokinase exprimiert wird, ist der Fructosestoffwechsel physiologisch mit der Glukoneogenese, nicht aber mit der Glykolyse verknüpft (18). Dies ist jedoch bei beschädigten Tubuli nicht der Fall. Tatsächlich sind die beschädigten proximalen Tubuluszellen oft mit mitochondrialen Veränderungen verbunden, was zu einer metabolischen Umstellung von mitochondrialer oxidativer Phosphorylierung auf Glykolyse mit verstärkter Expression von Glykolyseenzymen führt (48). Wichtig ist, dass die Glucokinase-Aktivität verstärkt wird, wenn Fructose mit Glucose metabolisiert wird (49–52).
KÖNNTEN DIE VORTEILHAFTEN WIRKUNGEN VON SGLT2-INHIBITOREN BEI DIABETISCHER UND NICHT-DIABETISCHER CNE AUF DIE VERHINDERUNG EINER STOFFWECHSELSCHALTUNG ZUR GLYKOLYSE ZURÜCKZUFÜHREN SEIN?SGLT2-Hemmer haben kürzlich die Aufmerksamkeit von Klinikern und Forschern wegen ihrer großen therapeutischen Vorteile auf sich gezogen, die über die glykämische Kontrolle sowohl bei Nicht-Diabetikern als auch bei Diabetikern hinausgehenNierenerkrankungenund bei den kardiovaskulären Komplikationen im Zusammenhang mit CKD (53, 54). Während die genauen Mechanismen unklar bleiben, haben neuere Studien gezeigt, dass die schützenden Wirkungen auf die Verhinderung des metabolischen Wechsels von Lipidoxidation zu Glykolyse zurückzuführen sein könnten, da eine abweichende Glykolyse wahrscheinlich mit einer epithelialen zu mesenchymalen Transformation proximaler Tubuluszellen bei Diabetikern verbunden war Nephropathie (55, 56). Darüber hinaus können SGLT2-Hemmer reduzierenintrarenalwirken, indem sie die Glukoseaufnahme blockieren und dadurch reduzierenintrarenalHypoxie mit der Blockierung der HIF-1a-Akkumulation und mit der Verhinderung einer Reduktion von Klotho, Ereignisse, von denen erwartet wird, dass sie die Glykolyse reduzieren (57, 58). Ein zusätzlicher Schutzeffekt, der durch die SGLT2-Hemmung ausgeübt wird, ist die chronische Verschiebung der Brennstoffverwertung hin zu fetthaltigen Substraten, um eine signifikante Erhöhung der Lipolyse und Ketogenese zu induzieren (59). Der Anstieg des Ketongehalts deutet auch auf einen Anstieg der b-Oxidation und eine Verringerung der Glykolyserate hin (60), was sowohl die kardioprotektiven als auch die nephroprotektiven Wirkungen erklären könnte (61). Die Stimulation von AMPK und Sirtuin-1 ist wahrscheinlich ein weiterer Mechanismus für die Schutzwirkung von SGLT2-Inhibitoren (62).
Eine der Hauptwirkungen von SGLT2-Inhibitoren besteht darin, die Absorption von Glukose in die S1- und S2-Segmente des proximalen Tubulus zu blockieren, und dies sollte dazu beitragen, die Menge an Glukose, die in Fruktose umgewandelt wird, zu reduzieren. Da an der Stelle (15) etwas Fructokinase exprimiert wird, könnte dies einen Weg darstellen, den Warburg-Effekt zu blockieren. In Übereinstimmung mit diesem Vorschlag verringert das Blockieren von Fructokinase die Schwere der diabetischen Nephropathie bei Mäusen (6, 7). Wir haben jedoch zuvor vorgeschlagen, dass die Blockierung der Glukoseaufnahme in die S1- und S2-Segmente des proximalen Tubulus die Menge an Glukose, die vom S3-Segment reabsorbiert wird, erhöhen könnte, was zu einer ausreichenden Fructoseerzeugung führen könnte, die zu einer tubulären Metabolisierung durch Fructokinase führen könnte Verletzungen und akutNierenverletzung(63). In der Gesamtbilanz wäre jedoch zu erwarten, dass der Einsatz von SGLT2-Inhibitoren protektiv für die istNiere.
KONTROVERSE ROLLE FÜR GLYKOLYSE VS. OXIDATIVER STOFFWECHSEL BEI DER MAKROPHAGEN-AKTIVIERUNGMakrophagen sind an Fruktose-induzierten beteiligtNieren-Entzündung (14, 15, 22). Es gibt zwei Hauptmakrophagen-Phänotypen: einen entzündungsfördernden (M1) Phänotyp, der auf der Glykolyse beruht, und einen entzündungshemmenden/auflösenden (M2) Phänotyp, der auf oxidativer Phosphorylierung beruht (64, 65). Da Makrophagen Glut5 auf ihrer Oberfläche exprimieren (66) und Fruktose Makrophagen dazu anregt, entzündungsfördernde Zytokine freizusetzen (67, 68), könnte Fruktose aufgrund ihrer Fähigkeit, die Glykolyse zu stimulieren, ein idealer Brennstoff für die M1-Makrophagen sein. Obwohl mehrere Studien darauf hindeuten, dass die mitochondriale Atmungskette auch in entzündlichen M1-Makrophagen aktiv ist, kann sie dazu dienen, reaktive Sauerstoffspezies zu produzieren, um infektiöse Bakterien abzutöten, anstatt die ATP-Synthese zu stimulieren (69).

Im Gegensatz dazu zeigte eine kürzlich durchgeführte Studie, dass der oxidative Metabolismus, aber nicht die Glykolyse, eine dominierende Rolle der Makrophagenaktivierung bei fructoseinduzierten Entzündungen spielt, da die Blockierung der oxidativen Phosphorylierung, aber nicht die Hemmung der Glykolyse, die Freisetzung von entzündungsfördernden Zytokinen unterdrückt (67). Eine wichtige Erkenntnis war, dass Fruktose die Glutaminaufnahme stimuliert, um den TCA-Zyklus zu aktivieren, was zu einer mTORC1-Aktivierung für die Freisetzung entzündlicher Zytokine in menschlichen Monozyten und Mausmakrophagen führt. Während der Fruktosestoffwechsel Aconitase hemmt und daher den TCA-Zyklus unterdrückt, liefert der Glutaminstoffwechsel a-Ketoglutarat, das diesen Schritt umgehen kann, wodurch eine oxidative Phosphorylierung stattfinden kann (70, 71).
Angesichts dieser Tatsachen verwenden Makrophagen wahrscheinlich entweder Glykolyse oder oxidative Phosphorylierung für ihre Aktivierung, und der genaue Mechanismus, wie Makrophagen Stoffwechselwege auswählen, bleibt unklar. Eine mögliche Erklärung ist, dass die Sauerstoffverfügbarkeit eine Determinante ist, da die Aktivität der Cytochrom-C-Oxidase-Aktivität abnimmt, wenn die Sauerstoffkonzentration unter 1,0 mM fällt (72). Ebenso haben Semba et al. untersuchten kürzlich auch die Rolle von Sauerstoff bei der Migration von Makrophagen und zeigten, dass bei schwerer Hypoxie die Glykolyse dominant ist, während die Cytochrom-C-Oxidase-Aktivität stark blockiert ist (73). Die Cytochrom-c-Aktivität schaltet sich wiederum bei Verfügbarkeit von Sauerstoff ein, und die Glykolyse wird vollständig durch die oxidative Phosphorylierung unter aeroben Bedingungen ersetzt.
Zusammengenommen legen diese Studien nahe, dass Makrophagen für ihre Aktivierung sowohl von der Glykolyse als auch von der oxidativen Phosphorylierung abhängen und die Auswahl der Stoffwechselwege teilweise von der Sauerstoffverfügbarkeit abhängen kann. Es ist wahrscheinlich, dass die Glykolyse die M1-Makrophagenaktivierung unter hypoxischen Bedingungen antreibt, während die oxidative Phosphorylierung unter aeroben Bedingungen verwendet wird (73). Diese Studien legen nahe, dass der Fruktosestoffwechsel auch durch die Sauerstoffverfügbarkeit beeinflusst werden könnte, so dass die Aktivierung des Stoffwechselwegs in Makrophagen sowohl durch die Fruktosekonzentration als auch durch die Sauerstoffgehalte bestimmt werden könnte.
SCHLUSSFOLGERUNGENUnsere Studien deuten darauf hin, dass Fructose bei CNE eine Rolle spielen könnte. Dies könnte sekundär zu einer übermäßigen Aufnahme von Nahrungsfruktose aus der Nahrung auftreten. Es könnte jedoch auch eine Folge der endogenen Fruktoseproduktion sein, die von getrieben wirdintrarenalIschämie oder erhöhter Glukosehandel. Schließlich kann die Unterdrückung dieser Signalwege die schützende Wirkung von SGLT2-Inhibitoren sowohl bei diabetischer als auch bei nicht-diabetischer CKD erklären.
