GLP-1-Rezeptoragonisten bei diabetischer Nierenerkrankung: Aktuelle Erkenntnisse und zukünftige Richtungen
Jul 14, 2023
Abstrakt
Mit dem Aufkommen verschiedener Klassen von blutzuckersenkenden Mitteln wird bei der Diabetesbehandlung die Auswahl des geeigneten Arzneimittels für jeden Patienten immer wichtiger. Unter den Arzneimitteln auf Inkretinbasis sind Glucagon-ähnliche Peptid-1-Rezeptoragonisten (GLP-1) eine vielversprechende Therapieoption für Patienten mit diabetischer Nierenerkrankung (DKD). Mehrere kardiovaskuläre Outcome-Studien haben gezeigt, dass GLP-1-Rezeptor-Agonisten über ihre blutzuckersenkende Wirkung hinaus positive Auswirkungen auf die kardiorenalen Outcomes bei Patienten mit Typ-2-Diabetes mellitus (T2DM) haben. Die renalschützende Wirkung von GLP-1-Rezeptoragonisten resultiert wahrscheinlich aus ihrer direkten Wirkung auf die Niere, zusätzlich zu ihren indirekten Wirkungen, die herkömmliche Risikofaktoren für DKD verbessern, wie z. B. die Senkung des Blutzuckerspiegels, des Blutdrucks und des Körpergewichts . Die Hemmung von oxidativem Stress und Entzündungen sowie die Induktion von Natriurese sind wichtige renoprotektive Mechanismen von GLP-1-Analoga. Erste Erkenntnisse aus der Entwicklung von Zwei- und Dreifachkombinationswirkstoffen deuten darauf hin, dass GLP-1-Rezeptoragonisten wahrscheinlich zu beliebten Behandlungsoptionen für Patienten mit T2DM werden.
Schlüsselwörter
Diabetische Nephropathien, Glucagon-ähnliches Peptid 1, Typ-2-Diabetes mellitus
Klicken Sie hier, um den Cistanche-Extrakt zu kaufen
Einführung
Die Zahl der Patienten mit Diabetes mellitus (DM) nimmt weltweit weiter zu und DM ist die Hauptursache für chronische Nierenerkrankungen (CKD) und Nierenerkrankungen im Endstadium (ESRD) [1]. In Korea lag die Prävalenz von Diabetes bei Erwachsenen über 30 Jahren im Jahr 2018 bei 13,8 Prozent [2], und bis 2030 soll sie bei Männern 29,2 Prozent und bei Frauen 19,7 Prozent betragen [3]. Die Gesamtzahl der neuen Patienten, die eine Nierenersatztherapie (RRT) wegen terminaler Niereninsuffizienz begannen, stieg von 10,000 im Jahr 2011 auf 18.642 im Jahr 2019 [4], und der Anteil der Patienten mit DM als zugrundeliegender Ursache der terminalen Niereninsuffizienz stieg von 2011 auf 18.642 19,5 Prozent im Jahr 1992 auf 50,6 Prozent im Jahr 2012 [5], was DM zur häufigsten Ursache für terminale Niereninsuffizienz in Korea macht [4]. Trotz der Fortschritte in der Medizintechnik und den Behandlungen steigt der Bedarf an RRT weltweit und wird sich bis 2030 im Vergleich zu 2010 voraussichtlich mehr als verdoppeln [6].
Die diabetische Nierenerkrankung (DKD) ist die Hauptursache für Morbidität und Mortalität bei Diabetes [7,8]. Daher ist es von entscheidender Bedeutung, den Ausbruch und das Fortschreiten der DKD zu hemmen, unter anderem durch die Entwicklung therapeutischer Ansätze zur Vorbeugung oder Verzögerung. Die Kontrolle von Blutzucker und Blutdruck mithilfe von Angiotensin-Converting-Enzym-Inhibitoren oder Angiotensin-Rezeptor-Blockern ist das aktuelle Ziel bei der DKD-Behandlung [9], und es werden keine speziellen Medikamente oder anderen Therapieoptionen weit verbreitet, um das Fortschreiten der DKD zu verzögern. Mehrere kardiovaskuläre Outcome-Studien (CVOTs) haben jedoch gezeigt, dass Natrium-Glucose-Cotransporter-2-Inhibitoren (SGLT2) und Glucagon-like-Peptid-1-Rezeptoragonisten (GLP-1) positive Auswirkungen auf kardiorenale Outcomes haben, insbesondere bei Patienten mit Typ 2 DM (T2DM), bei denen ein hohes Risiko für Herz-Kreislauf-Erkrankungen (CVD) besteht [10–12]. Basierend auf den Ergebnissen klinischer Studien empfehlen die aktuellen Richtlinien der American Diabetes Association und der Korean Diabetes Association, dass Ärzte die Verschreibung von SGLT2-Inhibitoren oder GLP-1-Rezeptor-Agonisten nach Metformin als Teil der glukosesenkenden Therapie für Patienten mit T2DM in Betracht ziehen und CKD [13,14]. In diesem Übersichtsartikel konzentrieren wir uns auf GLP-1-Agonisten und diskutieren die klinischen und präklinischen Beweise für ihre nephroprotektiven Wirkungen und die möglichen Mechanismen, die diesen Wirkungen zugrunde liegen.
Physiologie und metabolische Wirkungen des Glucagon-ähnlichen Peptids 1
Die orale Aufnahme von Glukose führt aufgrund des Vorhandenseins von Darmhormonen, den sogenannten Inkretinen, zur Sekretion von mehr Insulin als bei einer Injektion von Glukose [15]. Gastrointestinales Peptid (GIP) und die GLPs (GLP-1, GLP-2) sind Inkretinhormone, die von enteroendokrinen L-Zellen des distalen Dünndarms und Dickdarms produziert werden [16]. Beim Menschen liegt die Nüchternkonzentration des Gesamt-GLP-1 zwischen 5 und 10 pmol/L und kann als Reaktion auf Mahlzeiten auf 40–50 pmol/L ansteigen [17]. Die Plasmakonzentration von biologisch aktivem, intaktem GLP-1 ist viel niedriger als die (Fasten,<2 pmol/L; peak postprandial concentrations, 5–10 pmol/L) [18].
Die GLP-1-Freisetzung nach einer Mahlzeit erfolgt zweiphasig. Ein anfänglicher schneller Anstieg des zirkulierenden GLP-1-Spiegels tritt 15 bis 30 Minuten nach einer Mahlzeit auf, gefolgt von einem zweiten geringfügigen Höhepunkt nach 90 bis 120 Minuten [19,20]. Der schnelle Anstieg der GLP-1-Sekretion nach den Mahlzeiten hängt mit der proximal-distalen Schleife zusammen, die durch Neurotransmitter wie Acetylcholin und Gastrin-freisetzende Peptide reguliert wird [21]. Es wird angenommen, dass der zweite spätere Höhepunkt von GLP-1 auftritt, wenn aufgenommene Nährstoffe durch das Lumen wandern und direkt mit distalen L-Zellen interagieren [22,23].
Natives GLP-1 hat aufgrund der Spaltung durch Dipeptidylpeptidase IV (DPP IV)-Enzyme und der renalen Elimination eine extrem kurze Halbwertszeit von weniger als 2 Minuten [24].
DPP IV-Enzyme spalten die aktiven Formen von GLP-17-36 und GLP-17-37, um inaktives GLP-19-36 bzw. GLP-19-37 zu produzieren, die eine geringe Affinität für GLP{{4) aufweisen }}-Rezeptor [25,26]. Nur 10 bis 15 Prozent des sezernierten GLP-1 erreichen die Bauchspeicheldrüse über den systemischen Kreislauf [25], und sowohl die aktive als auch die inaktive Form von GLP-1 werden über die Nieren schnell aus dem Kreislauf ausgeschieden. Obwohl der anfängliche DPP IV-vermittelte Abbau von GLP-1 nicht durch eine Beeinträchtigung der Nierenfunktion beeinflusst wird, ist die GLP-1-Clearance bei Patienten mit Niereninsuffizienz verzögert [24]. Beim Menschen wird der GLP-1-Rezeptor in der Bauchspeicheldrüse, der Lunge, dem Gehirn, den Nieren, dem Magen und dem Herzen exprimiert, jedoch nicht in der Leber, dem Skelettmuskel oder dem Fettgewebe [27]. Durch die Bindung zwischen GLP-1 und seinem Rezeptor wird die Adenylatcyclase aktiviert, was zu einem Anstieg des zyklischen AMP-Spiegels und des zytoplasmatischen Ca plus 2 führt, was die Insulinsekretion induziert [28]. Zusätzlich zu der kurzfristigen Wirkung von GLP-1, die glukoseabhängige Stimulation der Insulinsekretion zu verstärken, steigert die kontinuierliche GLP-1-Aktivierung auch die Insulinsynthese [29] und moduliert die Zellproliferation [30]. und hemmt die Zellapoptose [31] und die Glucagonfreisetzung [32]. Inkretinhormone verringern außerdem die Magenentleerung [33], hemmen die Nahrungsaufnahme [34] und erhöhen die Natriurese und Diurese [35,36].

Cistanche tubulosa
Klassifizierung von Glucagon-ähnlichen Peptid-1-Rezeptoragonisten
GLP-1-Rezeptoragonisten haben zwei Hauptgerüststrukturen und werden als Exendin-4-- oder humane GLP-1--basierte Verbindungen klassifiziert [37]. Sie werden in kurz- und langwirksame Wirkstoffe unterteilt und einige Formulierungen werden mit Insulin gemischt (Tabelle 1). Exendin-4 ist ein Protein, das 1992 aus dem Speichel der Gila-Monsterechse (Heloderma Suspectum) isoliert wurde [38]. Dieses Protein besteht aus 39 Aminosäuren und weist in der Basensequenz eine Ähnlichkeit von 53 Prozent mit nativem menschlichem GLP-1 auf. Exenatid und Lixisenatid basieren auf der Struktur von Exendin-4. Exenatide ist eine rekombinante Form des Peptids Exendin-4 und war der erste GLP-1-Rezeptoragonist, der für die T2DM-Behandlung entwickelt wurde. Lixisenatid ist ein Exendin-4-Analogon mit zusätzlich sechs Lysinen am C-Terminus, was ihm eine längere Halbwertszeit als Exenatid verleiht. Diese Exendin-4--basierten Wirkstoffe haben relativ kurze Halbwertszeiten (~3 Stunden) und hemmen die Magenentleerung stark [39], was gastrointestinale Nebenwirkungen wie Übelkeit verursachen kann. Sie haben aber auch starke postprandiale antihyperglykämische Wirkungen und könnten möglicherweise schnell wirkendes Insulin zu den Mahlzeiten ersetzen [39]. Diese kürzer wirkenden Wirkstoffe sind aufgrund ihrer kurzen Halbwertszeit weniger wirksam bei der Senkung des Nüchternglukosespiegels.
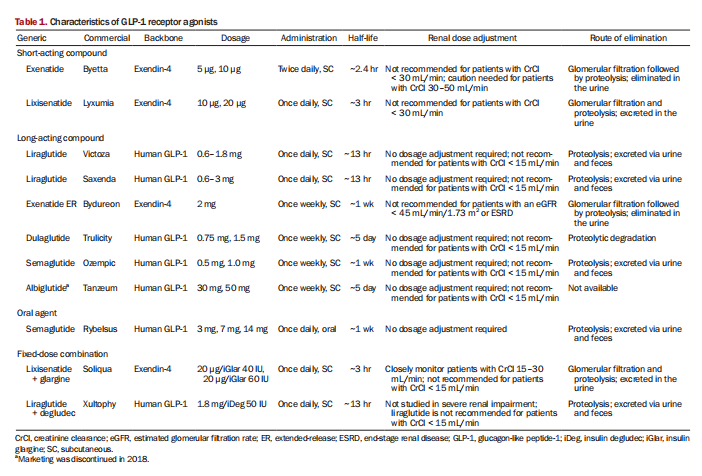
Menschliche GLP-1-basierte Agenten ähneln strukturell eher nativem GLP-1 als denen, die auf Exendin-4 basieren. Sie haben eine Aminosäurehomologie von 90 bis 97 Prozent mit endogenem menschlichem GLP-1 und eine verlängerte Halbwertszeit, die durch DPP IV-Resistenz und nichtkovalente Bindung an Serumalbumin verursacht wird. Diese länger wirkenden Wirkstoffe führen zu einer stärkeren Senkung des Nüchtern-Plasmaglukose- und Hämoglobin-A1c-Spiegels (HbA1c) als die kürzer wirkenden Wirkstoffe [39,40]. Die menschlichen GLP-1-Verbindungen sind Liraglutid, Albiglutid, Dulaglutid und Liraglutid, allesamt injizierbare Wirkstoffe. Albiglutid und Dulaglutid sind große Moleküle, die an große Proteine konjugiert sind, was ihre Halbwertszeit verlängert und eine einmal wöchentliche Verabreichung ermöglicht. Semaglutid ist sowohl in injizierbarer als auch oraler Form erhältlich. Da Albiglutid aus kommerziellen Gründen vom Markt genommen wurde, sind Liraglutid, Dulaglutid und Liraglutid (oral und subkutan) derzeit verfügbare, zugelassene humane GLP-1-Rezeptor-Agonisten.
Tabelle 1 zeigt die empfohlenen Anwendungen von GLP-1-Rezeptor-Agonisten entsprechend der geschätzten glomerulären Filtrationsrate (eGFR). Von menschlichem GLP-1 abgeleitetes Dulaglutid, Liraglutid und Semaglutid werden nicht über die Nieren ausgeschieden und können bis zu einer eGFR von 15 ml/min/1,73 m2 verwendet werden; Es liegen keine ausreichenden Erfahrungen vor, um den Einsatz dieser Wirkstoffe bei darunter liegenden eGFR-Werten zu empfehlen [41]. Umgekehrt sind Exenatid und Lixisenatid, die über die Nieren ausgeschieden werden, aufgrund des Risikos einer Akkumulation und Toxizität unter einer eGFR von 30 ml/min/1,73 m2 kontraindiziert [24]. Exenatide sollte bei Patienten mit einer eGFR von 30–50 ml/min/1,73 m2 mit Vorsicht angewendet werden (Tabelle 1).
Niereneffekte von Glucagon-ähnlichen Peptid-1-Rezeptoragonisten bei Patienten mit Typ-2-Diabetes mellitus
Mehrere CVOTs haben GLP-1-Rezeptoragonisten untersucht; jedoch konzentrierte sich keine auf den primären Endpunkt renaler Ereignisse; renale Ergebnisse wurden als sekundäre Ergebnisse nach primären kardiovaskulären Ergebnissen berichtet. Dieser Abschnitt konzentriert sich auf die renalen Ergebnisse der Behandlung mit GLP-1-Rezeptor-Agonisten, die in randomisierten kontrollierten Studien berichtet wurden (Tabelle 2).

Der erste CVOT für einen GLP-1-Rezeptoragonisten war die ELIXA-Studie (Evaluation of Lixisenatide in Acute Coronary Syndrome), deren Ergebnisse 2015 veröffentlicht wurden [42]. Insgesamt wurden 6.068 Teilnehmer mit T2DM, einem Myokardinfarkt oder instabiler Angina pectoris in der Vorgeschichte, einem durchschnittlichen HbA1c-Ausgangswert von 7,7 Prozent und einer mittleren Nachbeobachtungszeit von 25 Monaten eingeschrieben. Obwohl renale Ereignisse in der primären ELIXA-Studie nicht untersucht wurden, wurde eine explorative Analyse der renalen Ergebnisse durchgeführt [43]. Nach einer mittleren Nachbeobachtungszeit von 108 Wochen reduzierte Lixisenatid das Fortschreiten des Harn-Albumin-Kreatinin-Verhältnisses (UACR) bei Makroalbuminurie-Patienten und war mit einem geringeren Risiko einer neu auftretenden Makroalbuminurie verbunden, nach Anpassung an den Ausgangs- und Studien-HbA1c und andere traditionelle Nierenrisikofaktoren. Es wurden keine signifikanten Unterschiede in der eGFR-Abnahme zwischen den Behandlungsgruppen festgestellt. Diese Studie hatte im Vergleich zu den anderen Studien in Tabelle 2 eine kurze Nachbeobachtungszeit von 2 Jahren, einen hohen Prozentsatz an Teilnehmern unter Statintherapie und eine geringe Compliance mit der Medikation.
In der im Jahr 2016 veröffentlichten LEADER-Studie (Liraglutide Effect and Action in Diabetes: Evaluation of Cardiocular Outcome Results) [44] waren Teilnehmer mit T2DM entweder 50 Jahre alt oder älter mit mindestens eine Herz-Kreislauf-Erkrankung oder 60 Jahre oder älter mit mindestens einem kardiovaskulären Risikofaktor. Insgesamt waren 9.340 Teilnehmer mit einer mittleren Nachbeobachtungszeit von 3,8 Jahren eingeschrieben, und der durchschnittliche HbA1c-Ausgangswert betrug 8,7 Prozent. Ungefähr 23 Prozent der Teilnehmer hatten eine mittelschwere bis schwere CKD, was auf eine sehr risikoreiche Population schließen lässt. Bemerkenswert ist, dass an dieser Studie 220 Personen mit einer eGFR von 15–30 ml/min/1,73 m2 teilnahmen. Liraglutid senkte das Risiko des sekundären kombinierten renalen Endpunkts (neu auftretende Makroalbuminurie, anhaltende Serumkreatinin-Duplikation, Einleitung einer RRT oder Nierentod) um 22 Prozent (Hazard Ratio 0,78; 95-Prozent-Konfidenzintervall [KI] 0,67–0,92); p=0.003) [45]. Dieser Befund war in erster Linie auf eine Verringerung der neu aufgetretenen persistierenden Makroalbuminurie zurückzuführen. Diese Studie war die erste, die zeigte, dass ein GLP-1-Agonist kardiovaskuläre Vorteile hatte, obwohl er bei Patienten mit geringem kardiovaskulären Risiko möglicherweise nicht anwendbar war.
Der SUSTAIN{{0}} (Trial to Evaluate Cardiocular and Other Long-term Outcomes with Semaglutide in Subjects with Type 2 Diabetes) war der nächste CVOT, der ebenfalls im Jahr 2016 veröffentlicht wurde [46]. Insgesamt wurden 3.297 Patienten nach dem Zufallsprinzip eingeteilt, und 3.232 Patienten schlossen die Studie über eine mittlere Nachbeobachtungszeit von 2,1 Jahren ab. Bei 83 % der Teilnehmer wurde eine Herz-Kreislauf-Erkrankung, eine chronische Nierenerkrankung oder beides festgestellt, und der mittlere HbA1c-Wert der gesamten Studienpopulation betrug 8,7 %. Einmal wöchentlich verabreichtes Semaglutid bewirkte eine 36-prozentige Reduktion (HR, 0,64; 95-Prozent-KI, 0,46–0,88; p=0,005) des sekundären kombinierten renalen Endpunkts (neu auftretende Makroalbuminurie, Verdoppelung). von Serumkreatinin, eGFR von<45 mL/min/1.73 m2, initiation of RRT, or renal death). This result was mainly driven by a reduction in new-onset macroalbuminuria. Across the SUSTAIN 1–7 trials [47], semaglutide lowered albuminuria compared with placebo beginning as early as 16 weeks and lasting over the entire treatment period.
Die nächste Studie, die 2017 veröffentlicht wurde, war die EXSCEL-Studie (Exenatide Study of Cardiocular Event Lowering), um die Wirkung einer einmal wöchentlichen Exenatid-Retardfreisetzung (ER) auf kardiovaskuläre Ergebnisse bei Teilnehmern mit T2DM zu bewerten [48]. Insgesamt wurden 14.752 Patienten, von denen 73,1 Prozent eine frühere Herz-Kreislauf-Erkrankung hatten, durchschnittlich 3,2 Jahre lang beobachtet. Exenatide ER hatte in einer zusätzlichen Analyse der EXSCEL-Studiendaten keine signifikanten Auswirkungen auf die Nierenergebnisse [49]. Auch die zweimal tägliche Gabe von Exenatid hatte im Vergleich zu Insulin Glargin über den {{13}wöchigen Studienzeitraum keinen Einfluss auf eGFR oder Albuminurie [50].
Die kardiovaskulären Wirkungen von Albiglutid wurden bei Patienten mit T2DM und CVD in der 2018 veröffentlichten HARMONY-Studie (NCT02465515) [51] untersucht. Insgesamt waren 9.463 Teilnehmer mit einem mittleren HbA1c von 8,7 Prozent eingeschrieben; Dabei handelte es sich um eine relativ risikoreiche Population mit hohen Grundglukosewerten. Nach einer durchschnittlichen Nachbeobachtungszeit von 1,6 Jahren erbrachte Albiglutid keinen signifikanten Vorteil bei der Verlangsamung der eGFR-Abnahmerate.
Die renalen Ergebnisse der Dulaglutid-Behandlung wurden in zwei repräsentativen Studien untersucht. Die erste Studie war die AWARD{{0}}-Studie (NCT01621178), veröffentlicht im Jahr 2018 [52]. In diese Studie wurden 577 Teilnehmer mit T2DM und mittelschwerer bis schwerer CKD einbezogen. Eine einmal wöchentliche Injektion von Dulaglutid war im Vergleich zu Insulin Glargin über 52 Wochen mit einem deutlich geringeren Rückgang der eGFR verbunden. Der mittlere eGFR-Rückgang mit 1,5-mg Dulaglutid betrug etwa 10 Prozent des unter Insulin glargin beobachteten Werts (–0,5 ml/min/1,73 m2 im 1,{{ 19}}mg Dulaglutid-Gruppe im Vergleich zu –5,5 ml/min/1,73 m2 in der Insulin-Glargin-Gruppe). Dieser Zusammenhang zwischen Dulaglutid und einem verringerten eGFR-Rückgang war am deutlichsten bei Teilnehmern mit Makroalbuminurie. Eine weitere Studie über die Auswirkungen von injizierbarem Dulaglutid auf kardiovaskuläre Ergebnisse bei Typ-2-Diabetes war die REWIND-Studie (Researching Cardiocular Events with a Weekly Incretin in Diabetes) [53,54], die 2019 veröffentlicht wurde. Diese Studie sollte im Gegensatz zu den vorherigen Studien die Überlegenheit demonstrieren. Insgesamt 9,901 Teilnehmer mit T2DM wurden durchschnittlich 5,4 Jahre lang nachbeobachtet, ein längerer Zeitraum als in den vorherigen Studien. Diese Studie war insofern einzigartig, als die Teilnehmer ein geringes Risiko aufwiesen, mit einem durchschnittlichen HbA1c-Ausgangswert von 7,2 Prozent, einer mittleren eGFR von 74,9 ml/min/1,73 m2, einer Ausgangsprävalenz von CVD von 31,5 Prozent und einer Ausgangsprävalenz von Albuminurie von 35.{{ 60}} Prozent. Das kombinierte renale Ergebnis trat in der Dulaglutid-Gruppe deutlich seltener auf als in der Placebo-Gruppe (HR 0,85; 95-Prozent-KI 0,77–0,93; p=0 0,0004), und der größte Effekt war eine Verringerung der Entwicklung der Makroalbuminurie in der Dulaglutid-Gruppe (HR 0,77; 95-Prozent-KI 0,68–0,87; p < 0,0001).
Die PIONEER 6-Studie (Peptide Innovation for Early Diabetes Treatment) wurde entwickelt, um die kardiovaskulären Ergebnisse der einmal täglichen oralen Gabe von Semaglutid bei T2DM-Patienten mit hohem kardiovaskulärem Risiko zu bewerten [55]. Die Ergebnisse wurden 2019 veröffentlicht. An dieser Studie nahmen 3.183 Teilnehmer teil wurden im Median 15,9 Monate lang nachbeobachtet, was die kürzeste Dauer der in Tabelle 2 aufgeführten Studien darstellt. Allerdings wurde in dieser Studie kein renaler Endpunkt für die Bewertung vordefiniert.
Die jüngste CVOT für GLP-1-Agonisten war die AMPLITUDE-O-Studie (Effect of Efpeglenatide on Cardiovascular Outcomes) bei Patienten mit T2DM und einer Vorgeschichte von CVD oder CKD [56]; Die Ergebnisse wurden im Jahr 2021 veröffentlicht. Das einmal wöchentlich injizierbare Efpeglenatid ist ein neuer GLP-1-Rezeptoragonist auf Exendin-4--Basis. Insgesamt wurden 4.076 Teilnehmer eingeschrieben und durchschnittlich 1,81 Jahre lang nachbeobachtet. Im Vergleich zu Placebo führte Efpeglenatid zu einem um 32 Prozent geringeren Risiko eines kombinierten renalen Outcome-Ereignisses (vorkommende Makroalbuminurie, Anstieg der UACR um mehr als oder gleich 30 Prozent gegenüber dem Ausgangswert, anhaltende Abnahme der eGFR um mehr als oder gleich 40 Prozent, Beginn). von RRT oder anhaltender eGFR von<15 mL/min/1.73 m2 ), independently of baseline use of SGLT2 inhibitors or metformin and baseline eGFR (HR, 0.68; 95% CI, 0.57–0.79; p < 0.001). However, a kidney function outcome event, defined as a composite of a decrease in eGFR of at least 40% for ≥30 days, ESRD, or death from any cause, did not differ between the efpeglenatide group and the placebo group (HR, 0.77; 95% CI, 0.57–1.02; p = 0.07).

Cistanche-Ergänzung
Vorgeschlagene nephroprotektive Mechanismen von Glucagon-ähnlichen Peptid-1-Rezeptoragonisten
1 Indirekte Effekte durch Verbesserung herkömmlicher Risikofaktoren für diabetische Nierenerkrankungen
Hyperglykämie spielt eine entscheidende Rolle bei der Pathogenese von DKD [57,58] und GLP-1-Rezeptor-Agonisten haben starke glukosesenkende Wirkungen [59–62]. Die Richtlinien für die klinische Praxis „The Kidney Disease: Improving Global Outcomes (KDIGO) 2020“ empfehlen GLP-1-Rezeptoragonisten als ausgezeichnete Option für Patienten mit DKD, die ihr glykämisches Ziel nicht erreicht haben, oder als Alternative für Patienten, die Metformin oder andere Medikamente nicht vertragen SGLT2-Inhibitor [63]. Obwohl auch glukoseunabhängige Mechanismen betont werden, geht man davon aus, dass die antihyperglykämischen Wirkungen von GLP-1-Rezeptoragonisten zu deren nephroprotektiven Wirkungen bei Patienten mit DKD beitragen. Darüber hinaus induzieren GLP-1-Rezeptoragonisten eine Verringerung des Körpergewichts, des Blutdrucks und der Dyslipidämie, was ebenfalls zu ihrer antialbuminurischen Wirkung beitragen könnte [64,65].
In der LEADER-Studie [44] zeigte die Liraglutid-Gruppe eine Reduzierung des HbA1c um 0,4 Prozent im Vergleich zur Placebo-Gruppe. Der Gewichtsverlust war 2,3 kg höher und der systolische Blutdruck war 1,2 mmHg niedriger in der Liraglutid-Gruppe als in der Placebo-Gruppe. In der REWIND-Studie [54] hatten Teilnehmer der Gruppe mit einmal wöchentlicher Einnahme von 1,5-mg Dulaglutid einen um 0,61 Prozent niedrigeren HbA1c, ein um 1,46 kg geringeres Körpergewicht und einen um 1,7 mmHg niedrigeren systolischen Blutdruck als die Teilnehmer der Placebogruppe. In der SUSTAIN-6-Studie [46] war der mittlere HbA1c-Wert um 1,0 Prozentpunkte niedriger, das mittlere Körpergewicht sank um weitere 4,3 kg und der mittlere systolische Blutdruck war um 2,6 mmHg niedriger in der Gruppe, die einmal wöchentlich 1,0 mg Semaglutid erhielt, als in der Placebogruppe. In der PIONEER-5-Studie [55] war die einmal tägliche orale Gabe von Semaglutid (14 mg) dem Placebo bei der Senkung von HbA1c und Körpergewicht bei Patienten mit Typ-2-Diabetes überlegen. Die statistische Korrektur des HbA1c-Spiegels während des Versuchs, der Blutdruckänderung und der Abnahme des Körpergewichts veränderte jedoch nicht signifikant die beobachtete Abnahme der Albuminurie, die durch GLP-1-Rezeptoragonisten in mehreren CVOTs hervorgerufen wurde [66], was auf eine schützende Wirkung auf die Nieren schließen lässt von GLP-1-Rezeptor-Agonisten sind nicht ausschließlich auf Verbesserungen der Risikofaktoren zurückzuführen.
Zusätzlich zu seinen Auswirkungen auf Körpergewicht, Blutdruck und Glukose reguliert GLP-1 auch den Fettstoffwechsel. Dyslipidämie ist ein starker Risikofaktor für CKD und DKD. Experimentelle Studien haben Daten geliefert, die die Annahme stützen, dass Lipidanomalien zur Entstehung und zum Fortschreiten glomerulärer Erkrankungen beitragen [67]. Eine systematische Überprüfung und Metaanalyse von 35 Studien zeigte, dass GLP-1-Rezeptoragonisten mit einer Senkung des Gesamt- und Low-Density-Lipoprotein-Cholesterin- und Triglyceridspiegels verbunden sind [68]. GLP-1 hemmt die Magenlipasesekretion [69] und die intestinale Lipoprotein- und Chylomikronenproduktion beim Menschen [70]. Die Signalübertragung des GLP-1-Rezeptors verringert den Triglyceridgehalt in der Leber und beeinträchtigt die Lipogenese in der Leber durch Stimulierung des AMP-aktivierten Proteinkinase-Signalwegs [71,72]. Es erhöht auch die periphere Nutzung von triglyceridreichen Lipoproteinen durch erhöhte Fettverbrennung und Aktivierung der Funktion des braunen Fettgewebes [73,74]. Es ist jedoch ungewiss, ob diese Wirkungen direkt zu den nephroprotektiven Wirkungen von GLP-1-Rezeptoragonisten beitragen.
2 Mögliche direkte Mechanismen, die für die renale Schutzwirkung von Glucagon-ähnlichen Peptid-1-Rezeptor-Agonisten verantwortlich sind
Der GLP-1-Rezeptor wird in der Nierenrinde und im Gefäßsystem sowie in den proximalen Tubuluszellen exprimiert [75,76], obwohl hinsichtlich der Rezeptorlokalisation in der Niere aufgrund des Mangels an Antikörpern mit hoher Empfindlichkeit und Spezifität weiterhin Unsicherheiten bestehen. Die Hemmung von oxidativem Stress und Entzündungen, die Induktion von Natriurese und die Verringerung des intraglomerulären Drucks sind potenzielle direkte Mechanismen, die den renalen Schutzwirkungen von GLP-1-Analoga zugrunde liegen (Abb. 1). Systemischer oxidativer Stress erhöht das Stadium einer beginnenden DKD [77]. Eine Studie an diabetischen Ratten ergab, dass rekombinantes menschliches GLP-1 den oxidativen Stress in den Glomeruli und glomerulären mikrovaskulären Endothelzellen durch Hemmung der Proteinkinase C und Aktivierung der Proteinkinase A (PKA) abschwächt [78]. Liraglutid reduzierte auch oxidativen Stress und Albuminurie bei Streptozotocin-induzierten Typ-1-DM-Ratten durch PKA-vermittelte Hemmung der renalen Nicotinamidadenindinukleotidphosphatoxidasen [79]. Es wurde gezeigt, dass Exendin-4 den Nrf2-Signalweg in glatten Gefäßmuskelzellen aktiviert, der eine Schlüsselrolle bei der Verhinderung von oxidativem Stress und der Aufrechterhaltung der Redoxhomöostase spielt [80,81].

Entzündungen spielen eine zentrale Rolle bei der Entstehung von DKD. Die zunehmenden experimentellen Daten deuten darauf hin, dass die entzündungshemmende Wirkung den nephroprotektiven Wirkungen von GLP zugrunde liegt-1. GLP-1-Rezeptoragonisten verringern die Produktion von proinflammatorischen Zytokinen, Adhäsionsmolekülen und profibrotischen Signalen [82–84]. Liraglutid hemmte die Aktivierung des renalen Tumornekrosefaktors (TNF)- -vermittelten Kernfaktors Kappa B (NF-κB) und die Aktivierung des Mitogen-aktivierten Proteinkinase-Signalwegs in den glomerulären Podozyten eines Mausmodells mit Adipositas-assoziierter Glomerulopathie [82]. Exendin-4 schwächte Albuminurie, glomeruläre Hyperfiltration, glomeruläre Hypertrophie und mesangiale Matrixexpansion ab, ohne den Blutzuckerspiegel bei diabetischen Ratten zu senken, indem es oxidativen Stress und die NF-κB-Aktivierung hemmte [83]. Beim Menschen reduzierte Exenatid die Erzeugung reaktiver Sauerstoffspezies und die Expression von NF-κB, TNF-, Interleukin-1, c-Jun N-terminaler Kinase-1, Toll-like-Rezeptor-4 und Suppressor des Zytokinsignals 3 bei adipösen Patienten mit T2DM, unabhängig vom Gewichtsverlust [84]. Exenatid reduzierte auch das hochempfindliche C-reaktive Protein um 61 Prozent [85] und verringerte die Ausscheidung des transformierenden Wachstumsfaktors im Urin- 1 und der Typ-IV-Kollagenausscheidung bei Patienten mit T2DM [86]. Die Behandlung mit Liraglutid war bei adipösen Patienten mit T2DM mit einem verringerten Spiegel an entzündlichen Zytokinen und einem Anstieg des Adiponektinspiegels im Serum verbunden [87]. Liraglutid verbesserte auch den oxidativen Stress, indem es die Glutathionkonzentration erhöhte und die Lipidhydroperoxid- und Hämoxygenase--1-Spiegel im Serum bei Patienten mit T2DM senkte, unabhängig von seinen blutzuckersenkenden Wirkungen [88].
Es wurde vermutet, dass die natriuretische Wirkung von GLP-1-Rezeptoragonisten der GLP-1-induzierten Blutdrucksenkung zugrunde liegt, über die bei großen CVOTs berichtet wird. GLP-1-vermittelte Natriurese und Diurese scheinen eine Umverteilung und Verringerung der Aktivität von Na plus /H plus Austauscher 3 (NHE3) zu beinhalten, der sich am Bürstensaum der proximalen Nierentubuli befindet [89]. GLP-1-Rezeptoragonisten phosphorylierten NHE3 an den PKA-Konsensusstellen Ser552 und Ser605 und verringerten so seine Aktivität [36]. GLP-1-Rezeptoragonisten steigerten auch die Natriurese und Diurese, indem sie den Nierenblutfluss bei Ratten erhöhten [90]. Humanstudien haben gezeigt, dass die GLP-1-Infusion die proximale tubuläre Natriumreabsorption verringert und die Angiotensin-II-Konzentration im Plasma senkt [91]. Darüber hinaus erhöhte eine einzelne subkutane Injektion von Liraglutid die Natriumausscheidung bei Menschen mit T2DM [92]. Die Hemmung von NHE3 durch GLP-1 könnte auch die glomeruläre Hämodynamik beeinflussen, indem es die tubuloglomeruläre Rückkopplung aktiviert. Der Anstieg der Natriumabgabe an die Macula densa aufgrund der geringen NHE3-Aktivität führt zu einer afferenten arteriolären Vasokonstriktion und einer geringeren glomerulären Hyperfiltration und einem geringeren Druck. Liraglutid ist mit einer akuten Verringerung der eGFR und einer anschließenden Stabilisierung im Laufe der Zeit verbunden, was darauf hindeutet, dass GLP-1 hämodynamische Auswirkungen auf die Nieren hat [93].

Herba Cistanche
Laufende Studien und in der Entwicklung befindliche Medikamentenkandidaten
Derzeit läuft die FLOW-Studie (NCT03819153) zur Bewertung der Wirkung von einmal wöchentlich verabreichtem Semaglutid auf das Fortschreiten einer Nierenfunktionsstörung. Das primäre renale Ergebnis umfasst eine anhaltende Verringerung der eGFR um mehr als oder gleich 50 Prozent oder eine anhaltende eGFR von<15 mL/min/1.73 m2, initiation of RRT, or death from kidney disease or CVD. This study recently began recruiting more than 3,000 T2DM patients with moderate/advanced CKD and albuminuria, and its estimated completion date is 2024. This trial will be the first to investigate the effects of a GLP-1 receptor agonist on primary kidney outcomes.
Darüber hinaus handelt es sich bei der SOUL-Studie (NCT03914326) um eine derzeit laufende CVOT-Studie zur Bewertung der Hypothese, dass orales Semaglutid das Risiko kardiovaskulärer Ereignisse bei T2DM-Patienten mit hohem Risiko für CVD senkt. In dieser Studie ist der zusammengesetzte renale Endpunkt ein sekundäres Ergebnis, das aus einer anhaltenden Verringerung der eGFR um mehr als oder gleich 50 Prozent oder einer anhaltenden eGFR von besteht<15 mL/min/1.73 m2, initiation of RRT, and renal death. Oral semaglutide received the approval of the U.S. Food and Drug Administration in September 2019.
Unter Polypharmakologie versteht man die Kombination mehrerer strukturell verwandter Hormone zu einer einzigen Einheit. Die Behandlung mit GLP-1/Glucagon-Dualagonisten führte bei Mäusen mit ernährungsbedingter Fettleibigkeit zu einem Gewichtsverlust und einer antihyperglykämischen Wirksamkeit, die der von GLP-1-selektiven Agonisten allein überlegen war [94]. GLP-1 und Glucagon sind strukturell ähnlich, und Glucagon wirkt auch auf den GLP-1-Rezeptor [95], was die Erwartung weckt, dass eine Kombination der beiden Medikamente wirksamer sein könnte als die Verwendung beider Medikamente an diesem eigen. Derzeit laufen mehrere klinische Phase-2-Studien mit GLP-1/Glucagon-Dualagonisten. Darüber hinaus haben duale GLP-1/GIP-Agonisten aufgrund der Fettacylierung oder PEGylierung längere Halbwertszeiten. Ein einmal wöchentlich einzunehmender GLP-1/GIP-Co-Agonist namens Tripeptid (LY3298176) war Dulaglutid in Bezug auf Gewichtsverlust und verbessertem HbA1c-Spiegel in einer Phase-2-Studie an Patienten mit T2DM überlegen [96]. Klinische Phase-1-Studien für GLP-1/Glucagon/GIP-Dreifachkombinationswirkstoffe wurden von Hanmi Pharmaceuticals (HM15211) und Novo Nordisk (NNC9204-1706) durchgeführt.
Es wurde festgestellt, dass GLP-1--basierte Kombinationstherapien größere metabolische Vorteile bieten als die Behandlung mit einer der beiden Verbindungen allein. Basierend auf der verbesserten Wirksamkeit von GLP-1/Glucagon- und GLP-1/GIP-Co-Agonisten ist es sinnvoll zu bestimmen, ob Dual- oder Triple-Agonisten möglicherweise eine größere Wirksamkeit bieten als die jeweiligen Monoagonisten. Verschiedene mögliche Kombinationen sind GLP-1 mit GLP-2 [97], Leptin [98], Gastrin [99], Amylin [100], Peptid YY [101], Cholecystokinin [102], Insulin [103 ], Adrenomedullin [104], Fibroblasten-Wachstumsfaktor 21 [105], Östrogen [106], Dexamethason [107], ein Proprotein-Konvertase-Subtilisin/Kexin-Typ-9-Antikörper [108], Melanocortin-4-Agonist [109], Farnesoid -x [110] oder ein SGLT2-Inhibitor [111]. Zukünftige Studien sind erforderlich, um zu bewerten, ob eine dieser Wirkstoffkombinationen eine nephroprotektive Wirkung hat, die der von GLP-1-Monoagonisten bei DKD-Patienten überlegen ist.

Standardisierte Cistanche
Schlussfolgerungen und Zukunftsperspektiven
GLP-1-Rezeptoragonisten sind vielversprechende Therapieoptionen für Patienten mit DKD, deren Vorteile über ihre blutzuckersenkende Wirkung hinausgehen. Diese Wirkstoffe scheinen überwiegend die Makroalbuminurie zu beeinflussen, wohingegen ihre Auswirkungen auf harte renale Endpunkte weniger klar sind. Obwohl diese Wirkstoffe bei CKD-Patienten mit einer eGFR von bis zu 15 ml/min/1,73 m2 eingesetzt werden können, muss die Sicherheit von GLP-1-Rezeptoragonisten bei DKD-Patienten mit CKD im Stadium 5 untersucht werden. Im Hinblick auf die künftige Forschungsrichtung sollten weitere Studien ähnlich der laufenden FLOW-Studie durchgeführt werden, um die primären Nierenergebnisse der Behandlung mit GLP-1-Rezeptor-Agonisten zu bewerten. Darüber hinaus muss untersucht werden, ob eine Kombinationsbehandlung mit GLP-1-Rezeptoragonisten und anderen Wirkstoffklassen mit positiven Auswirkungen auf die Niere bei Patienten mit DKD synergistische renoprotektive Wirkungen haben wird.
Verweise
1. Alicia RZ, Rooney MT, Tuttle KR. Diabetische Nierenerkrankung: Herausforderungen, Fortschritte und Möglichkeiten. Clin J Am Soc Nephrol 2017;12:2032–2045.
2. Jung CH, Son JW, Kang S, et al. Faktenblätter zu Diabetes in Korea, 2020: eine Einschätzung des aktuellen Stands. Diabetes Metab J 2021;45:1– 10.
3. Baik I. Prognose der Diabetes-Prävalenz bei koreanischen Erwachsenen für das Jahr 2030 unter Verwendung von Risikofaktoren, die aus nationalen Daten ermittelt wurden. Diabetes Metab J 2019;43:90–96.
4. Hong YA, Ban TH, Kang CY, et al. Trends bei epidemiologischen Merkmalen von Nierenerkrankungen im Endstadium aus dem Korean Renal Data System (KORDS) von 2019. Kidney Res Clin Pract 2021;40:52–61.
5. Jin DC, Han JS. Nierenersatztherapie in Korea, 2012. Kidney Res Clin Pract 2014;33:9–18.
6. Liyanage T., Ninomiya T., Jha V. et al. Weltweiter Zugang zur Behandlung von Nierenerkrankungen im Endstadium: eine systematische Überprüfung. Lancet 2015;385:1975–1982.
7. Li S, Wang J, Zhang B, Li X, Liu Y. Diabetes mellitus und ursachenspezifische Mortalität: eine bevölkerungsbasierte Studie. Diabetes Metab J 2019;43:319–341.
8. Afkarian M, Sachs MC, Kestenbaum B, et al. Nierenerkrankungen und erhöhtes Sterberisiko bei Typ-2-Diabetes. J Am Soc Nephrol 2013;24:302–308.
9. Yamazaki T, Mimura I, Tanaka T, Nangaku M. Behandlung der diabetischen Nierenerkrankung: Gegenwart und Zukunft. Diabetes Metab J 2021;45:11–26.
10. Kristensen SL, Rørth R, Jhund PS, et al. Kardiovaskuläre, Mortalitäts- und Nierenergebnisse mit GLP-1-Rezeptoragonisten bei Patienten mit Typ-2-Diabetes: eine systematische Überprüfung und Metaanalyse von Studien zu kardiovaskulären Ergebnissen. Lancet Diabetes Endocrinol 2019;7:776–785.
11. Neuen BL, Young T, Heerspink HJ, et al. SGLT2-Inhibitoren zur Prävention von Nierenversagen bei Patienten mit Typ-2-Diabetes: eine systematische Überprüfung und Metaanalyse. Lancet Diabetes Endocrinol 2019;7:845–854.
12. Oh TJ, Moon JY, Hur KY, et al. Natrium-Glucose-Cotransporter-2-Inhibitor zur Erhaltung der Nierenfunktion bei Patienten mit Typ-2-Diabetes mellitus: eine Konsenserklärung der Korean Diabetes Association und der Korean Society of Nephrology. Kidney Res Clin Pract 2020;39:269–283.
13. Hur KY, Moon MK, Park JS, et al. 2021 Richtlinien für die klinische Praxis bei Diabetes mellitus der Korean Diabetes Association. Diabetes Metab J 2021;45:461–481.
14. American Diabetes Association. 9. Pharmakologische Ansätze zur glykämischen Behandlung: Standards der medizinischen Versorgung bei Diabetes-2021. Diabetes Care 2021;44(Suppl 1): S111–S124.
15. Elrick H, Stimmler L, Hlad CJ Jr, Arai Y. Plasmainsulinreaktion auf orale und intravenöse Glukoseverabreichung. J Clin Endocrinol Metab 1964;24:1076–1082.
16. Eissele R, Göke R, Willemer S, et al. Glucagon-ähnliche Peptid-1-Zellen im Magen-Darm-Trakt und in der Bauchspeicheldrüse von Ratten, Schweinen und Männern. Eur J Clin Invest 1992;22:283–291.
17. Orskov C, Wettergren A, Holst JJ. Die Sekretion der Inkretinhormone Glucagon-ähnliches Peptid-1 und Magen-inhibitorisches Polypeptid korreliert mit der Insulinsekretion bei normalen Männern im Laufe des Tages. Scand J Gastroenterol 1996;31:665–670.
18. Kuhre RE, Wewer Albrechtsen NJ, Hartmann B, Deacon CF, Holst JJ. Messung der Inkretinhormone: Glucagon-ähnliches Peptid-1 und glukoseabhängiges insulinotropes Peptid. J Diabetes Complications 2015;29:445–450.
19. Rask E, Olsson T, Söderberg S, et al. Eine beeinträchtigte Inkretinreaktion nach einer gemischten Mahlzeit ist bei nichtdiabetischen Männern mit einer Insulinresistenz verbunden. Diabetes Care 2001;24:1640–1645.
20. Elliott RM, Morgan LM, Tredger JA, Deacon S, Wright J, Marks V. Glucagon-ähnliche Peptid-1 (7-36)amid- und glukoseabhängige insulinotrope Polypeptidsekretion als Reaktion auf die Nährstoffaufnahme in Mann: akute postprandiale und 24-h Sekretionsmuster. J Endocrinol 1993;138:159–166.
21.Roberge JN, Brubaker PL. Regulierung der intestinalen Proglucagon-abgeleiteten Peptidsekretion durch glukoseabhängiges insulinotropes Peptid in einer neuartigen enteroendokrinen Schleife. Endokrinologie 1993;133:233–240.
22. Lim GE, Brubaker PL. Sekretion des Glucagon-ähnlichen Peptids 1 durch die L-Zelle: der Blick von innen. Diabetes 2006;55(Suppl_2):S70–S77.
23. Plaisancie P, Bernard C, Chayvialle JA, Cuber JC. Regulierung der Amidsekretion des Glucagon-ähnlichen Peptids-1-(7-36) durch intestinale Neurotransmitter und Hormone im isolierten, gefäßdurchbluteten Dickdarm der Ratte. Endokrinologie 1994;135:2398–2403.
24. Meier JJ, Nauck MA, Kranz D, et al. Sekretion, Abbau und Eliminierung von Glucagon-ähnlichem Peptid 1 und Magen-inhibitorischem Polypeptid bei Patienten mit chronischer Niereninsuffizienz und gesunden Kontrollpersonen. Diabetes 2004;53:654–662.
25. Deacon CF, Johnsen AH, Holst JJ. Der Abbau des Glucagon-ähnlichen Peptids -1 durch menschliches Plasma in vitro führt zu einem N-terminal verkürzten Peptid, das in vivo ein wichtiger endogener Metabolit ist. J Clin Endocrinol Metab 1995;80:952–957.
26. Kieffer TJ, McIntosh CH, Pederson RA. Abbau des glukoseabhängigen insulinotropen Polypeptids und des verkürzten Glucagon-ähnlichen Peptids 1 in vitro und in vivo durch Dipeptidylpeptidase IV. Endokrinologie 1995;136:3585–3596.
27. Wei Y, Mojsov S. Gewebespezifische Expression des menschlichen Rezeptors für Glucagon-ähnliches Peptid-I: Gehirn-, Herz- und Pankreasformen haben die gleichen abgeleiteten Aminosäuresequenzen. FEBS Lett 1995;358:219–224.
28. Doyle ME, Egan JM. Wirkmechanismen des Glucagon-ähnlichen Peptids 1 in der Bauchspeicheldrüse. Pharmacol Ther 2007;113:546–593.
29. Wang Y, Egan JM, Raygada M, Nadiv O, Roth J, Montrose-Rafizadeh C. Glucagon-ähnliches Peptid-1 beeinflusst die Gentranskription und die Stabilität von Messenger-Ribonukleinsäuren von Komponenten des Insulinsekretionssystems in RIN {{ 4}} Zellen. Endokrinologie 1995;136:4910–4917.
30. Buteau J. GLP-1-Rezeptor-Signalisierung: Auswirkungen auf die Proliferation und das Überleben von Betazellen in der Bauchspeicheldrüse. Diabetes Metab 2008;34 Suppl 2:S73–S77.
31. Li Y, Hansotia T, Yusta B, Ris F, Halban PA, Drucker DJ. Die Signalübertragung des Glucagon-like-Peptid--1-Rezeptors moduliert die Betazell-Apoptose. J Biol Chem 2003;278:471–478.
32. Hare KJ, Knop FK, Asmar M, et al. Erhaltene Hemmwirkung von GLP-1 auf die Glucagonsekretion bei Typ-2-Diabetes mellitus. J Clin Endocrinol Metab 2009;94:4679–4687.
33. Little TJ, Pilichiewicz AN, Russo A, et al. Auswirkungen von intravenös verabreichtem Glucagon-ähnlichem Peptid-1 auf die Magenentleerung und intragastrische Verteilung bei gesunden Probanden: Beziehungen zu postprandialen glykämischen und insulinämischen Reaktionen. J Clin Endocrinol Metab 2006;91:1916–1923.
34. Toft-Nielsen MB, Madsbad S, Holst JJ. Die kontinuierliche subkutane Infusion von Glucagon-ähnlichem Peptid 1 senkt den Plasmaglukosespiegel und reduziert den Appetit bei Typ-2-Diabetikern. Diabetes Care 1999;22:1137–1143.
35. Asmar A, Cramon PK, Simonsen L, et al. Die Erweiterung des extrazellulären Flüssigkeitsvolumens deckt eine natriuretische Wirkung von GLP-1 auf: eine funktionelle GLP-1-Nierenachse beim Menschen. J Clin Endocrinol Metab 2019;104:2509–2519.
36. Crajoinas RO, Oricchio FT, Pessoa TD, et al. Mechanismen, die die diuretischen und natriuretischen Wirkungen des Inkretinhormons Glucagon-ähnliches Peptid vermitteln-1. Am J Physiol Renal Physiol 2011;301:F355–F363.
37. Trujillo JM, Nuffer W. GLP-1-Rezeptoragonisten für Typ-2-Diabetes mellitus: aktuelle Entwicklungen und neue Wirkstoffe. Pharmakotherapie 2014;34:1174–1186.
38. Drucker DJ, Nauck MA. Das Inkretinsystem: Glucagon-ähnliche Peptid-1-Rezeptoragonisten und Dipeptidylpeptidase-4-Inhibitoren bei Typ-2-Diabetes. Lancet 2006;368:1696–1705.
39. Meier JJ. GLP-1-Rezeptoragonisten zur individuellen Behandlung von Typ-2-Diabetes mellitus. Nat Rev Endocrinol 2012;8:728–742.
40. Neumiller JJ. Inkretin-Pharmakologie: Ein Überblick über die Inkretin-Wirkung und aktuelle Inkretin-basierte Therapien. Cardiovasc Hematol Agents Med Chem 2012;10:276–288.
41. Jespersen MJ, Knop FK, Christensen M. GLP-1-Agonisten für Typ-2-Diabetes: pharmakokinetische und toxikologische Überlegungen. Expertenmeinung Drug Metab Toxicol 2013;9:17–29.
42. Pfeffer MA, Claggett B, Diaz R, et al. Lixisenatid bei Patienten mit Typ-2-Diabetes und akutem Koronarsyndrom. N Engl J Med 2015;373:2247–2257.
43. Muskiet MH, Tonneijck L, Huang Y, et al. Lixisenatid und renale Ergebnisse bei Patienten mit Typ-2-Diabetes und akutem Koronarsyndrom: eine explorative Analyse der randomisierten, placebokontrollierten ELIXA-Studie. Lancet Diabetes Endocrinol 2018;6:859– 869.
44. Marso SP, Daniels GH, Brown-Frandsen K, et al. Liraglutid und kardiovaskuläre Ergebnisse bei Typ-2-Diabetes. N Engl J Med 2016;375:311–322.
45. Mann JF, Ørsted DD, Brown-Frandsen K, et al. Liraglutid und Nierenergebnisse bei Typ-2-Diabetes. N Engl J Med 2017;377:839–848.
46. Marso SP, Bain SC, Consoli A, et al. Semaglutid und kardiovaskuläre Ergebnisse bei Patienten mit Typ-2-Diabetes. N Engl J Med 2016;375:1834–1844.
47. Mann JF, Hansen T, Idorn T, et al. Auswirkungen von einmal wöchentlich subkutan verabreichtem Semaglutid auf die Nierenfunktion und -sicherheit bei Patienten mit Typ-2-Diabetes: eine Post-hoc-Analyse der randomisierten kontrollierten SUSTAIN 1-7-Studien. Lancet Diabetes Endocrinol 2020;8:880–893.
48. Holman RR, Bethel MA, Mentz RJ, et al. Auswirkungen von einmal wöchentlichem Exenatid auf kardiovaskuläre Ergebnisse bei Typ-2-Diabetes. N Engl J Med 2017;377:1228–1239.
49. Bethel MA, Mentz RJ, Merrill P, et al. Mikrovaskuläre und kardiovaskuläre Ergebnisse entsprechend der Nierenfunktion bei Patienten, die mit einmal wöchentlichem Exenatid behandelt wurden: Erkenntnisse aus der EXSCEL-Studie. Diabetes Care 2020;43:446–452.
50. Muskiet MH, Bunck MC, Heine RJ, et al. Exenatid zweimal täglich hat keinen Einfluss auf die Nierenfunktion oder Albuminurie im Vergleich zu titriertem Insulin Glargin bei Patienten mit Typ-2-Diabetes mellitus: eine Post-hoc-Analyse einer 52-wöchigen randomisierten Studie. Diabetes Res Clin Pract 2019;153:14–22.
51. Hernandez AF, Green JB, Janmohamed S, et al. Albiglutid und kardiovaskuläre Ergebnisse bei Patienten mit Typ-2-Diabetes und Herz-Kreislauf-Erkrankungen (Harmony Outcomes): eine doppelblinde, randomisierte, placebokontrollierte Studie. Lancet 2018;392:1519–1529.
52. Tuttle KR, Lakshmanan MC, Rayner B, et al. Dulaglutid versus Insulin Glargin bei Patienten mit Typ-2-Diabetes und mittelschwerer bis schwerer chronischer Nierenerkrankung (AWARD-7): eine multizentrische, offene, randomisierte Studie. Lancet Diabetes Endocrinol 2018;6:605–617.
53. Gerstein HC, Colhoun HM, Dagenais GR, et al. Dulaglutid und Nierenergebnisse bei Typ-2-Diabetes: eine explorative Analyse der randomisierten, placebokontrollierten REWIND-Studie. Lancet 2019;394:131–138.
54. Gerstein HC, Colhoun HM, Dagenais GR, et al. Dulaglutid und kardiovaskuläre Ergebnisse bei Typ-2-Diabetes (REWIND): eine doppelblinde, randomisierte, placebokontrollierte Studie. Lancet 2019;394:121–130.
55. Husain M, Birkenfeld AL, Donsmark M, et al. Orales Semaglutid und kardiovaskuläre Ergebnisse bei Patienten mit Typ-2-Diabetes. N Engl J Med 2019;381:841–851.
56. Gerstein HC, Sattar N, Rosenstock J, et al. Kardiovaskuläre und renale Ergebnisse mit Efpeglenatid bei Typ-2-Diabetes. N Engl J Med 2021;385:896–907.
57. Coca SG, Ismail-Beigi F, Haq N, Krumholz HM, Parikh CR. Rolle der intensiven Glukosekontrolle bei der Entwicklung renaler Endpunkte bei Typ-2-Diabetes mellitus: eine systematische Überprüfung und Metaanalyse der intensiven Glukosekontrolle bei Typ-2-Diabetes. Arch Intern Med 2012;172:761–769.
58. Tuttle KR, Bruton JL, Perusek MC, Lancaster JL, Kopp DT, DeFronzo RA. Einfluss einer strengen Blutzuckerkontrolle auf die hämodynamische Reaktion der Niere auf Aminosäuren und die Nierenvergrößerung bei insulinabhängigem Diabetes mellitus. N Engl J Med 1991;324:1626–1632.
59. Blonde L, Jendle J, Gross J, et al. Einmal wöchentliches Dulaglutid im Vergleich zu Insulin Glargin vor dem Schlafengehen, beide in Kombination mit prandialem Insulin Lispro, bei Patienten mit Typ-2-Diabetes (AWARD-4): eine randomisierte, offene Phase-3-Nicht-Minderwertigkeitsstudie. Lancet 2015;385:2057–2066.
60. Mosenzon O, Blicher TM, Rosenlund S, et al. Wirksamkeit und Sicherheit von oralem Semaglutid bei Patienten mit Typ-2-Diabetes und mittelschwerer Nierenfunktionsstörung (PIONEER 5): eine placebokontrollierte, randomisierte Phase-3a-Studie. Lancet Diabetes Endocrinol 2019;7:515–527.
61. Lingvay I, Catarig AM, Frias JP, et al. Wirksamkeit und Sicherheit von einmal wöchentlichem Semaglutid im Vergleich zu täglichem Canagliflozin als Zusatz zu Metformin bei Patienten mit Typ-2-Diabetes (SUSTAIN 8): eine doppelblinde, randomisierte kontrollierte Phase-3b-Studie. Lancet Diabetes Endocrinol 2019;7:834–844.
62. Nauck M, Rizzo M, Johnson A, Bosch-Traberg H, Madsen J, Cariou B. Einmal täglich Liraglutid versus Lixisenatid als Zusatz zu Metformin bei Typ-2-Diabetes: eine {{5}wöchige randomisierte kontrollierte klinische Studie Versuch. Diabetes Care 2016;39:1501–1509.
63. Nierenerkrankung: Verbesserung der globalen Ergebnisse (KDIGO) Diabetes-Arbeitsgruppe. KDIGO 2020-Leitlinie für die klinische Praxis zur Diabetesbehandlung bei chronischer Nierenerkrankung. Kidney Int 2020;98(4S): S1–S115.
64. Vitale M, Haxhi J, Cirrito T, Pugliese G. Nierenschutz mit Glucagon-ähnlichen Peptid-1-Rezeptoragonisten. Aktuelle Stellungnahme Pharmacol 2020;54:91–101.
65. Dalsgaard NB, Vilsbøll T, Knop FK. Auswirkungen von Glucagon-ähnlichen Peptid--1-Rezeptoragonisten auf kardiovaskuläre Risikofaktoren: eine narrative Übersicht direkter Vergleiche. Diabetes Obes Metab 2018;20:508–519.
66. Mosterd CM, Bjornstad P, van Raalte DH. Nephroprotektive Wirkung von GLP-1-Rezeptoragonisten: Wo stehen wir? J Nephrol 2020;33:965–975.
67. Kamanna VS, Roh DD, Kirschenbaum MA. Hyperlipidämie und Nierenerkrankungen: Konzepte aus der Histopathologie und Zellbiologie des Glomerulus. Histopathol 1998;13:169–179.
68. Sun F, Wu S, Wang J, et al. Wirkung von Glucagon-ähnlichen Peptid--1-Rezeptoragonisten auf Lipidprofile bei Typ-2-Diabetes: eine systematische Überprüfung und Netzwerk-Metaanalyse. Clin Ther 2015;37:225–241.
69. Wøjdemann M, Wettergren A, Sternby B, et al. Hemmung der Sekretion menschlicher Magenlipase durch Glucagon-ähnliches Peptid-1. Dig Dis Sci 1998;43:799–805.
70. Xiao C, Bandsma RH, Dash S, Szeto L, Lewis GF. Exenatid, ein Glucagon-ähnlicher Peptid--1-Rezeptoragonist, hemmt bei gesunden Menschen akut die intestinale Lipoproteinproduktion. Arterioscler Thromb Vasc Biol 2012;32:1513–1519.
71. Ben-Shlomo S, Zvibel I, Schnell M, et al. Das Glucagon-ähnliche Peptid -1 reduziert die Leberlipogenese durch Aktivierung der AMP-aktivierten Proteinkinase. J Hepatol 2011;54:1214–1223.
72. Ding X, Saxena NK, Lin S, Gupta NA, Anania FA. Exendin-4, ein Glucagon-ähnliches Protein-1 (GLP-1)-Rezeptoragonist, kehrt Lebersteatose bei ob/ob-Mäusen um. Hepatologie 2006;43:173–181.
73. Kooijman S., Wang Y., Parlevliet ET. et al. Die Signalübertragung des zentralen GLP-1-Rezeptors beschleunigt die Plasmaclearance von Triacylglycerin und Glucose durch Aktivierung des braunen Fettgewebes bei Mäusen. Diabetologia 2015;58:2637–2646.
74. Beiroa D, Imbernon M, Gallego R, et al. Der GLP-1-Agonismus stimuliert die Thermogenese und Bräunung des braunen Fettgewebes durch hypothalamische AMPK. Diabetes 2014;63:3346–3358.
75. Pyke C, Heller RS, Kirk RK, et al. Lokalisierung des GLP-1-Rezeptors in Affen- und menschlichem Gewebe: Neue Verteilung mit umfassend validiertem monoklonalem Antikörper entdeckt. Endokrinologie 2014;155:1280–1290.
76. Schlatter P, Beglinger C, Drewe J, Gutmann H. Expression des Glucagon-ähnlichen Peptid-1-Rezeptors in primären proximalen tubulären Schweinezellen. Regul Pept 2007;141:120–128.
77. Fujita H., Sakamoto T., Komatsu K. et al. Reduzierung der zirkulierenden Superoxiddismutaseaktivität bei Typ-2-Diabetikern mit Mikroalbuminurie und deren Modulation durch Telmisartan-Therapie. Hypertens Res 2011;34:1302–1308.
78. Yin W, Jiang Y, Xu S, et al. Proteinkinase C und Proteinkinase A sind am Schutz des rekombinanten menschlichen Glucagon-ähnlichen Peptids-1 auf Glomeruli und Tubuli bei diabetischen Ratten beteiligt. J Diabetes Investig 2019;10:613–625.
79. Hendarto H., Inoguchi T., Maeda Y. et al. Das GLP-1-Analogon Liraglutid schützt vor oxidativem Stress und Albuminurie bei Streptozotocin-induzierten diabetischen Ratten durch Proteinkinase A-vermittelte Hemmung der renalen NAD(P)H-Oxidasen. Stoffwechsel 2012;61:1422–1434.
80. Wang C, Li C, Peng H, et al. Die Aktivierung des Nrf2-ARE-Signalwegs mildert durch Hyperglykämie verursachte Schäden in Maus-Podozyten. Cell Physiol Biochem 2014;34:891–902.
81. Zhou T, Zhang M, Zhao L, Li A, Qin X. Die Aktivierung von Nrf2 trägt zur Schutzwirkung von Exendin-4 gegen Angiotensin II-induzierte Seneszenz vaskulärer glatter Muskelzellen bei. Am J Physiol Cell Physiol 2016;311:C572–C582.
82. Ye Y, Zhong Obes Res Clin Pract 2019;13:385–390.
83. Kodera R, Shikata K, Kataoka HU, et al. Der Glucagon-ähnliche Peptid--1-Rezeptoragonist lindert Nierenschäden durch seine entzündungshemmende Wirkung, ohne den Blutzuckerspiegel in einem Rattenmodell für Typ-1-Diabetes zu senken. Diabetologia 2011;54:965–978.
84. Chaudhuri A, Ghanim H, Vora M, et al. Exenatid übt eine starke entzündungshemmende Wirkung aus. J Clin Endocrinol Metab 2012;97:198–207.
85. Bunck MC, Diamant M, Eliasson B, et al. Exenatid beeinflusst zirkulierende Biomarker für das kardiovaskuläre Risiko unabhängig von Veränderungen der Körperzusammensetzung. Diabetes Care 2010;33:1734–1737.
86. Zhang H, Zhang Kidney Blood Press Res 2012;35:483–488.
87. Hogan AE, Gaoatswe G, Lynch L, et al. Die Glucagon-like-Peptid-1-Analogon-Therapie moduliert direkt die angeborene immunvermittelte Entzündung bei Personen mit Typ-2-Diabetes mellitus. Diabetologia 2014;57:781–784.
88. Rizzo M, Abate N, Chandalia M, et al. Liraglutid reduziert oxidativen Stress und stellt den Hämoxygenase--1- und Ghrelinspiegel bei Patienten mit Typ-2-Diabetes wieder her: eine prospektive Pilotstudie. J Clin Endocrinol Metab 2015;100:603–606.
89. Yip KP, Tse CM, McDonough AA, Marsh DJ. Durch akute und chronische Hypertonie induzierte Umverteilung der Na plus /H plus-Austauscher-Isoform NHE3 in proximalen Tubuli. Am J Physiol 1998;275:F565–F575?
90. Ronn J, Jensen EP, Wewer Albrechtsen NJ, Holst JJ, Sorensen CM. Das Glucagon-ähnliche Peptid -1 beeinflusst den Nierenblutfluss und die Harnflussrate bei spontan hypertensiven Ratten trotz deutlich verringerter renaler Expression von GLP -1-Rezeptoren akut. Physiol Rep 2017;5:e13503.
91. Skov J, Dejgaard A, Frøkiær J, et al. Glucagon-ähnliches Peptid-1 (GLP-1): Wirkung auf die Hämodynamik der Nieren und das Renin-Angiotensin-Aldosteron-System bei gesunden Männern. J Clin Endocrinol Metab 2013;98:E664–E671.
92. Skov J, Pedersen M, Holst JJ, et al. Kurzfristige Auswirkungen von Liraglutid auf die Nierenfunktion und vasoaktive Hormone bei Typ-2-Diabetes: eine randomisierte klinische Studie. Diabetes Obes Metab 2016;18:581–589.
93. von Scholten BJ, Hansen TW, Goetze JP, Persson F, Rossing P. Glucagon-ähnlicher Peptid-1-Rezeptoragonist (GLP-1 RA): Langzeitwirkung auf die Nierenfunktion bei Patienten mit Typ-2-Diabetes. J Diabetes Complications 2015;29:670–674.
94. Pocai A, Carrington PE, Adams JR, et al. Der duale Agonismus des Glucagon-ähnlichen Peptids 1/Glucagon-Rezeptors kehrt Fettleibigkeit bei Mäusen um. Diabetes 2009;58:2258–2266.
95. Capozzi ME, Svendsen B, Encisco SE, et al. Der Zelltonus wird durch Proglucagon-Peptide durch cAMP-Signalisierung definiert. JCI Insight 2019;4:e126742.
96. Frias JP, Nauck MA, Van J, et al. Wirksamkeit und Sicherheit von LY3298176, einem neuartigen dualen GIP- und GLP-1-Rezeptoragonisten, bei Patienten mit Typ-2-Diabetes: eine randomisierte, placebokontrollierte und aktive komparatorkontrollierte Phase-2-Studie. Lancet 2018;392:2180–2193.
97. Madsen KB, Askov-Hansen C, Naimi RM, et al. Akute Auswirkungen kontinuierlicher Infusionen von GLP-1, GLP-2 und der Kombination (GLP-1 plus GLP-2) auf die intestinale Resorption beim Kurzdarmsyndrom (SBS)-Patienten: eine placebokontrollierte Studie. Regul Pept 2013;184:30–39.
98. Müller TD, Sullivan LM, Habegger K, et al. Wiederherstellung der Leptin-Reaktionsfähigkeit bei ernährungsbedingt fettleibigen Mäusen unter Verwendung eines optimierten Leptin-Analogons in Kombination mit Exendin-4 oder FGF21. J Pept Sci 2012;18:383–393.
99. Suarez-Pinzon WL, Power RF, Yan Y, Wasserfall C, Atkinson M, Rabinovitch A. Eine Kombinationstherapie mit Glucagon-ähnlichem Peptid -1 und Gastrin stellt die Normoglykämie bei diabetischen NOD-Mäusen wieder her. Diabetes 2008;57:3281–3288.
100. Trevaskis JL, Mack CM, Sun C, et al. Verbesserte Glukosekontrolle und reduziertes Körpergewicht bei Nagetieren mit einem doppelten Wirkmechanismus von Peptidhybriden. PLoS One 2013;8:e78154.
101. Neary NM, Small CJ, Druce MR, et al. Das Peptid YY3-36 und das Glucagon-ähnliche Peptid-17-36 hemmen zusätzlich die Nahrungsaufnahme. Endokrinologie 2005;146:5120–5127.
102. Gutzwiller JP, Degen L, Matzinger D, Prestin S, Beglinger C. Wechselwirkung zwischen GLP-1 und CCK-33 bei der Hemmung der Nahrungsaufnahme und des Appetits bei Männern. Am J Physiol Regul Integr Comp Physiol 2004;287:R562–R567.
103. Balena R, Hensley IE, Miller S, Barnett AH. Kombinationstherapie mit GLP-1-Rezeptoragonisten und Basalinsulin: eine systematische Überprüfung der Literatur. Diabetes Obes Metab 2013;15:485–502.
104. Bech EM, Voldum-Clausen K, Pedersen SL, et al. Adrenomedullin und Glucagon-ähnliches Peptid-1 haben additive Wirkungen auf die Nahrungsaufnahme bei Mäusen. Biomed Pharmacother 2019;109:167–173.
105. Pan Q, Lin S, Li Y, et al. Ein neuartiger dualer GLP-1- und FGF21-Agonist hat therapeutisches Potenzial für Diabetes und nichtalkoholische Steatohepatitis. EBioMedicine 2021;63:103202.
106. Finan B, Yang B, Ottaway N, et al. Eine gezielte Östrogenabgabe kehrt das metabolische Syndrom um. Nat Med 2012;18:1847–1856.
107. Quarta C, Clemmensen C, Zhu Z, et al. Die molekulare Integration der Inkretin- und Glukokortikoidwirkung kehrt immunmetabolische Dysfunktion und Fettleibigkeit um. Cell Metab 2017;26:620–632.
108. Chodorge M, Celeste AJ, Grimsby J, et al. Entwicklung einer GLP- 1-analogen Peptid/Anti-PCSK9-Antikörper-Fusion zur Behandlung von Typ-2-Diabetes. Sci Rep 2018;8:17545.
109. Clemmensen C, Finan B, Fischer K, et al. Der duale Melanocortin-4-Rezeptor- und GLP-1-Rezeptor-Agonismus verstärkt die metabolischen Vorteile bei ernährungsbedingt fettleibigen Mäusen. EMBO Mol Med 2015;7:288–298.
110. Jouihan H., Will S., Guionaud S. et al. Überlegene Reduzierung der Lebersteatose und -fibrose durch gleichzeitige Verabreichung eines Glucagon-ähnlichen Peptid--1-Rezeptoragonisten und Obeticholsäure bei Mäusen. Mol Metab 2017;6:1360–1370.
111. Frías JP, Guja C, Hardy E, et al. Exenatide einmal wöchentlich plus Dapagliflozin einmal täglich im Vergleich zu Exenatid oder Dapagliflozin allein bei Patienten mit Typ-2-Diabetes, die mit einer Metformin-Monotherapie unzureichend kontrolliert wurden (DAUER-8): eine 28-Woche, multizentrisch, doppelblind, Phase 3, randomisiert Kontrollierter Versuch. Lancet Diabetes Endocrinol 2016;4:1004–1016.
Ji Hee Yu, So Young Park, Da Young Lee, Nan Hee Kim, Ji A Seo
Abteilung für Endokrinologie und Stoffwechsel, Abteilung für Innere Medizin, Korea University Ansan Hospital, Korea University College of Medicine, Ansan, Republik Korea






