Die Hemmung der menschlichen Tyrosinase erfordert molekulare Motive, die sich deutlich von der Tyrosinase aus Pilzen unterscheiden
Apr 10, 2023
Cistanchehat auch die Funktion vonFörderung der Kollagenproduktion, was die Elastizität und den Glanz der Haut erhöhen und helfen kannreparieren beschädigte Hautzellen. CistanchePhenylethanolglycosidehaben eine signifikante herunterregulierende Wirkung auf die Tyrosinase-Aktivität, und die Wirkung auf die Tyrosinase ist nachweislich eine kompetitive und reversible Hemmung, was eine wissenschaftliche Grundlage für die Entwicklung und Verwendung der aufhellenden Inhaltsstoffe in Cistanche liefern kann. Daher spielt Cistanche eine Schlüsselrolle für die HautAufhellung. Es kannhemmen die Melaninproduktionum Verfärbungen und Mattheit zu reduzieren; und fördern die Kollagenproduktion, um die Elastizität und Ausstrahlung der Haut zu verbessern. Aufgrund der weit verbreiteten Anerkennung dieser Wirkung von Cistanche haben viele Hautaufhellungsprodukte damit begonnen, pflanzliche Inhaltsstoffe wie Cistanche zuzusetzen, um der Nachfrage der Verbraucher gerecht zu werden, wodurch der kommerzielle Wert von Cistanche in Hautaufhellungsprodukten erhöht wird. Zusammenfassend ist die Rolle von Cistanche bei der Hautaufhellung von entscheidender Bedeutung. Es istAntioxidansWirkung undKollagenbildende Wirkungkann Verfärbungen und Mattheit reduzieren, die Elastizität und den Glanz der Haut verbessern und so einen aufhellenden Effekt erzielen. Auch die weit verbreitete Anwendung von Cistanche in Hautaufhellungsprodukten zeigt, dass seine Rolle im kommerziellen Wert nicht zu unterschätzen ist.

Klicken Sie zum Aufhellen auf Bio-Cistanche
Für mehr Information:
david.deng@wecistanche.com WhatApp:86 13632399501
Tyrosinase ist das geschwindigkeitsbestimmende Enzym der Melaninproduktion und dementsprechend das wichtigste Ziel zur Hemmung der Hyperpigmentierung. Zahlreiche Tyrosinase-Inhibitoren wurden identifiziert, aber den meisten von ihnen mangelt es an klinischer Wirksamkeit, da sie mithilfe von Pilztyrosinase als Ziel identifiziert wurden. Deshalb verwendeten wir rekombinante menschliche Tyrosinase, um eine Bibliothek von 50 000 Verbindungen zu screenen und verglichen die aktiven Screening-Treffer mit bekannten aufhellenden Inhaltsstoffen. Hydrochinon und sein Derivat Arbutin hemmten die menschliche Tyrosinase nur schwach mit einer halbmaximalen Hemmkonzentration (IC50) im millimolaren Bereich, und Kojisäure zeigte eine schwache Wirksamkeit (IC50 > 500 mmol/L). Die wirksamsten Inhibitoren der menschlichen Tyrosinase, die in diesem Screening identifiziert wurden, waren Resorcinol-Thiazol-Derivate, insbesondere das neu identifizierte Thiamidol (Beiersdorf AG, Hamburg, Deutschland) (Isobutylamido-Thiazolylresorcinol), das einen IC50 von 1,1 mmol/L aufwies. Im Gegensatz dazu hemmte Thiamidol die Pilztyrosinase nur schwach (IC50 =108 mmol/L). In Melanozytenkulturen hemmte Thiamidol die Melaninproduktion stark, aber reversibel (IC50 =0,9 mmol/L), wohingegen Hydrochinon die Melaninbildung irreversibel hemmte (IC 50 = 16,3 mmol/L). Klinisch reduzierte Thiamidol sichtbar das Auftreten von Altersflecken innerhalb von 4 Wochen, und nach 12 Wochen waren einige Altersflecken nicht mehr von der normalen angrenzenden Haut zu unterscheiden. Das volle Potenzial von Thiamidol zur Reduzierung der Hyperpigmentierung der menschlichen Haut muss in zukünftigen Studien erforscht werden.
EINFÜHRUNG
Melasma, aktinische und senile Lentigines sowie postinflammatorische Hyperpigmentierung sind große kosmetische Probleme, wegen deren viele Patienten ärztlichen Rat einholen. Im Allgemeinen betreffen diese Störungen Bevölkerungsgruppen mit dunklerer Haut häufiger und schwerer (Stratigos und Katsambas, 2004). Für die Behandlung hyperpigmentierter Erkrankungen stehen viele topische Produkte zur Verfügung, die verschiedene Wirkstoffe enthalten, um die Melaninproduktion und/oder -verteilung zu reduzieren. Obwohl die Hyperpigmentierung der Haut durch verschiedene Mechanismen reduziert werden kann (Briganti et al., 2003), ist Tyrosinase, das geschwindigkeitsbestimmende Enzym der Melaninproduktion, das offensichtliche Ziel für Inhibitoren der Hyperpigmentierung (Kanteev et al., 2015; Lee et al., 2014; Ramsden und Riley, 2014). Viele Substanzen wurden in der Literatur als Tyrosinase-Inhibitoren beschrieben, den meisten von ihnen fehlt jedoch die klinische Wirksamkeit, und nur wenige Verbindungen werden derzeit in topischen dermatologischen Produkten verwendet (Chang, 2009; Kim und Uyama, 2005; Rescigno et al., 2002). ). Unter diesen sind Kojisäure, Hydrochinon und Arbutin am häufigsten (Solano et al., 2006).
Die unbefriedigende klinische Wirksamkeit derzeit verwendeter Tyrosinase-Inhibitoren ist groß, da diese Verbindungen nur mit Tyrosinase getestet wurden, die aus dem Pilz Agaricus bisporus (mTyr) isoliert wurde (Espin et al., 2000; Garcia-Molina et al., 2005), was die einzige ist Aktive Tyrosinase ist leicht im Handel erhältlich. Die katalytischen Aktivitäten und Substratspezifitäten von mTyr unterscheiden sich deutlich vom Säugetierenzym (Hearing et al., 1980). Die dreidimensionalen Strukturen mehrerer Tyrosinasen wurden kürzlich aufgeklärt, darunter die Strukturen von mTyr (Ismaya et al., 2011) und von zwei bakteriellen Enzymen aus Streptomyces castaneoglobisporus (Matoba et al., 2006) und Bacillus megaterium (Sendovski et al. , 2011). Im Gegensatz dazu sind für menschliche Tyrosinase (hTyr) nur sehr wenige kinetische oder strukturelle Informationen verfügbar, hauptsächlich aufgrund der erheblichen Schwierigkeiten, ausreichende Mengen an hTyr aus natürlichen Quellen oder durch heterologe Expression zu erhalten. hTyr wurde vorübergehend in verschiedenen tierischen Zelllinien exprimiert (Olivares et al., 2002; Schweikardt et al., 2007; Tripathi et al., 1992; Wendt, 2006), aber die Ausbeuten waren immer zu niedrig für eine detaillierte Charakterisierung der resultierenden Zelllinien hTyr-Präparate. In jüngerer Zeit haben mehrere Gruppen effizientere Expressionssysteme für hTyr entwickelt (Cordes et al., 2013; Fogal et al., 2015; Lai et al., 2016), aber Daten zur dreidimensionalen Struktur von hTyr oder kinetische Daten von hTyr-Inhibitoren fehlten noch.

ERGEBNISSE
Hemmung von hTyr
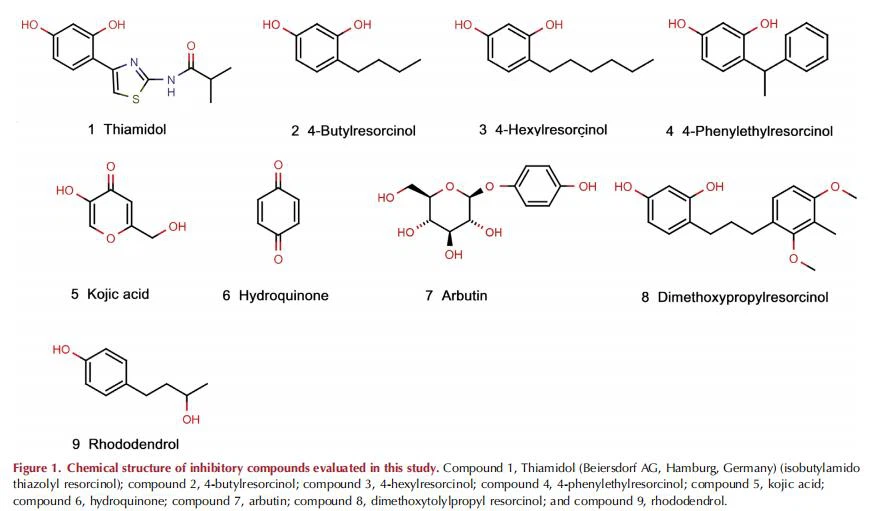
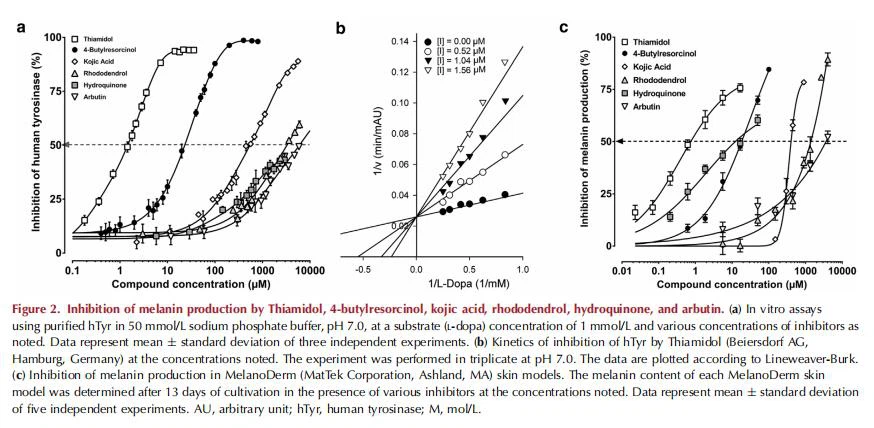
A screen of 50,000 compounds in the library, which spans a wide chemical space, yielded several hit series of active and effective hTyr inhibitors. Among them, derivatives of thiazolyl-resorcinol were the most promising group. This lead compound was then optimized to develop derivatives with high activity and physicochemical properties compatible with topical formulations. Thiamidol (isobutyl amido thiazolyl resorcinol, compound 1) (Figure 1) was identified as one of the most potent derivatives. In addition to Thiamidol, 4-butyl resorcinol (compound 2) and the classical tyrosinase inhibitors kojic acid (compound 5), hydroquinone (compound 6), and arbutin (compound 7), as well as rhododendron (compound 9), were also tested as inhibitors of the diphenols (L-dopa oxidase) activity of hTyr over a wide range of concentrations (up to 4 orders of magnitude). The results are summarized in Figure 2a and Table 1. Among these actives, Thiamidol was by far the most efficient inhibitor of hTyr, with a half-maximal inhibitory concentration (IC50) of 1.1 mmol/L, with almost complete enzyme inhibition of hTyr occurring at concentrations above 10 mmol/L. The resorcinol derivatives 4-butylresorcinol, 4-hexylresorcinol, and 4-phenylethylresorcinol had IC50 values of 21mmol/L, 94mmol/L, and 131 mmol/L, respectively (Table 1). With an IC50 of about 500 mmol/L, kojic acid was 500 times less potent than Thiamidol. Hydroquinone and arbutin were both very poor inhibitors of hTyr, with IC50 values in the millimolar range. Kojic acid, arbutin, and hydroquinone were not able to completely inhibit hTyr in the concentration range tested. Racemic rhododendron was also rather ineffective as an inhibitor of L-dopa oxidation, with an IC50 >1.200 mmol/L (Abbildung 2a).
Eine detaillierte kinetische Analyse der Hemmung von hTyr durch Thiamidol ergab einen streng kompetitiven Hemmtyp mit einer Inhibitorkonstante (Ki) von 0,25 mmol/L (Abbildung 2b, Tabelle 1). Dieser Wert stimmt mit dem aus Dosis-Wirkungs-Kurven geschätzten IC50-Wert (1,1 mmol/L) (vgl. Abbildung 2a) überein, der für eine kompetitive Hemmung etwa dreimal höher sein sollte als der Ki. Die Ki-Werte für 4-Butylresorcinol (9 mmol/L), 4-Hexylresorcinol (39 mmol/L) und 4-Phenylethylresorcinol (24 mmol/L) waren ebenfalls deutlich höher als die Ki-Wert von Thiamidol (Tabelle 1). Diese Daten veranschaulichen, dass die Thiazolylamid-Einheit von Thiamidol eine viel bessere Hemmung von hTyr bewirkt als die Kohlenwasserstoffseitenketten in drei anderen Derivaten von Resorcin (4-Butyl-, 4-Hexyl- und {{ 21}}Phenylethylresorcinol). Wie bereits erwähnt, ist die Wirksamkeit bei mTyr deutlich anders, wo 4-Butylresorcinol, 4-Hexylresorcinol und 4-Phenylethylresorcinol und sogar Kojisäure Thiamidol bei der Hemmung des Enzyms überlegen sind (Tabelle 1). Somit wäre Thiamidol bei einem Screening mit mTyr nicht als positiv identifiziert worden und die Wirksamkeit von 4-Phenylethylresorcinol wäre stark überschätzt worden.
Garcia-Jimenez et al. (2016) berichteten kürzlich, dass mTyr bestimmte Resorcine langsam oxidiert, vorausgesetzt, dass die vorherrschende Met-Form des Enzyms zuvor durch Zusätze wie H2O2 und Ascorbat in die Oxy- oder Desoxy-Form umgewandelt wird und die Reaktion durch o-Diphenole aufrechterhalten wird . Daher verwendeten wir eine quantitative Hochleistungsflüssigkeitschromatographie-Analyse (Ito und Wakamatsu, 2015), um festzustellen, ob Thiamidol möglicherweise auch ein Substrat von hTyr ist. Unter unseren normalen Testbedingungen (d. h. in Abwesenheit der von Garcia-Jimenez et al., 2016) genannten Zusatzstoffe fand innerhalb mehrerer Stunden nach der Inkubation mit hTyr keine nachweisbare Oxidation von Thiamidol statt, wohingegen Rhododendron innerhalb dieses Zeitraums leicht oxidiert wurde (siehe ergänzende Abbildung S1 online). Daher gehen wir davon aus, dass die von Garcia-Jimenez et al. ist für Thiamidol und hTyr unter physiologischen Bedingungen nicht relevant.
Hemmung der Melaninproduktion
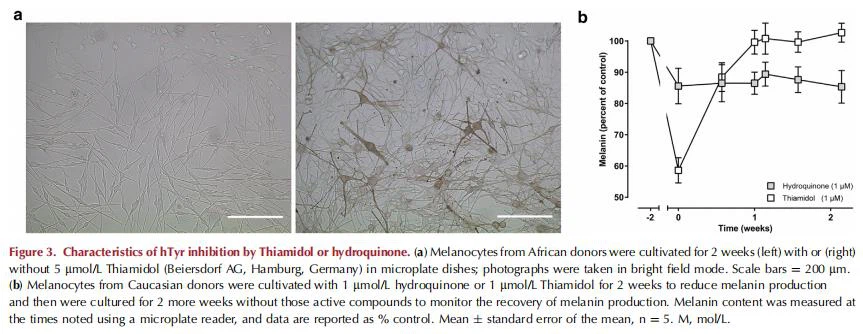
Anschließend haben wir die potenzielle Hemmwirkung dieser Verbindungen anhand eines dreidimensionalen Modells für die menschliche Haut getestet. Wie bei gereinigtem hTyr beobachtet, zeigte Arbutin nur eine vernachlässigbare Wirksamkeit bei der Hemmung der Melaninproduktion in Hautmodellen von MelanoDerm (MatTek Corporation, Ashland, MA) (IC50 > 4,000 mmol/L) (Abbildung 2c) . Kojisäure hemmte die Melaninproduktion mit einem IC50-Wert von 400 mmol/L und zeigte eine überraschend steile Dosis-Wirkungs-Kurve, wobei Konzentrationen unter 200 mmol/L die Melaninproduktion nur geringfügig hemmten (d. h. um 5 Prozent bei 150 mmol/L). Rhododendron zeigte nur geringfügige Auswirkungen auf die Melanogenese, mit einem offensichtlichen IC50-Wert für die Hemmung von w1.200 mmol/L. Hydrochinon hemmte die Melaninproduktion in MelanoDerm-Hautmodellen mit einem IC50 von 15 mmol/L, was darauf hindeutet, dass es einen anderen Mechanismus als die Tyrosinase-Hemmung hat. 4-Butylresorcinol hemmte die Melaninsynthese mit einem IC50 von 13,5 mmol/L. Auch hier war Thiamidol mit einem IC50 von 0,9 mmol/L bei weitem der stärkste Inhibitor der Melaninproduktion in MelanoDerm-Hautmodellen, und in Monoschichtkulturen reduzierte Thiamidol die Melaninbildung sichtbar (Abbildung 3a).

Anschließend wurden Hydrochinon und Thiamidol in Langzeit-Melanozyten-Monoschichtkulturen getestet, um die mögliche Reversibilität der Hemmung zu überprüfen. Obwohl 1 mmol/L Thiamidol die Melaninproduktion nach 2 Wochen auf weniger als 60 Prozent reduzierte, reduzierte 1 mmol/L Hydrochinon die Melaninproduktion nur auf etwa 85 Prozent (Abbildung 3b). Bei der weiteren Kultivierung ohne die Wirkstoffe begannen Melanozyten, die durch Thiamidol gehemmt worden waren, jedoch schnell wieder mit der Melaninproduktion und erreichten innerhalb einer Woche das Niveau vor der Behandlung. Im Gegensatz dazu erlangten mit Hydrochinon behandelte Zellen ihre volle Kapazität zur Melaninproduktion innerhalb der 2-wöchigen Kulturperiode nicht wieder, und die Melaninproduktion blieb bei 85 Prozent des Niveaus vor der Behandlung.
Molekulare Modellierung
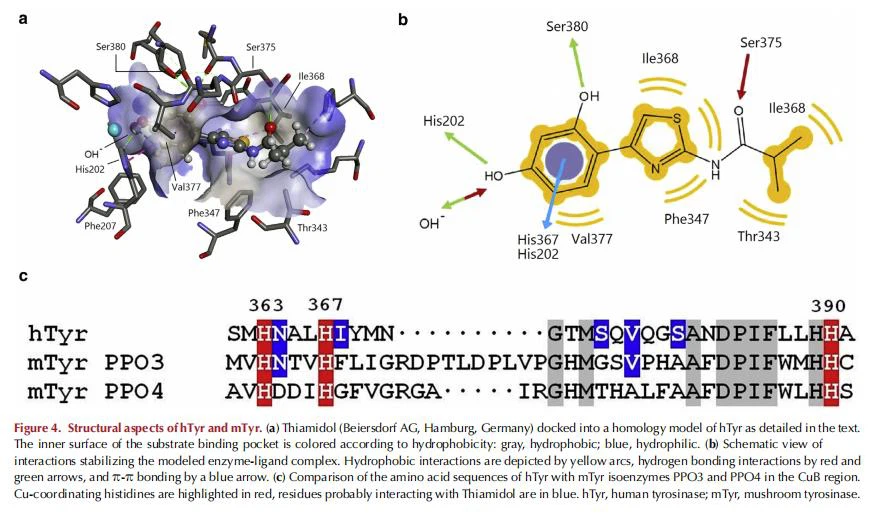
Mögliche Bindungsmodi von Thiamidol an hTyr wurden durch virtuelle Docking-Studien untersucht. Abbildung 4a zeigt das aktive Zentrum des Homologiemodells von hTyr in der Met-Form mit einem angedockten Thiamidol-Liganden in einer Konformation mit der niedrigsten Energie. Links ist das Di-Kupfer-Zentrum mit dem verbrückenden Sauerstoff zu sehen. Es werden nur Aminosäurereste angezeigt, die unmittelbar an den gebundenen Inhibitor angrenzen. (Die Restnummerierung umfasst das Signalpeptid). Die Innenfläche der Bindungstasche ist je nach Hydrophobie auf einer Skala von blau für hydrophil bis braun für hydrophob gefärbt. Obwohl die Umgebung des Dikupferzentrums deutlich hydrophil ist, wird eine stark hydrophobe Untertasche hauptsächlich durch die Seitenketten von I368, V377 und F347 gebildet. In der gezeigten räumlichen Ausrichtung stellt die 1-Hydroxygruppe des aromatischen Rings des Liganden umfangreiche Kontakte mit dem Dikupferzentrum her, und die 3-Hydroxygruppe ist an Wasserstoffbrückenbindungen mit der Seitenkette beteiligt S380 und das Rückgrat-Carbonyl von M374. Der Thiazolylring wird durch hydrophobe Wechselwirkungen mit der unpolaren Tasche (Abbildung 4b) an Ort und Stelle gehalten, die aus Seitenketten von Aminosäuren besteht, von denen sich die meisten zwischen mTyr und hTyr unterscheiden (Abbildung 4c).
Vergleichbare Ergebnisse wurden erhalten, als Thiamidol an die kürzlich veröffentlichte Röntgenstruktur des strukturell ähnlichen TRP1 angedockt wurde, einem Zn2þ-haltigen melanogenen Enzym mit noch unbekannter Funktion beim Menschen (Ghanem und Fabrice, 2011; Lai et al., 2017), was darauf hindeutet dass das TYRP1-Enzym auch durch Thiamidol gehemmt wird (siehe ergänzende Abbildung S2 online).
Klinische Studien
Die In-vivo-Wirksamkeit von Thiamidol wurde dann in klinischen Studien untersucht, in denen ältere Probanden Altersflecken auf ihrer Haut zweimal täglich mit einer Formel behandelten, die {{0}},2 Prozent Thiamidol enthielt, oder nur mit dem Vehikel als Kontrolle. Bereits nach 4 Wochen Behandlung waren die behandelten Altersflecken deutlich heller als die unbehandelten Kontrollaltersflecken (Abbildung 5a). Die Verbesserung hielt über den gesamten Behandlungszeitraum an und nach 12 Wochen waren einige der Altersflecken nicht mehr von der umgebenden normal pigmentierten Haut zu unterscheiden (Abbildung 5b). EpiFlash-Fotos (Canfifield Scientifific Inc., Parsippany, NJ) zeigten eine sichtbare Verbesserung des Erscheinungsbilds von Altersflecken, und die unbehandelten Kontrollaltersflecken blieben unverändert (nicht gezeigt). Eine Folgestudie zeigte, dass Konzentrationen von Thiamidol bereits ab 0,1 Prozent die Sichtbarkeit von Altersflecken wirksam reduzierten (siehe ergänzende Abbildung S3 online).
DISKUSSION
Der sicherste und wirksamste Weg zur Behandlung einer kutanen Hyperpigmentierung besteht darin, die Melaninproduktion durch Hemmung der Tyrosinase-Aktivität zu reduzieren. Den meisten in der Literatur beschriebenen Tyrosinase-Inhibitoren mangelt es jedoch an klinischer Wirksamkeit, wenn sie in topische Produkte eingearbeitet werden. Fast alle von ihnen wurden nur gegen mTyr getestet (Espin et al., 2000; Garcia-Molina et al., 2005) und erwiesen sich daher, obwohl sie gegen mTyr wirksam waren, als schlechte Inhibitoren von hTyr. Im Handel erhältliches mTyr ist kein homogenes Präparat, sondern eine Mischung aus mehreren Tyrosinase-Isoenzymen und geringen Mengen zusätzlicher Enzymaktivitäten, die Inhibitionsstudien auf unvorhersehbare Weise beeinflussen können (Pretzler et al., 2017). Die Isoenzyme AbPPO3 und AbPPO4, die Hauptbestandteile von kommerziell erhältlichem mTyr, weisen im Bereich des aktiven Zentrums Aminosäuresequenzen auf, die sich deutlich von denen von hTyr unterscheiden (Abbildung 4c). Beide mTyr-Isoenzyme enthalten zusätzliche Schleifen zwischen Asn371 (einer der Glykosylierungsstellen von hTyr) und Gly372. Mehrere der Reste, die in hTyr mit Thiamidol interagieren (vgl. Abbildung 4b), sind in mTyr nicht konserviert, zum Beispiel Ile368, Ser375 und Ser380. Phe207 ist in mTyr strukturell konserviert, Phe347 hingegen nicht. Da selbst kleine Änderungen der Enzym-Ligand-Wechselwirkungen dramatische Auswirkungen auf die Bindungsaffinitäten haben können, waren die unterschiedlichen Hemmprofile von hTyr und mTyr (zusammengefasst in Tabelle 1) keine Überraschung.
Das Hauptziel dieser Studie bestand darin, die Wirkungen von Arbutin, Hydrochinon und Kojisäure mit verschiedenen Resorcin-Derivaten auf die katalytische Funktion von hTyr und auf die Melaninproduktion in vivo zu vergleichen. Bis auf Thiamidol wurden alle getesteten Substanzen als Tyrosinase-Inhibitoren beschrieben (Kim et al., 2012); Ihre berichteten Hemmaktivitäten sind jedoch äußerst unterschiedlich. In der medizinischen Literatur gilt Hydrochinon als Standardkriterium für die Behandlung von Hauthyperpigmentierung, obwohl erhebliche Bedenken hinsichtlich seiner Sicherheit bestehen. Die Verwendung von Hydrochinon in Kosmetika ist in der Europäischen Union verboten, in den USA wird es jedoch immer noch als rezeptfreies Medikament in Formulierungen mit bis zu 2 Prozent Hydrochinon verkauft. Kürzlich äußerte die US-amerikanische Food and Drug Administration (2006) Bedenken hinsichtlich Hydrochinon; Eine endgültige Entscheidung steht jedoch noch aus. Die veröffentlichten IC50-Werte für die Hydrochinon-Hemmung von mTyr decken einen Bereich von 1,1 mmol/L (Kang et al., 2003) bis 680 mmol/L (Abu Ubeid et al., 2009) ab. In unserer Analyse war Hydrochinon bemerkenswert unwirksam gegen hTyr und hemmte es nur geringfügig und erreichte gerade einmal eine 50-prozentige Hemmung bei etwa 4,000 mmol/L. Obwohl Hydrochinon seit den frühen 1990er Jahren als Tyrosinase-Inhibitor gilt (Palumbo et al., 1991), legen unsere Ergebnisse nahe, dass seine zytotoxischen Eigenschaften wichtiger sind, nicht nur wegen seiner schädlichen Wirkung auf Melanozyten, sondern auch wegen seiner Wirksamkeit als Inhibitor der Melanogenese (Jimbow et al., 1974; Penney et al., 1984; Smith et al., 1988). Diese Ansicht wird nicht nur durch unsere Ergebnisse mit hTyr und die Tatsache, dass Hydrochinon die Melaninproduktion in Hautmodellen deutlich reduzierte, sondern auch durch unsere Experimente mit Melanozytenkulturen untermauert. Hier reduzierte Hydrochinon die Melaninproduktion, aber die behandelten Zellen erlangten nach der Entfernung des Wirkstoffs nicht wieder die volle Kapazität zur Melaninproduktion.

Although arbutin is generally considered an effective tyrosinase inhibitor, the published IC50 values of arbutin for mTyr range from 40 mmol/L (Ying et al., 1999) to more than 30,000 mmol/L (Sugimoto et al., 2005). In our test system, we found very high IC50 values (>4,000 mmol/L) für Arbutin sowohl mit gereinigtem hTyr als auch mit dem MelanoDerm-Hautmodell. Daten zur Wirksamkeit von a-Arbutin und b-Arbutin wurden veröffentlicht (Garcia-Jimenez et al., 2017). Allerdings handelt es sich bei beiden Verbindungen um Hydrochinon-Prodrugs, deren biologische Aktivität von der Freisetzung von Hydrochinon aus dem Molekül abhängt (Briganti et al., 2003). Der Wissenschaftliche Ausschuss für Verbraucherprodukte der Europäischen Union (2008) veröffentlichte eine kritische Stellungnahme zu Arbutin. Aufgrund der Freisetzung von Hydrochinon aus dem Molekül hält sie die Verwendung von Arbutin in kosmetischen Produkten für unsicher.
Die veröffentlichten IC50-Werte für die Tyrosinase-Hemmung durch Kojisäure reichen von 6 mmol/L (Curto et al., 1999) bis über 100 mmol/L (Jeon et al., 2005). Als Inhibitor von hTyr ist Kojisäure mit einem IC50 von etwa 500 mmol/L deutlich weniger wirksam. Kojisäure zeigt eine gemischte Art der Hemmung mit einem Ki von 145 mmol/L, was darauf hindeutet, dass sie an die Desoxyform der Tyrosinase bindet (Sun et al., 2014). Bei Verwendung zur Behandlung des MelanoDerm-Modells zeigt Kojisäure eine außergewöhnlich steile Dosis-Wirkungs-Kurve, wobei die relative Hemmung von 5 Prozent bei 150 mmol/L auf über 75 Prozent Hemmung bei 900 mmol/L ansteigt (siehe Abbildung 2c). Diese Tatsache könnte der Hauptgrund für die sehr begrenzte Wirksamkeit von Kojisäure in vivo sein. Was die Sicherheit von Kojisäure betrifft, so erachtet der Europäische Wissenschaftliche Ausschuss für Verbrauchersicherheit (2012) Kojisäure in Konzentrationen von bis zu 1,0 Prozent als sicher für kosmetische Produkte, wenn sie auf gesunde Haut aufgetragen werden, eine Ansicht, die auch vom Expertengremium für die Überprüfung kosmetischer Inhaltsstoffe ( Cosmetic Ingredient Review Expert Panel) geteilt wird ( Burnett et al., 2010).
Rhododendron erhielt 2008 in Japan den Status einer Quasidroge und wurde als aufhellender Inhaltsstoff in Kosmetikprodukten verwendet. Es wurde angenommen, dass es sich um einen kompetitiven Inhibitor der Tyrosinase handelt. Im Jahr 2013 wurden jedoch rhododendronhaltige Produkte in zehn asiatischen Ländern zurückgerufen, als fast 20000 Verbraucher nach der Verwendung der Produkte an Leukodermie erkrankten. Es wurde gezeigt, dass Rhododendron nicht nur ein Inhibitor, sondern auch ein Substrat sowohl von hTyr (Ito et al., 2014a) als auch von mTyr (Ito et al., 2014b) ist. Die Tyrosinase-abhängige Akkumulation von Stress im endoplasmatischen Retikulum und/oder die Aktivierung des apoptotischen Signalwegs können zur Melanozyten-Zytotoxizität von Rhododendron beitragen (Sasaki et al., 2014).
Das 4-substituierte Resorcin-Motiv ist seit einiger Zeit als wirksame chemische Einheit bekannt, die Tyrosinase hemmt (Khatib et al., 2005). Viele natürliche Verbindungen, die als Aufheller identifiziert wurden, vor allem Flavonoide, enthalten dieses Motiv (Shimizu et al., 2000, 2011). Da die Bioverfügbarkeit von Flavonoiden im Allgemeinen gering ist, bestand unser Ziel darin, Resorcin-Derivate mit besserer Wirksamkeit und Bioverfügbarkeit zu identifizieren. 4-Butylresorcinol wurde bereits als Inhibitor der Tyrosinase von Maus und Mensch (Kim et al., 2005; Kolbe et al., 2013) und der Dihydroxyindolcarbonsäureoxidase-Aktivität von Maus-TYRP1 (Katagiri et al.) identifiziert. , 2001) und ist kommerziell für die medizinische und kosmetische Behandlung von Hyperpigmentierung erhältlich (Bohnsack et al., 2012; Jimenez und Garcia-Carmona, 1997; Kim et al., 2005). Dennoch fehlten noch detaillierte kinetische Daten von 4-Butylresorcin. Im hTyr-Assay fanden wir eine streng kompetitive Art der Hemmung durch 4-Butylresorcin mit einem Ki von 9,1 mmol/L, was in hervorragender Übereinstimmung mit dem ermittelten IC50-Wert steht (Tabelle 1).

In unseren In-vitro-Experimenten war Thiamidol mit einem IC50 von 1,1 mmol/L im hTyr-Enzymtest und 0,9 mmol/L im MelanoDerm-Hautmodell mit Abstand die wirksamste aller getesteten Substanzen. Weitere Experimente bestätigten, dass Thiamidol ein streng kompetitiver Inhibitor ist (Abbildung 2b) und kein Substrat für Tyrosinase (siehe ergänzende Abbildung S1) und Thiamidol daher nicht in ein toxisches und möglicherweise Leukodermie auslösendes Chinon umgewandelt wird. Daher wurde Thiamidol für klinische Studien ausgewählt, um seine Wirksamkeit in vivo zu bewerten. Eine Studie mit Thiamidol unter Verwendung eines Spot-Applikators zeigte eine kontinuierliche Verbesserung des Erscheinungsbilds von Altersflecken über den gesamten 12-wöchigen Behandlungszeitraum und erreichte bereits nach 4 Wochen statistische Signifikanz. Diese Ergebnisse zeigen eine starke pigmentreduzierende Wirksamkeit des Thiamidol-Testprodukts und einen klaren klinischen Nutzen bei der Behandlung von Hauthyperpigmentierung.
MATERIALEN UND METHODEN
Menschliche Tyrosinase
Eine verkürzte, His-markierte Form von hTyr (hTyr-DHis), die die katalytische Domäne von hTyr umfasst, wurde in HEK 293-Zellen exprimiert und durch Metallaffinitätschromatographie auf Ni2þ-Sepharose (GE Healthcare, München, Deutschland) wie an anderer Stelle beschrieben gereinigt ( Cordes et al., 2013). Das resultierende Präparat hatte die gleichen katalytischen Eigenschaften wie Wildtyp-hTyr.

Quellen von Inhibitoren
Aus der Evotec-Verbindungsbibliothek (Evotec, Hamburg, Deutschland) wurden 50 000-Verbindungen ausgewählt, die einen weiten chemischen Bereich abdecken, um eine HTS für hTyr-Inhibitoren durchzuführen, die mit dem im nächsten Abschnitt beschriebenen Tyr-Assay bewertet wurde. Anschließend wurden Derivate vielversprechender Leitverbindungen zur weiteren Optimierung synthetisiert. Die anderen Inhibitoren wurden von verschiedenen Lieferanten gekauft (Einzelheiten siehe Online-Ergänzungsmaterialien).
Tyrosin-Assay und HTS-Verfahren
Ausführliche Informationen zur L-Dopa-Oxidase-Aktivität und den verwendeten HTS-Screeningverfahren finden Sie in den ergänzenden Materialien.
Molekulare Modellierung
Das In-silico-Docking basierte auf einem neuen Homologiemodell von hTyr, das an anderer Stelle beschrieben wurde (Mann et al., 2017). Die Simulationen wurden mit Molegro Virtual Docker (Molegro, Aarhus, Dänemark) durchgeführt. Für die visuelle Datenanalyse und Präsentation wurde Discovery Studio Visualizer 4.0 (Accelrys, San Diego, CA) verwendet. Die Sequenzen wurden der UniProt-Datenbank entnommen (UniProt Consortium, 2017).
Hautmodelltests
Ausführliche Informationen zu den als Hautmodell verwendeten MelanoDerm-Geweben und der Menge ihres Melaningehalts finden Sie in den ergänzenden Materialien.
Melanozytenkulturen
Ausführliche Informationen zu Melanozytenkulturen und der Quantifizierung ihres Melaningehalts finden Sie in den ergänzenden Materialien.
Klinische Studien
Es wurden zwei randomisierte In-vivo-Studien (blind für die Testprodukte, offen für die unbehandelte Kontrolle) durchgeführt. An einer Studie nahmen 18 weibliche Probanden (56–71 Jahre alt) teil, wobei 17 Probanden die Studie abschlossen. Die zweite Studie wurde mit 19 Probanden (18 Frauen, 1 Mann; 58e7{{10}} Jahre alt) durchgeführt, wobei alle 19 Probanden die Studie abschlossen. Jeder Proband trug zwei verschiedene Formulierungen zweimal täglich mit einem Spot-Applikator auf Altersflecken an seinen Unterarmen auf. Die Formulierungen unterschieden sich nur im Wirkstoff: 0,2 Prozent Thiamidol gegenüber Vehikel in der ersten Studie und 0,1 Prozent Thiamidol gegenüber Vehikel in der zweiten Studie. Ein Altersfleck pro Proband wurde mit einer Formel behandelt, die den Wirkstoff enthielt, und ein Kontrollfleck wurde nur mit dem Vehikel behandelt. Die Pigmentierung der Altersflecken wurde wie in den ergänzenden Materialien beschrieben analysiert. Die In-vivo-Studien wurden gemäß den Empfehlungen der aktuellen Fassung der Deklaration von Helsinki und den Richtlinien der International Conference on Harmonisation of Good Clinical Practice durchgeführt. Alle Teilnehmer dieser Studien gaben eine schriftliche Einverständniserklärung ab. Darüber hinaus wurden die Studien vom Institutional Review Board der Beiersdorf AG (Hamburg, Deutschland) genehmigt und freigegeben.
INTERESSENKONFLIKT
ERGÄNZUNGSMATERIAL
Ergänzendes Material ist mit der Online-Version des Papiers verlinkt.
VERWEISE
1. Abu Ubeid A, Zhao L, Wang Y, Hantash BM. Kurzsequenz-Oligopeptide mit inhibitorischer Wirkung gegen Tyrosinase aus Pilzen und Menschen. J Invest Dermatol 2009;129:2242e9.
2. Bohnsack K, Koop U, Hiddemann S, Kolbe L, Rippke F. Pigmentierungsreduzierende Wirksamkeit und Verträglichkeit von sechs neuen Gesichtspflegeformulierungen mit 4-n-Butylresorcinol, Poster-Nr. P864. Poster präsentiert auf dem 21. EADV-Kongress, 27-30 September 2012; Prag, Tschechische Republik.
3. Briganti S, Camera E, Picardo M. Chemische und instrumentelle Ansätze zur Behandlung von Hyperpigmentierung. Pigment Cell Res 2003;16:101e10.
4. Burnett CL, Bergfeld WF, Belsito DV, Hill RA, Klaassen CD, Liebler DC, et al. Abschlussbericht der Sicherheitsbewertung von Kojisäure zur Verwendung in Kosmetika. Int J Toxicol 2010;29(6 Suppl.). 244Se73.
5. Chang TS. Eine aktualisierte Übersicht über Tyrosinase-Inhibitoren. Int J Mol Sci 2009;10: 2440e75.
6. Chen QX, Ke LN, Song KK, Huang H, Liu XD. Hemmende Wirkung von Hexylresorcin und Dodecylresorcin auf die Tyrosinase von Pilzen (Agaricus bisporus). Protein J 2004;23:135e41.
7. Cordes P, Sun W, Wolber R, Kolbe L, Klebe G, Röhm KH. Expression in nicht melanogenen Systemen und Reinigung löslicher Varianten menschlicher Tyrosinase. Biol Chem 2013;394:685e93.
8. Curto EV, Kwong C, Hermersdo¨rfer H, Glatt H, Santis C, Virador V, et al. Inhibitoren der Melanozyten-Tyrosinase von Säugetieren: In-vitro-Vergleiche von Alkylestern der Gentisinsäure mit anderen mutmaßlichen Inhibitoren. Biochem Pharmacol 1999;57:663e72.
9. Espin JC, Varon R, Fenoll LG, Gilabert MA, Garcia-Ruiz PA, Tudela J, et al. Kinetische Charakterisierung der Substratspezifität und des Mechanismus der Pilztyrosinase. Eur J Biochem 2000;267:1270e9.
10. Fogal S, Carotti M, Giaretta L, Lanciai F, Nogara L, Bubacco L, Bergantino E. In Insektenzellen produzierte menschliche Tyrosinase: ein Meilenstein für das Screening neuer Medikamente, die sich mit ihrer Aktivität befassen. Mol Biotechnol 2015;57:45e57.
11. Garcia-Jimenez A, Teruel-Puche JA, Berna J, Rodriguez-Lopez JN, Tudela J, Garcia-Canovas F. Wirkung von Tyrosinase auf Alpha- und Beta-Arbutin: Eine kinetische Studie. PLoS One 2017;12:e0177330.
12. Garcia-Jimenez A, Teruel-Puche JA, Berna J, Rodriguez-Lopez JN, Tudela J, Garcia-Ruiz PA, Garcia-Canovas F. Charakterisierung der Wirkung von Tyrosinase auf Resorcinole. Bioorg Med Chem 2016;24:4434e43.
13. Garcia-Molina F, Hiner AN, Fenoll LG, Rodriguez-Lopez JN, Garcia-Ruiz PA, Garcia-Canovas F, et al. Pilztyrosinase: Katalaseaktivität, Hemmung und Suizidinaktivierung. J Agric Food Chem 2005;53:3702e9.
14. Ghanem G, Fabrice J. Tyrosinase-verwandtes Protein 1 (Tyrp1/gp75) im menschlichen Hautmelanom. Mol Oncol 2011;5:150e5.
15. Anhörung von VJ Jr, Ekel TM, Montague PM, Nicholson JM. Säugetier-Tyrosinase. Stöchiometrie und Messung von Reaktionsprodukten. Biochim Biophys Acta 1980;611:251e68.
16. Ismaya WT, Rozeboom HJ, Weijn A, Mes JJ, Fusetti F, Wichers HJ, Dijkstra BW. Kristallstruktur der Pilztyrosinase aus Agaricus bisporus: Identität der Tetramer-Untereinheiten und Wechselwirkung mit Tropolon. Biochemie 2011;50:5477e86.
17. Ito S, Gerwat W, Kolbe L, Yamashita T, Ojika M, Wakamatsu K. Menschliche Tyrosinase kann beide Enantiomere von Rhododendron oxidieren. Pigment Cell Melanoma Res 2014a;27:1149e53.
18. Ito S, Ojika M, Yamashita T, Wakamatsu K. Tyrosinase-katalysierte Oxidation von Rhododendron erzeugt 2-Methylchroman-6,7-Dion, den mutmaßlich ultimativen toxischen Metaboliten: Auswirkungen auf die Melanozytentoxizität . Pigment Cell Melanoma Res 2014b;27:744e53.
19. Ito S, Wakamatsu K. Eine praktische Screening-Methode zur Unterscheidung phenolischer hautaufhellender Tyrosinase-Inhibitoren von Leukodermie-induzierenden Phenolen. J Dermatol Sci 2015;80:18e24.
20. Jeon SH, Kim KH, Koh JU, Kong KH. Hemmende Wirkung der L-Dopa-Oxidation von Tyrosinase durch Hautaufheller. Bull Korean Chem Soc 2005;26:1135e7.
21. Jimbow K, Obata H, Pathak MA, Fitzpatrick TB. Mechanismus der Depigmentierung durch Hydrochinon. J Invest Dermatol 1974;62:436e49.
22. Jimenez M, Garcia-Carmona F. 4-substituierte Resorcine (Sulfit-Alternativen) als langsam bindende Inhibitoren der Tyrosinase-Katecholase-Aktivität. J Agric Food Chem 1997;45:2061e5.
23. Kang HH, Rho HS, Hwang JS, Oh SG. Depigmentierende Aktivität und geringe Zytotoxizität von Alkoxybenzoaten oder Alkoxycinnamat in kultivierten Melanozyten. Chem Pharm Bull (Tokio) 2003;51:1085e8.
24. Kanteev M, Goldfeder M, Fishman A. Struktur-Funktions-Korrelationen in Tyrosinasen. Prot Sci 2015;24:1360e9.
25. Katagiri T, Okubo T, Oyobikawa M, Futaki K, Shaku M, Kawai M, et al. Hemmende Wirkung von 4-n-Butylresorcin auf die Melanogenese und seine hautaufhellende Wirkung. J Soc Cosmet Chem Jpn 2001;35:42e9.
26. Khatib S, Nerya O, Musa R, Shmuel M, Tamir S, Vaya J. Chalcones als potente Tyrosinase-Inhibitoren: die Bedeutung einer 2,4-substituierten Resorcin-Einheit. Bioorg Med Chem 2005;13:433e41.
27. Kim DS, Kim SY, Park SH, Choi YG, Kwon SB, Kim MK, et al. Hemmende Wirkung von 4-n-Butylresorcin auf die Tyrosinaseaktivität und die Melaninsynthese. Biol Pharm Bull 2005;28:2216e9.
28. Kim H, Choi HR, Kim DS, Park KC. Topische hypopigmentierte Mittel bei Pigmentstörungen und ihre Wirkmechanismen. Ann Dermatol 2012;24:1e6.
29. Kim YJ, Uyama H. Tyrosinase-Inhibitoren aus natürlichen und synthetischen Quellen, Struktur, Hemmmechanismus und Perspektive für die Zukunft. Cell Mol Life Sci 2005;62:1707e23.
30. Kolbe L, Mann T, Gerwat W, Batzer J, Ahlheit S, Scherner C, et al. 4-n-Butylresorcin, ein hochwirksamer Tyrosinasehemmer zur topischen Behandlung von Hyperpigmentierung. J Eur Acad Dermatol Venereol 2013;27: 19e23.
31. Lai X, Soler-Lopez M, Wichers HJ, Dijkstra BW. Rekombinante Expression und Reinigung menschlicher Tyrosinase im großen Maßstab, geeignet für Strukturstudien. PLoS One 2016;11:e0161697. 32. Lai X, Wichers HJ, Soler-Lopez M, Dijkstra BW. Die Struktur des menschlichen Tyrosinase-verwandten Proteins 1 zeigt ein zweikerniges aktives Zinkzentrum, das für die Melanogenese wichtig ist. Angew Chem Int Ed Engl 2017;56:9812e5.
33. Lee SY, Baek N, Nam TG. Natürliche, halbsynthetische und synthetische Tyrosinase-Inhibitoren. J Enzyme Inhib Med Chem 2014;31:1e13.
34. Mann T, Gerwat W, Wenck H, Ro¨hm KH, Kolbe L. Isobutylamido Thiazolyl Resorcinol, ein neuer starker Inhibitor der menschlichen Tyrosinase. Pigment Cell Melanoma Res 2017:e85.
35. Matoba Y, Kumagai T, Yamamoto A, Yoshitsu H, Sugiyama M. Kristallographischer Beweis, dass das zweikernige Kupferzentrum der Tyrosinase während der Katalyse FL-flexibel ist. J Biol Chem 2006;281:8981e90.
35. Nesterov A, Zhao J, Minter D, Hertel C, Ma W, Abeysinghe P, et al. 1-(2,4- dihydroxy phenyl)-3-(2,4-dimethoxy-3-methyl phenyl)propan, ein neuartiger Tyrosinase-Inhibitor mit starker depigmentierender Wirkung. Chem Pharm Bull (Tokio) 2008;56:1292e6.
36. Olivares C, Garcia-Borron JC, Solano F. Identifizierung von Resten des aktiven Zentrums, die an der Metall-Cofaktor-Bindung und der stereospezifischen Substraterkennung in Säugetier-Tyrosinase beteiligt sind. Auswirkungen auf den Katalysezyklus. Biochemie 2002;41:679e86.
37. Palumbo A, d'Ischia M, Misuraca G, Prota G. Mechanismus der Hemmung der Melanogenese durch Hydrochinon. Biochim Biophys Acta 1991;1073:85e90.
38. Penney KB, Smith CJ, Allen JC. Die depigmentierende Wirkung von Hydrochinon beruht auf der Störung grundlegender Zellprozesse. J Invest Dermatol 1984;82:308e10.
39. Pretzler M, Bijelic A, Rompel A. Heterologe Expression und Charakterisierung der funktionellen Pilztyrosinase (AbPPO4). Sci Rep 2017;7:1810.
40. Ramsden CA, Riley PA. Tyrosinase: die vier Oxidationsstufen des aktiven Zentrums und ihre Bedeutung für die enzymatische Aktivierung, Oxidation und Inaktivierung. Bioorg Med Chem 2014;22:2388e95.
41. Rescigno A, Sollai F, Pisu B, Rinaldi A, Sanjust E. Tyrosinase-Hemmung, allgemeine und angewandte Aspekte. J Enzyme Inhib Med Chem 2002;17:207e18.
42. Sasaki M, Kondo M, Sato K, Umeda M, Kawabata K, Takahashi Y, et al. Rhododendron, eine depigmentierungsinduzierende Phenolverbindung, übt über einen Tyrosinase-abhängigen Mechanismus eine Melanozyten-Zytotoxizität aus. Pigment Cell Melanoma Res 2014;27:754e63.
43. Schweikardt T, Olivares C, Solano F, Jaenicke E, Garcia-Borron JC, Decker H. Ein dreidimensionales Modell des aktiven Zentrums der Säugetier-Tyrosinase, das den Verlust von Funktionsmutationen erklärt. Pigment Cell Res 2007;20: 394e401.
44. Wissenschaftlicher Ausschuss für Verbraucherprodukte. Meinung zu b-Arbutin; 2008 (abgerufen am 21. November 2017).
45. Wissenschaftlicher Ausschuss für Verbrauchersicherheit. Meinung zu Kojisäure; 2012 (abgerufen am 21. November 2017).
46. Sendovski M, Kanteev M, Ben-Yosef VS, Adir N, Fishman A. Die ersten Strukturen einer aktiven bakteriellen Tyrosinase zeigen Kupferplastizität. J Mol Biol 2011;405: 227e37.
47. Shimizu K, Kondo R, Sakai K. Hemmung der Tyrosinase durch Flavonoide, Stilbene und verwandte 4-substituierte Resorcine: Struktur-Aktivitäts-Untersuchungen. Planta Med 2000;66:11e5.
48. Shimizu MM, Melo GA, Brombini Dos Santos A, Bottcher A, Cesarino I, Arau´jo P, et al. Enzymcharakterisierung, Isolierung und cDNA-Klonierung von Polyphenoloxidase im Herzen von Palmen von drei kommerziell wichtigen Arten. Plant Physiol Biochem 2011;49:970e7.
49. Smith CJ, O'Hare KB, Allen JC. Die selektive Zytotoxizität von Hydrochinon für von Melanozyten abgeleitete Zellen wird durch Tyrosinaseaktivität vermittelt, ist jedoch unabhängig vom Melaningehalt. Pigment Cell Res 1988;1:386e9.
50. Solano F, Briganti S, Picardo M, Ghanem G. Hypopigmentierende Mittel: eine aktualisierte Übersicht über biologische, chemische und klinische Aspekte. Pigment Cell Res 2006;19:550e71.
51. Stratigos AJ, Katsambas AD. Optimale Behandlung hartnäckiger Hyperpigmentierungsstörungen bei dunkelhäutigen Patienten. Am J Clin Derm 2004;5: 161e8.
52. Sugimoto K, Nomura K, Nishimura T, Kiso T, Sugimoto K, Kuriki T. Synthesen von a-Arbutin-a-glycosiden und ihre hemmende Wirkung auf die menschliche Tyrosinase. J Biosci Bioeng 2005;99:272e6.
53. Sun W, Wendt M, Klebe G, Röhm KH. Zur Interpretation der Tyrosinase-Hemmkinetik. J Enzyme Inhib Med Chem 2014;29:92e9.
54. Tripathi RK, Hearing VJ, Urabe K, Aroca P, Spritz RA. Mutationskartierung der katalytischen Aktivitäten menschlicher Tyrosinase. J Biol Chem 1992;267: 23707e12.
55.UniProt-Konsortium. UniProt: die universelle Protein-Wissensdatenbank. Nucleic Acids Res 2017;45:D158e69.
56. US-amerikanische Lebensmittel- und Arzneimittelbehörde, Ministerium für Gesundheit und menschliche Dienste. Arzneimittel zur Hautaufhellung zur rezeptfreien Anwendung beim Menschen; vorgeschlagene Regel. 71 Federal Register 51146-5115521 (kodifiziert nach 21 CFR Part 310); 2006.
57. Vielhaber G, Schmaus G, Jacobs K, Franke H, Lange S, Herrmann M, et al. 4-(1-phenylmethyl)1,3-benzoldiol: ein neues, hocheffizientes Aufhellungsmittel. Int J Cosmet Sci 2007;29:65e6. 58. Wendt M. Rationales Design neuer Tyrosinase-Inhibitoren. Ph.D. These. Marburg, Deutschland: Medizinische Fakultät der Universität Marburg; 2006.
59. Ying YH, Lee SJ, Chung MH, Ying HJ, Suk JL, Myung HC, et al. Aloesin und Arbutin hemmen synergistisch die Tyrosinaseaktivität über einen unterschiedlichen Wirkmechanismus. Arch Pharm Res 1999;22:232e6.
Für weitere Informationen: david.deng@wecistanche.com WhatApp:86 13632399501
