KidneyNetwork: Verwendung von Genexpressionsdaten aus der Niere zur Vorhersage und Priorisierung neuartiger Gene, die an Nierenerkrankungen beteiligt sind Ⅰ
Aug 07, 2023
Gentests bei Patienten mit Verdacht auf erbliche VeranlagungNierenerkrankungDie genetische Ursache der Erkrankung lässt sich möglicherweise nicht erkennen, da potenziell pathogene Varianten in Genen liegen können, von denen noch nicht bekannt ist, dass sie daran beteiligt sindNierenerkrankung. Wir haben das Kidney Network entwickelt, das die gewebespezifische Expression nutzt, um die Priorisierung von Kandidatengenen speziell für Nierenerkrankungen zu informieren. KidneyNetwork ist eine neuartige Methode, die durch die Integration eines Nieren-RNA-Sequenzierungs-Koexpressionsnetzwerks aus 878 Proben mit einem Multigewebenetzwerk aus 31.499 Proben entsteht. Es verwendet Expressionsmuster und etablierte Gen-Phänotyp-Assoziationen, um unvoreingenommen vorherzusagen, welche Gene mit welchen (Krankheits-)Phänotypen in Zusammenhang stehen könnten. Wir haben KidneyNetwork auf seltene Varianten in Exomsequenzierungsdaten von 13 Patienten mit Nierenerkrankungen ohne genetische Diagnose angewendet, um Kandidatengene zu priorisieren. KidneyNetwork kann nierenspezifische Genfunktionen und (Nierenerkrankungs-)Phänotypen für krankheitsassoziierte Gene genau vorhersagen. Die Kreuzung priorisierter Gene mit Genen, die seltene Varianten tragen, bei einem Patienten mit Nieren- und Leberzysten identifizierte ALG6 als plausibles Kandidatengen. Wir untermauern diese Plausibilität, indem wir ALG6-Varianten in mehreren Fällen von zystischer Nieren- und Lebererkrankung ohne alternative genetische Erklärung identifizieren. Wir präsentieren KidneyNetwork, ein öffentlich zugängliches nierenspezifisches Koexpressionsnetzwerk mit optimierten Gen-Phänotyp-Vorhersagen für Phänotypen von Nierenerkrankungen.

Wir haben eine benutzerfreundliche Online-Schnittstelle entwickelt, die es Klinikern und Forschern ermöglicht, Genexpressions- und Co-Regulationsdaten zu nutzenGen-Phänotyp-Verbindungen, um Fortschritte in der Diagnose und Forschung erblicher Nierenerkrankungen zu beschleunigen.
ÜBERSETZUNGSERKLÄRUNG:Gentests bei Patienten mit Verdacht auf erbliche VeranlagungNierenerkrankungmöglicherweise nicht die genetische Ursache für die Erkrankung des Patienten offenlegen. Potenziell pathogene Varianten können in Genen liegen, von denen noch nicht bekannt ist, dass sie an Nierenerkrankungen beteiligt sind, was es schwierig macht, die Relevanz dieser Varianten zu interpretieren. Dies zeigt einen klaren Bedarf an Methoden, um die phänotypischen Folgen genetischer Variationen unvoreingenommen vorherzusagen. Hier beschreiben wir KidneyNetwork, ein Tool, das gewebespezifische Expression nutzt, um nierenspezifische Genfunktionen vorherzusagen. Durch die Anwendung von KidneyNetwork auf eine Gruppe nicht diagnostizierter Fälle wurde ALG6 als Kandidatengen in zystischer Niere identifiziertLeber erkrankung. Zusammenfassend kann KidneyNetwork die Interpretation genetischer Varianten unterstützen und daher bei der translationalen Nephrogenese von Nutzen sein und dazu beitragen, die diagnostische Ausbeute bei Patienten mit Nierenerkrankungen zu verbessern.

KLICKEN SIE HIER, UM CISTANCHE FÜR DIE NIEREN ZU ERHALTENKRANKHEIT
EINFÜHRUNG
Gentests bei Patienten mit Verdacht auf eine erbliche Nierenerkrankung können ursächliche pathogene Varianten aufdeckenNierenbezogene Gene. In vielen Fällen kann eine genetische Ursache jedoch noch nicht nachgewiesen werden. Pathogene Varianten bekannter nierenbezogener Gene werden bei etwa 10–30 Prozent der genetisch getesteten Patienten mit chronischer Nierenerkrankung jeglicher Ursache nachgewiesen [1–3]. Bei diesen Prozentsätzen handelt es sich jedoch wahrscheinlich um Unterschätzungen der Zahl der Patienten mit einer monogenen Ursache, da Varianten in Genen, die noch nicht an Nierenerkrankungen beteiligt sind, unbemerkt bleiben. In diesen Genen können sich potenziell schädliche Varianten befinden, was die Priorisierung und Interpretation der Relevanz dieser Varianten erschwert. Daher besteht im gegenwärtigen Zeitalter der Genommedizin eine der größten Herausforderungen nach einem negativen Diagnoseergebnis bei bekannten Genen darin, neue Kandidatengene mit potenziell pathogenen Varianten zu erkennen und zu priorisieren, die die Krankheit des Patienten erklären können [4].
RNA-Sequenzierungsdaten können zur Vorhersage des Kandidaten verwendet werdenKrankheitsgene[5]. Wir haben kürzlich GeneNetwork und die GeneNetwork-Assisted Diagnostic Optimization (GADO)-Methode entwickelt, um neue Kandidatengene für Krankheiten auf der Grundlage von RNA-Sequenzierungsdaten zu priorisieren [6]. Die Idee hinter dieser Methode ist, dass bestimmte seltene Erkrankungen durch Varianten in mehreren Genen verursacht werden können. Obwohl diese Gene unterschiedlich sind, haben sie normalerweise ähnliche biologische Funktionen. Bei der Untersuchung von Genexpressionsdaten aus einer großen Anzahl von Proben zeigen diese Krankheitsgene normalerweise eine starke Koexpression [6]. Wenn es also andere Gene gibt, die stark mit bekannten Genen für seltene Krankheiten koexprimiert werden, ist es möglich, dass Varianten dieser anderen Gene ebenfalls dieselbe Krankheit verursachen können.
Damit ein solches Tool optimal funktioniert, sollten die Koexpressionsinformationen so genau wie möglich sein. Für GADO haben wir ein Gen-Koexpressionsnetzwerk basierend auf öffentlich verfügbaren RNA-Sequenzierungsdatensätzen aus vielen verschiedenen Geweben aufgebaut und dieses Netzwerk verwendet, um vorherzusagen, welche Gene seltene Krankheiten verursachen könnten. Diese Vorhersagen wurden mithilfe der Human Phenotype Ontology (HPO)-Datenbank trainiert [7]. In der HPO-Datenbank werden Gene Phänotypen – sogenannten HPO-Begriffen – zugeordnet, die auf Anmerkungen zu Genkrankheiten und Krankheitssymptomen basieren, die in den Datenbanken OMIM (8) und Orphanet (9) vorhanden sind. Durch die Integration der Informationen aus der HPO-Datenbank mit dem Gen-Koexpressionsnetzwerk konnten wir Vorhersagewerte für jedes Gen pro HPO-Term berechnen. Zusammen bilden diese Ergebnisse GeneNetwork. GADO priorisiert dann Gene, indem es eine Eingabeliste von HPO-Begriffen, die den Phänotyp des Patienten beschreiben, mit einer Liste von Genen mit möglichen schädlichen Varianten dieses Patienten kombiniert. Die Priorisierung der Genliste basiert auf den kombinierten Genvorhersagewerten für die eingegebenen HPO-Begriffe [6].
Da wir beobachteten, dass die Vorhersageleistung von GeneNetwork für nierenbezogene HPO-Phänotypen begrenzt war, versuchten wir, die Vorhersage durch die Entwicklung eines nierenspezifischen Netzwerks zu verbessern. Dazu haben wir 878 Nieren-RNA-Sequenzierungsproben verwendet, die wir mit einem vorhandenen Datensatz von 31.499 Proben aus anderen Geweben angereichert haben [6]. Durch die Entwicklung eines neuen Vorhersagealgorithmus, der die in beiden Datensätzen vorhandenen Informationen gewichten kann, haben wir die Leistung für nierenbezogene Pfade verbessert. In diesem Artikel stellen wir das resultierende KidneyNetwork vor, ein Koexpressionsnetzwerk, das zur genauen Vorhersage von Gen-Phänotyp-Assoziationen von Genen verwendet werden kann, die für nierenbezogene HPO-Begriffe unbekannt sind. Als Grundsatzbeweis haben wir KidneyNetwork auf Exomsequenzierungsdaten einer Gruppe von Patienten mit bisher ungelösten Nierenerkrankungen angewendet.
METHODEN
Um die Vorhersage nierenbezogener Phänotypen zu verbessern, haben wir RNA-Sequenzierungsdaten aus Nieren gesammelt, GeneNetwork mit neueren Referenzdatenbanken und verbesserten statistischen Analysen aktualisiert und anschließend gewebespezifische Informationen integriert.
Datensätze in KidneyNetwork
RNA-Sequenzierungsdaten aus ausgewählten Nierenproben unterschiedlicher Herkunft, einschließlich Primär-, Tumor- und fötalem Gewebe, wurden mit einem vorhandenen Datensatz zur Multigewebe-RNA-Sequenzierung kombiniert, der als Grundlage für unser zuvor beschriebenes GeneNetwork [6] diente (Tabelle S1, S2). . Wir haben uns aus zwei Gründen für die Einbeziehung des Multigewebe-Datensatzes entschieden. Zunächst benötigten wir eine ausreichende Anzahl von Proben, um ein Basisnetzwerk aufzubauen. Zweitens wollten wir die Expression bewahren, die für mehrere oder alle Nierenzelltypen spezifisch ist, nicht jedoch für andere Gewebe. Wir haben dies getan, weil Gen-Phänotyp-Scores auf Expressionsunterschieden zwischen Proben basieren. Wenn alle Gene in allen in die Analyse einbezogenen Proben eine hohe (oder niedrige) Expression aufweisen, liefern sie keine ausreichenden Informationen zum Vorhersagealgorithmus. Der Multigewebe-Datensatz menschlicher RNA-Sequenzierungsproben, der zur Entwicklung von GeneNetwork verwendet wurde, wurde wie zuvor beschrieben wiederverwendet und verarbeitet [6]. Nach der Vorverarbeitung enthielt dieser Datensatz 31.499 Proben und 56.435 Gene.
3.194 aus der Niere stammende RNA-sequenzierte Proben wurden vom European Nucleotide Archive (ENA) und dem Genotype-Tissue Expression (GTEx) Project heruntergeladen (Anmerkung S1). Die Vorverarbeitung des Nierendatensatzes erfolgte ähnlich wie beim Multigewebe-Datensatz [6] (Anmerkung S2, Anmerkung S3). Nach der Proben- und Genauswahl blieben 58.283 Gene und 878 Nierenproben übrig. Wir untersuchten die verbleibenden 878 RNA-Sequenzierungsproben mit dem UMAP-Clustering-Algorithmus (Hinweis S4).
HPO-Filterung. Für die Konstruktion von KidneyNetwork verwendeten wir Gen-Phänotyp-Assoziationen aus der HPO-Datenbank [7] Version 1268. In der HPO-Datenbank basiert die Annotation von Genen zu HPO-definierten Phänotypen auf den Gen-Krankheitsanmerkungen im OMIM [8] morbid Karte (heruntergeladen am 26. März 2018) und die Orphanet [9] „en_product6.xml“-Dateiversion 1.3.1. Anmerkungen zu Genkrankheiten in diesen Datenbanken können auf mehreren Faktoren basieren, einschließlich statistischer Zusammenhänge und großräumiger Variationen der Kopienzahl. Wir wollten KidneyNetwork nur mit Genen trainieren, bei denen der Zusammenhang zwischen Gen und der seltenen Krankheit gut belegt ist. Daher haben wir die multigenen Syndrome ausgeschlossen, da oft nicht klar ist, welche Gene in den Kopiezahlvarianten zu welchen Phänotypen beitragen. Wir haben auch bloße Suszeptibilitätsgene ausgeschlossen (Anmerkung S5).
Ausdrucksnormalisierung. Nach der Proben- und Genqualitätskontrolle (QC) wurde die Expressionsmatrix der verbleibenden Proben und Gene log{0}}-transformiert und die Genzahlen wurden unter Verwendung von DESeq nach der Median-of-Ratios-Methode normalisiert. Anschließend haben wir die Genexpressionsdaten für Kovariaten korrigiert (Anmerkung S6).
Zersetzung
Nach der Filterung und Qualitätskontrolle des gesamten Datensatzes bestand der nächste Schritt darin, eine Zerlegung durchzuführen, um die Eigenvektoren des Datensatzes zu berechnen (Hinweis S7). Sowohl für GeneNetwork als auch für das Genregulationsnetzwerk basierend auf Nierendaten haben wir die optimale Anzahl von Komponenten definiert (Anmerkung S8). Die ersten 165 Eigenvektoren für GeneNetwork und die ersten 170 Eigenvektoren für die aus Nieren abgeleiteten Daten wurden identifiziert und zu einer größeren Matrix zusammengeführt, die alle 335 Eigenvektoren enthält.
Berechnung des Gen-HPO-Term-Scores Die Berechnung des Gen-Phänotyp-Scores erfolgte in mehreren Schritten (Abb. S5). Zuerst führten wir eine logistische Regression durch, wobei wir die kombinierten Eigenvektoren und die Gen-Phänotyp-Annotationsdatei als Eingabe verwendeten. Wir haben die resultierenden Werte und die Eigenvektor-Scores verwendet, um einen Gen-Log-Odds-Score für jedes Gen in jedem Eigenvektor zu berechnen (Anmerkung S9).

Um eine Überanpassung der Gen-Log-Odds-Scores bereits annotierter Gene zu vermeiden, haben wir einen Ansatz zur einmaligen Kreuzvalidierung angewendet (Hinweis S10). Die Log-Odds wurden anschließend unter Verwendung einer permutierten Nullverteilung für jeden Phänotyp in Gen-Z-Scores übersetzt (Anmerkung S11).
Um die Vorhersagegenauigkeit zu bestimmen, haben wir die Fläche unter der ROC-Kurve (AUC) berechnet. Die AUC wurde pro HPO-Term unter Verwendung der vorhergesagten Gen-Z-Scores und bekannter Anmerkungen berechnet. Die Signifikanz der Vorhersagen wurde mithilfe des zweiseitigen Mann-Whitney-Rangtests berechnet. Nach der Bonferroni-Korrektur wurde eine Vorhersage bei p < 0.05 als signifikant angesehen.
Vergleich der Vorhersageleistung
Wir verglichen die Vorhersageleistung von vier verschiedenen Netzwerken: (1) dem ursprünglichen GeneNetwork, (2) dem aktualisierten GeneNetwork, (3) dem nierenspezifischen Genregulationsnetzwerk, das ausschließlich auf Nierenproben basiert, und schließlich (4) KidneyNetwork, das kombiniert die letzten beiden. Die Qualität der von diesen Netzwerken gemachten HPO-Vorhersagen wurde anhand der AUC für jeden nierenbezogenen Phänotyp bewertet (Tabelle S3). Eine verbesserte Qualität eines Netzwerks wurde definiert als eine verbesserte Vorhersagegenauigkeit für nierenbezogene Begriffe, die bei jedem Vergleich zweier Netzwerke signifikant vorhergesagt wurden, und durch eine erhöhte Anzahl signifikant vorhergesagter nierenbezogener Begriffe. Die Bedeutung der Verbesserung der Vorhersagegenauigkeit eines Netzwerks im Vergleich zu einem anderen wurde mithilfe des im pROC R-Paket integrierten DeLong-Tests [10] bewertet [11].
Anwendung von KidneyNetwork bei 13 Patienten mit Verdacht auf erbliche Nierenerkrankung Eine der Anwendungen von KidneyNetwork ist die Priorisierung von Kandidatengenen bei Patienten mit ungelöster Nierenerkrankung. Um diese klinische Anwendung zu bewerten, verwendeten wir KidneyNetwork, um Kandidatengene für Patienten mit verschiedenen Nierenerkrankungen mithilfe der GADO-Methode zu priorisieren [6]. GADO kombiniert die über KidneyNetwork gerenderten Genvorhersage-Z-Scores für einen bestimmten Satz von HPO-Begriffen. Gene mit einem kombinierten Z-Score größer oder gleich 5 für den eindeutigen Satz von HPO-Begriffen, die jedem Patienten zugeordnet sind, wurden als potenzielle Kandidatengene für diesen Patienten angesehen.

Abb. 1 UMAP-Visualisierung der aus der Niere abgeleiteten Expressionsdaten. 878 Proben wurden in drei Hauptcluster eingeteilt: gesundes Primärgewebe (Mitte und unten), Entwicklungsproben (links) und Proben von Nierenzellkarzinomen (RCC) (rechts). Auf der linken Seite der Abbildung ist die Anhäufung von Podozyten aus pluripotenten Stammzellen (PSC) und aus PSC abgeleiteten Organoiden mit primären fetalen Proben und Nephron-Vorläuferzellen zu sehen. Auf der rechten Seite gruppieren sich RCC-Proben in der Nähe von proximalen Tubulusproben, und der RCC-Cluster, der gesunden Primärgewebeproben am nächsten liegt, besteht aus nicht klarzelligen RCC-Proben (nccRCC). In der Mitte und unten gruppieren sich gesunde Primärnierenproben nach ihrem Ursprungsgewebe.
Bei allen 13 in die Studie einbezogenen Patienten wurde eine monogene Nierenerkrankung vermutet, es lag jedoch keine genetische Diagnose vor (Anmerkung S12). Diesen Fällen wurden HPO-Begriffe basierend auf ihrem Phänotyp zugeordnet. Für jeden Patienten wurden die vollständigen Exomsequenzierungsdaten mit CAPICE [12] analysiert, um potenziell pathogene Varianten zu identifizieren. Gene, die Varianten mit einem gnomAD-Popmax-Filter-AF enthalten [13]<0.005 and a recall ≥99%, corresponding with a mild CAPICE cut-off of ≥0.0027, were considered interesting candidates.
Die Überlappung der durch die KidneyNetwork-Integration in GADO identifizierten Gene mit den durch CAPICE identifizierten Genen führte zu einer Liste von Genen für jeden Patienten. Diese Gene und Varianten in diesen Genen wurden von einem Nephrogenese-Expertengremium (AMvE, LRC, NVAMK) manuell auf ihr pathogenetisches Potenzial überprüft, basierend auf Populationsmetriken, Vorhersagetools, verfügbarer Literatur und Segregation (Anmerkung S13). Für das resultierende Kandidatengen wurden über Mitarbeiter und das 100,000 Genomes Project weitere Patienten identifiziert, die Varianten desselben Gens tragen [14]. Außerdem wurde das GeneMatcher-Tool [15] verwendet und brachte bis zum 15. Februar 2023 keine zusätzlichen Patienten.
Identifizierung zusätzlicher Patienten Die zuvor beschriebene Kohorte ungelöster polyzystischer Nieren- und Lebererkrankungen [16] wurde zur Bewertung seltener Varianten herangezogen (Anmerkung S14). Wir verwendeten den genauen Fisher-Test, um die Häufigkeit der identifizierten Variante(n) mit der europäischen Untergruppe der nicht-finnischen Europäer in der gnomAD-Datenbank zu vergleichen [17]. Darüber hinaus nutzten wir das 100,000 Genomes Project [14] zur Identifizierung zusätzlicher Patienten auf Basis der identifizierten Variante(n) (Anmerkung S15).

ERGEBNISSE
Datenabruf und Probenclusterung Wir haben 878 Nierenproben ausgewählt (Abb. S2), die wir mithilfe des UMAP-Algorithmus geclustert und dargestellt haben (Abb. 1). Im Allgemeinen gruppieren sich die Daten in drei Hauptcluster: primäre Nicht-Tumor-Nierendaten, Proben aus der Nierenentwicklung sowie Proben aus proximalen Tubuli, Glomeruli und Nierenzellkarzinomen (RCC).
KidneyNetwork verbessert die Vorhersage von Gen-Phänotypen. Zuerst haben wir GeneNetwork mit der aktualisierten HPO-Datenbank aktualisiert (Abb. S6) und die Pipeline zum Aufbau des Gennetzwerks optimiert (Abb. S7). Diese Änderungen führten zu einer Verbesserung des allgemeinen GeneNetwork im Vergleich zur Vorgängerversion (Abb. S8). Anschließend nutzten wir die verbesserte Pipeline, um das nierenspezifische Genregulationsnetzwerk aufzubauen. Angesichts der geringen Stichprobengröße schnitt diese Version des nierenspezifischen Netzwerks erwartungsgemäß weniger gut ab als GeneNetwork (Abb. S9). Anschließend lieferte die Kombination von GeneNetwork und dem nierenspezifischen Gen-Koexpressionsnetzwerk in KidneyNetwork unsere besten Ergebnisse für nierenbezogene HPO-Begriffe (Abb. 2A; Tabelle S5). Die Vorhersage-AUC, Präzision, Empfindlichkeit und f1--Scores für jeden vorhergesagten Pfad werden bereitgestellt (Tabelle S6).
Zwei Beispiele für verbesserte nierenbezogene HPO-Begriffe sind Hypomagnesiämie und tubulointerstitielle Anomalie (Abb. 2B). Die Visualisierung dieser Phänotypen in Dichtediagrammen zeigt höhere Priorisierungs-Z-Scores für bekannte krankheitsbezogene Gene im Vergleich zu nicht annotierten Genen. Bei unbekannten Genen gilt: Je höher der Vorhersage-Z-Score, desto wahrscheinlicher ist es, dass es sich um ein mögliches Krankheitsgen handelt. Die Visualisierung der Geninteraktionsnetzwerke bekannter Krankheitsgene auf der Grundlage der Vorhersagewerte zeigt erneut die Zunahme der Anzahl und Stärke der Interaktionen, die mit KidneyNetwork im Vergleich zu GeneNetwork erzielt wurden.
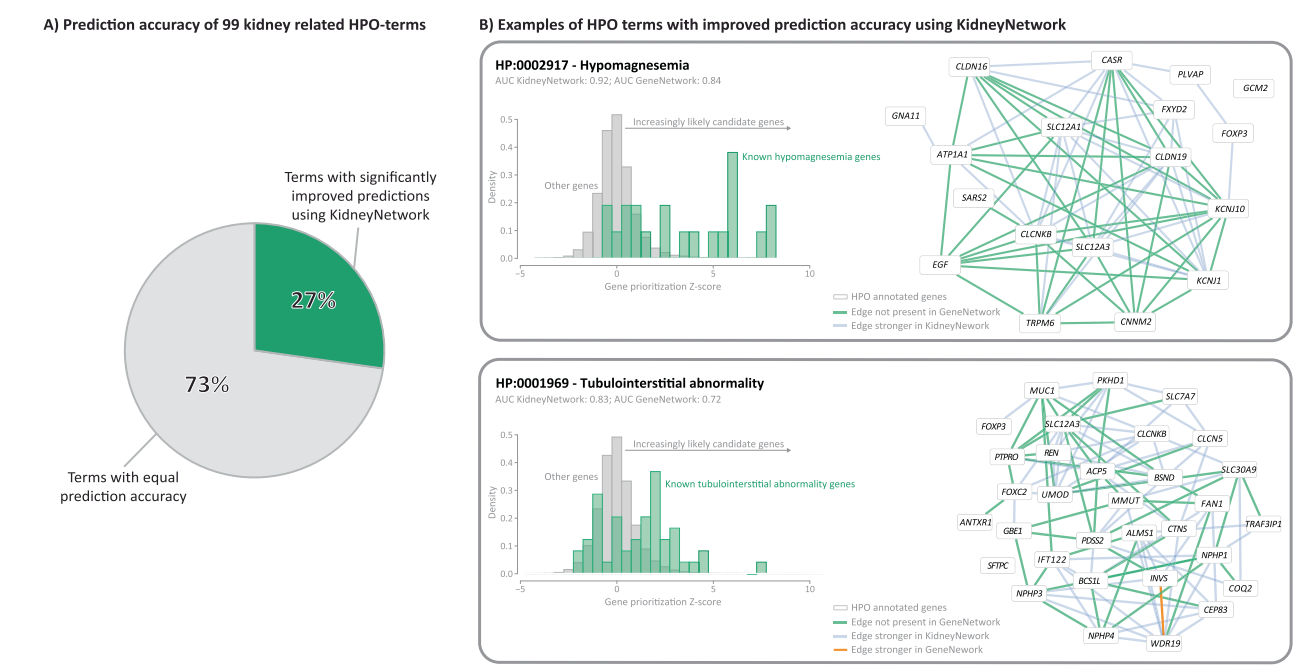
Abb. 2 KidneyNetwork schneidet bei nierenbezogenen HPO-Begriffen besser ab als das aktualisierte GeneNetwork. 27 Prozent der nierenbezogenen Phänotypen lassen sich mit KidneyNetwork deutlich besser vorhersagen als mit GeneNetwork. B Dichtediagramme der Genvorhersagewerte innerhalb von zwei der am stärksten verbesserten Phänotypen, Hypomagnesiämie und tubulointerstitielle Anomalie, zeigen höhere Vorhersagewerte für die für den Phänotyp annotierten Gene und sagen auch potenzielle unbekannte Kandidatengene voraus. Die mit KidneyNetwork vorhergesagten Netzwerke zeigen mehr und stärkere Korrelationen zwischen den annotierten Genen als die mit GeneNetwork vorhergesagten Netzwerke.
Wir sahen auch einen Anstieg der Anzahl signifikanter vorhergesagter nierenbezogener HPO-Begriffe für KidneyNetwork (n=71) im Vergleich zu GeneNetwork (n=63). Dies führte uns zu der Hypothese, dass KidneyNetwork nierenbezogene Begriffe insgesamt mit höherer Genauigkeit vorhersagt und daher in der Lage ist, mehr nierenbezogene Phänotypen mit höherer Signifikanz vorherzusagen. Ein gepaarter t-Test zeigt, dass der HPO-AUC-Wert für KidneyNetwork im Vergleich zu GeneNetwork insgesamt deutlich besser war (mittlere AUC: 0.76 gegenüber 0.74; t-Test-p-Wert: 4,5 × 10 −8 ). Dieses Ergebnis legt nahe, dass KidneyNetwork mehr nierenspezifische HPO-Terme mit einer höheren Vorhersagegenauigkeit vorhersagt als GeneNetwork.
KidneyNetwork priorisiert ALG6 als mögliches Krankheitsgen bei Patienten mit Nierenzysten und Leberzysten. Um den klinischen Nutzen von KidneyNetwork zu untersuchen, haben wir Gene für 13 Patienten mit Verdacht auf erbliche Nierenerkrankung, aber ohne genetische Diagnose priorisiert und diese mit Genen gekreuzt, die potenziell pathogene Varianten enthalten. Die resultierenden Genlisten enthielten 1–4 Kandidatengene für 9 der 13 Patienten (Tabelle S7). Bei einem Patienten (SAMPLE6) identifizierte die manuelle Kuratierung dieser Liste ALG6 (ALG6 alpha-1,3-glucosyltransferase) als potenzielles Kandidatengen zur Erklärung der Nieren- und Leberzysten des Patienten (Abb. 3). Der kombinierte Z-Score für ALG6 für die unterstellten HPO-Terme war in KidneyNetwork nach mehrfacher Testkorrektur signifikant (z=5,43). Dieses Gen wäre übersehen worden, wenn wir GeneNetwork verwendet hätten: Dort erreichte ALG6 nicht die Signifikanzschwelle des Z-Scores größer oder gleich 5.

ALG6 als Kandidatengen für Patienten mit Nieren- und Leberzysten Die von SAMPLE6 getragene ALG6-Variante c.680 plus 2 T > G ist heterozygot. Dies ist eine bekannte pathogene Spleißstellenvariante, die zu einer angeborenen Glykosylierungsstörung (CDG) Typ Ic führt, wenn pathogene Varianten auf beiden Allelen vorhanden sind [18, 19]. ALG6 ähnelt stark ALG8, das an den Phänotypen von Nieren- und Leberzysten beteiligt ist [20], und laut KidneyNetwork sind ALG6 und ALG8 stark koreguliert (Z-Score=8.59).
Angesichts dieser biologischen Plausibilität haben wir eine Kohorte von 120 unabhängigen Fällen von polyzystischer Nieren- und Lebererkrankung nach seltenen Varianten, MAF < 0.001, in ALG6 befragt. Diese Kohorte wurde geringfügig aktualisiert, da sie zuvor beschrieben wurde, und wurde durch Exomsequenzanalyse aufgrund von Mutationen mit Funktionsverlust oder gemeldeten pathogenen nicht-verkürzenden Varianten in PKD1, PKD2, PRKCSH, SEC63, GANAB, ALG8, ALG9, SEC61B, PKHD1 oder anderen ausgeschlossen DNAJB11 [16]. Drei nicht verwandte Fälle (YU372, YU378, YU481) trugen seltene ALG6-Varianten; jeder hatte das gleiche ALG6 c.257 plus 5 G > Eine nichtkanonische Spleißvariante, von der bekannt ist, dass sie für ALG6-CDG pathogen ist und in vitro den Spleiß verändert [19, 21]. Trotz einer gemeinsamen Mutation berichten diese drei Fälle jeweils, dass keine bekannten betroffenen Familienmitglieder aus verschiedenen Bundesstaaten der Vereinigten Staaten registriert wurden, und stehen in keinem Zusammenhang mit der besten Nachweisgrenze unter Verwendung des VCFtools-Relatedness2-Algorithmus mit einem Verwandtschafts_PHI < 0,005.
Angesichts der Darstellung dieser Variante in drei Fällen europäischer Abstammung in dieser phänotypisch definierten Kohorte haben wir ihre Häufigkeit in der europäischen Teilmenge der Fälle (n=105) mit nicht-finnischen Europäern in gnomAD [17] mit einer Abdeckung von verglichen diese Position (n=64,466) [17]. In der Patientenkohorte enthielten 3 von 210 Allelen diese Variante, während sie in gnomAD, einer Kohorte, die hinsichtlich der Nieren- oder Leberzystenbelastung nicht ausgewählt wurde, in 121 von 128.932 Allelen gefunden wurde. Diese ungefähr 10-fache Anreicherung ist nach Fishers exaktem Test statistisch signifikant, p=0.0011. Diese Mutation trat auch bei ALG6-CDG wieder auf [19].
Wir untersuchten auch den Datensatz des 100,000 Genomes Project [14] und kontaktierten Mitarbeiter, die drei zusätzliche Daten für die Anwendung auf Nierenerkrankungen identifizierten. Ein erheblicher Anteil der Patienten mit Verdacht auf eine genetisch bedingte Nierenerkrankung bleibt ohne genetische Diagnose, da die Liste der Krankheitsgene für viele Erkrankungen unvollständig ist. Die Identifizierung der an Nierenerkrankungen beteiligten Gene ist für die Verbesserung der Diagnoseausbeute bei Patienten mit Nierenerkrankungen und für die Untersuchung der Krankheitspathogenese im Hinblick auf Behandlungsmöglichkeiten von entscheidender Bedeutung. Die Etablierung neuartiger Krankheitsgene erfordert eine sorgfältige biologische Validierung. Es ist von entscheidender Bedeutung, Gene einzubeziehen, die einer solchen Untersuchung würdig sind. Die Anwendung von KidneyNetwork in Verbindung mit WES- oder GWAS-Daten durch Nephrologen, klinische Genetiker oder Forscher wird jeder dieser Gruppen helfen, sich an der Genimplikation zu beteiligen. KidneyNetwork kombiniert ein Koexpressionsnetzwerk basierend auf einem Nierenprobendatensatz mit dem zuvor veröffentlichten Multigewebe-Datensatz, der zum Aufbau der GeneNet-Arbeit verwendet wurde. Die Kombination der Datensätze in KidneyNetwork verbesserte Phänotypvorhersagen im Zusammenhang mit Nierenerkrankungen im Vergleich zu Netzwerken, die auf den beiden Datensätzen separat basieren. Als Grundsatzbeweis zeigen wir, dass die von KidneyNetwork erstellte Kandidatengenliste für den kombinierten Phänotyp von Nieren- und Leberzysten eine überschaubare Liste von Kandidatengenen aus einer langen Liste von Genen mit seltenen Varianten bei unserem Patienten mit diesem Phänotyp priorisierte.
Wir untersuchten auch den Datensatz des 100,000 Genomes Project [14] und kontaktierten Mitarbeiter, die drei weitere Patienten mit Nieren- und/oder Leberzysten identifizierten, die eine heterozygote potenziell schädliche Variante in ALG6 trugen, ohne eine alternative genetische Erklärung.

Abb. 3 KidneyNetwork integriert in die GADO-Methode in SAMPLE6, einem Patienten mit Nieren- und Leberzysten. 89 Kandidatengene aus allen Genen wurden von KidneyNetwork mithilfe von GADO priorisiert, basierend auf den HPO-Begriffen „Renal cysts“ (HP:0000107) und „Hepatic cysts“ (HP:0001407). Die CAPICE-Methode zur Interpretation der Exomsequenzierungsdaten ergab 322 Gene, die potenziell pathogene Varianten in den Exomsequenzierungsdaten des Patienten enthielten. Bei der Überlappung dieser Genlisten wurden drei Gene identifiziert, die die Auswahlkriterien erfüllten, eines davon war ALG6.
Insgesamt identifizierten wir sieben Patienten mit bekannten Spleißstellenvarianten, von denen berichtet wurde, dass sie bei stark betroffenen CDG-Patienten aufgrund von Homozygotie oder zusammengesetzter Heterozygotie krankheitsverursachend sind, und einen Patienten mit einer wahrscheinlich pathogenen Spleißstellenvariante (Tabelle 1). Im Gegensatz zu den schwer betroffenen ALG6-CDG-Patienten (mit Beteiligung mehrerer Organe einschließlich Entwicklungsverzögerung und mehreren neurologischen Symptomen) wiesen unsere Patienten einen Phänotyp aus mehreren Nierenzysten und/oder Leberzysten auf (Abb. 4). . Während PCLD ausgedehnt sein kann, scheint der Nierenphänotyp mild zu sein und es wurde trotz fortgeschrittenem Alter kein Rückgang der eGFR gemeldet (d. h. eine Patientin ist in den Dreißigern, die anderen sind zwischen 45 und 80 Jahre alt). Darüber hinaus stellten wir fest, dass sich die ALG6-Variante bei einigen ebenfalls betroffenen Familienmitgliedern abspaltete (Tabelle 1; Abb. 4).
Unterstützender Service:
E-Mail:wallence.suen@wecistanche.com
WhatsApp/Tel: plus 86 15292862950
Geschäft:
https://www.xjcistanche.com/cistanche-shop






