Hautaufheller: Medizinisch-chemische Perspektive von Tyrosinase-Inhibitoren Teil 1
May 05, 2023
ABSTRAKT
Melanogenese ist ein Prozess zur Synthese von Melanin, das hauptsächlich für die Pigmentierung der menschlichen Haut, Augen und Haare verantwortlich ist. Obwohl zahlreiche enzymatisch katalysierte und chemische Reaktionen am Melanogeneseprozess beteiligt sind, spielen Enzyme wie Tyrosinase und Tyrosinase-verwandtes Protein -1 (TRP-1) und TRP-2 eine wichtige Rolle bei Melanin Synthese. Insbesondere ist Tyrosinase ein Schlüsselenzym, das einen geschwindigkeitsbestimmenden Schritt der Melaninsynthese katalysiert, und die Herunterregulierung von Tyrosinase ist der wichtigste Ansatz für die Entwicklung von Melanogenese-Inhibitoren. Daher wurden in den letzten Jahren zahlreiche Inhibitoren entwickelt, die auf Tyrosinase abzielen. Die Übersicht konzentriert sich auf die jüngste Entdeckung von Tyrosinase-Inhibitoren, die direkt an der Hemmung der katalytischen Aktivität und Funktionalität von Tyrosinase aus allen Quellen beteiligt sind, einschließlich synthetischer Labormethoden, Naturstoffen, virtuellem Screening und strukturbasierten molekularen Docking-Studien.
Relevanten Studien zufolge ist Cistanche ein weit verbreitetes Kraut, das als „das Wunderkraut, das das Leben verlängert“ bekannt ist. Sein Hauptbestandteil ist Cistanosid, das verschiedene Wirkungen hat, wie z. B. antioxidative, entzündungshemmende und die Immunfunktion fördernde Wirkung. Der Mechanismus zwischen Cistanche und Hautaufhellung liegt in der antioxidativen Wirkung von Cistanche-Glykosiden. Melanin in der menschlichen Haut entsteht durch die durch Tyrosinase katalysierte Oxidation von Tyrosin. Die Oxidationsreaktion erfordert die Beteiligung von Sauerstoff, sodass die sauerstofffreien Radikale im Körper zu einem wichtigen Faktor werden, der die Melaninproduktion beeinflusst. Cistanche enthält Cistanosid, ein Antioxidans, das die Entstehung freier Radikale im Körper reduzieren und so die Melaninproduktion hemmen kann.

Klicken Sie auf So verwenden Sie Cistanche
Für mehr Information:
david.deng@wecistanche.com WhatApp:86 13632399501
SCHLÜSSELWÖRTER
menschliche Tyrosinase; Inhibitoren; Parkinson-Krankheit; Struktur-Aktivitäts-Beziehungen; Hautaufheller
Einführung
Es wird geschätzt, dass etwa 15 Prozent der Weltbevölkerung in Hautaufheller investieren, wobei der Schwerpunkt auf Asien liegt1. Globale Branchenanalysten (GIA) haben vorausgesagt, dass der Weltmarkt für Hautaufheller bis 2020 ein Volumen von 23 Milliarden US-Dollar erreichen wird, angetrieben durch neue Märkte in Asien, insbesondere Indien, Japan und China2. Laut dem SIRONA Biochem-Bericht1 wurden im asiatisch-pazifischen Raum etwa 13 Milliarden US-Dollar für Hautpflegeprodukte und Kosmetika ausgegeben. Allein in Indien wurden im Jahr 2010 schätzungsweise 432 Millionen US-Dollar für hautaufhellende Cremes und Hautpflegemittel ausgegeben. Eine aktuelle Umfrage ergab, dass 80 Prozent der indischen Männer Fairness-Cremes verwenden und die Zahl der Verbraucher jährlich um 18 Prozent wächst1. Der molekulare Mechanismus dieser hautaufhellenden Wirkstoffe besteht darin, Melanin zu reduzieren, das die Hauptquelle der Hautfarbe ist.
Melanin ist in erster Linie für die Pigmentierung der menschlichen Haut, Augen und Haut verantwortlich und wird aus Melanozyten der Epidermis in einem ungefähren Verhältnis von 1:36 zu basalen Keratinozyten hergestellt3. Als Reaktion auf die Bestrahlung mit ultraviolettem B (UVB) synthetisieren Melanozyten Melanin durch den Prozess, der Melanogenese genannt wird. Das synthetisierte Melanin in Melanosomen wird zu benachbarten Keratinozyten in der Epidermis transportiert4. Unter normalen physiologischen Bedingungen wirkt sich die Pigmentierung günstig auf den Lichtschutz der menschlichen Haut vor schädlichen UV-Schäden aus und spielt eine wichtige evolutionäre Rolle bei der Tarnung und Tiermimikry5. Eine übermäßige Produktion von Melanin verursacht jedoch dermatologische Probleme wie Sommersprossen, Lentigo solaris (Altersflecken) und Melasma6–9 sowie Krebs10 und postinflammatorische Melanodermie11. Darüber hinaus kann eine kontinuierliche UV-Bestrahlung zu DNA-Schäden, Genmutationen, Krebsentstehung und einer Beeinträchtigung des Immunsystems oder Lichtalterung führen12.
Regulierung der Melanogenese
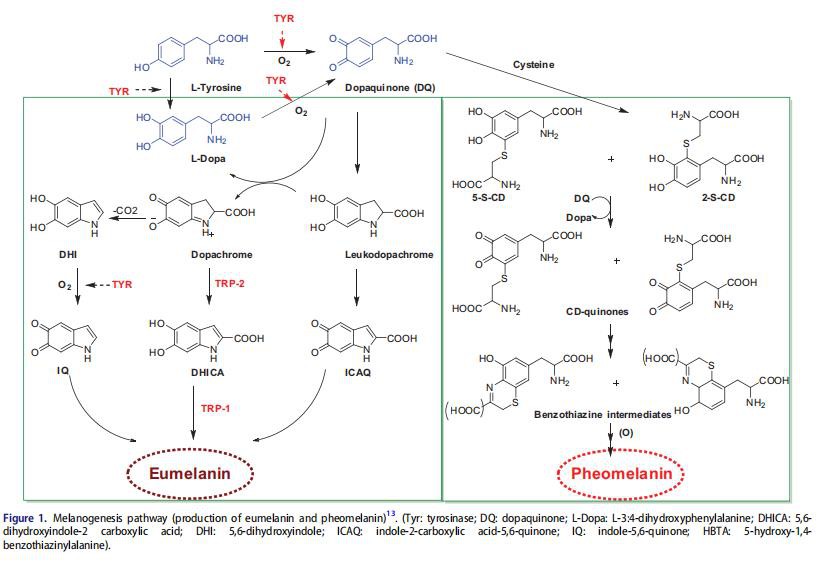
Melanogenese ist ein komplexer Weg, der eine Kombination aus enzymatischen und chemisch katalysierten Reaktionen umfasst. Melanozyten produzieren zwei Arten von Melanin: Eumelanin (braun-schwarz) und Phäomelanin (rot-gelb), die durch die Konjugation von Cystein oder Glutathion gebildet werden (Abbildung 1) 13–15.
Der Melanogeneseprozess wird mit der Oxidation von L-Tyrosin zu Dopaquinon (DQ) durch das Schlüsselenzym Tyrosinase (TYR) eingeleitet. Das resultierende Chinon dient als Substrat für die Synthese von Eumelanin und Phäomelanin16,17. Die Bildung von DQ ist ein geschwindigkeitsbestimmender Schritt in der Melaninsynthese, da der Rest der Reaktionssequenz bei einem physiologischen pH-Wert von 17 spontan ablaufen kann. Nach der DQ-Bildung erfolgt eine intramolekulare Cyclisierung zur Bildung von Indolin und Leukodopachrom (Cyclodopa). . Durch den Redoxaustausch zwischen Leukodopachrom und DQ entstehen Dopachrom und L-3,4-Dihydroxyphenylalanin (L-DOPA), das auch ein Substrat für TYR ist und vom Enzym wieder zu DQ oxidiert wird. Dopachrom zersetzt sich allmählich zu Dihydroxyindol (DHI) und Dihydroxyindol-2-carbonsäure (DHICA). Der letztere Prozess wird durch TRP-2 katalysiert, das heute als Dopachrom-Tautomerase (DCT) bekannt ist. Letztendlich werden diese Dihydroxyindole (DHI und DHICA) zu Eumelanin oxidiert. Es wird angenommen, dass TRP-1 die Oxidation von DHICA zu Eumelanin katalysiert. Daneben wird DQ in Gegenwart von Cystein oder Glutathion in 5-S-Cysteinyldopa oder Glutothionyldopa umgewandelt. Durch die anschließende Oxidation entstehen Benzothiazin-Zwischenprodukte und schließlich Phäomelanin. Obwohl drei Enzyme, TYR, TRP-1 und TRP-2, am Melanogeneseweg beteiligt sind, ist Tyrosinase ausschließlich für die Melanogenese notwendig.
Tyrosinase und ihre Schlüsselrolle bei der Melaninsynthese
Tyrosinase (Monophenol oder o-Diphenol, Sauerstoffoxidoreduktase, EC 1.14.18.1, syn. Polyphenoloxidase), ein multifunktionales, membrangebundenes kupferhaltiges Glykoprotein vom -3-Typ, befindet sich in der Membran des Melanosoms18. Tyrosinase wird nur von Melanozytenzellen produziert. Nach seiner Produktion und anschließenden Verarbeitung im endoplasmatischen Retikulum und Golgi wird es zu den Melanosomen transportiert, wo das Pigment Melanin synthetisiert wird. Aus struktureller Sicht sind zwei Kupferionen von drei Histidinresten umgeben, die für die katalytische Aktivität der Tyrosinase verantwortlich sind (Abbildung 2) 19. Das aktive Zentrum hat drei Zustände; Oxy-, Met- und Desoxyformen bei der Bildung der Pigmentierung. Genauer gesagt interagieren zwei Kupferionen im aktiven Zentrum mit Disauerstoff und bilden ein hochreaktives chemisches Zwischenprodukt, das direkt an der Hydroxylierung von Monophenolen zu Diphenolen (Mycophenolataktivität) und an der Oxidation von o-Diphenolen zu o-Chinonen (Diphenolaktivität) beteiligt ist )20,21. Tyrosinase katalysiert auch den Prozess der Neuromelaninproduktion, bei dem durch die Oxidation von Dopamin Dopachinone entstehen. Eine übermäßige Produktion von Dopaquinonen führt jedoch zu neuronalen Schäden und Zelltod. Dies legt nahe, dass Tyrosinase möglicherweise eine wichtige Rolle bei der Neuromelaninbildung im menschlichen Gehirn spielt und für die Neurodegeneration im Zusammenhang mit der Parkinson-Krankheit und der Huntington-Krankheit verantwortlich ist22–26. Tyrosinase wurde auch mit der Bräunung von Gemüse und Obst während des Nachernte- und Handhabungsprozesses in Verbindung gebracht, was zu einem schnellen Abbau führte27–29. Der Einsatz von Tyrosinase wurde im Häutungsprozess von Insekten weiter ausgeweitet30. Daher ist die Regulierung der Melaninsynthese durch Hemmung des Tyrosinase-Enzyms eine wichtige Motivation für Forscher im Zusammenhang mit der Prävention von Hyperpigmentierung.
Tyrosinase-Hemmer
Da Tyrosinase ein entscheidendes Enzym bei der Melaninsynthese durch Melanogenese ist, wird sie zum prominentesten und erfolgreichsten Ziel für Melanogenese-Inhibitoren, die die katalytische Aktivität der Tyrosinase direkt hemmen. Die meisten im Handel erhältlichen Kosmetika oder Hautaufheller sind Tyrosinasehemmer. Die Tatsache, dass die Inhibitoren auf Tyrosinase abzielen, kann die Melanogenese in Zellen gezielt und ohne Nebenwirkungen hemmen, da Tyrosinase ausschließlich von Melanozyten produziert wird. Viele Tyrosinaseinhibitoren wie Hydrochinon (HQ)31–34, Arbutin, Kojisäure35–37, Azelainsäure38,39, L-Ascorbinsäure40–42, Ellagsäure43–45, Tranexamsäure46–48 wurden als Hautaufheller verwendet. mit gewissen Nachteilen (Abbildung 3).

HQ ist potenziell mutagen für Säugetierzellen und wird mit mehreren Nebenwirkungen in Verbindung gebracht, darunter Kontaktdermatitis, Reizung, vorübergehendes Erythem, Brennen, Kribbeln, Leukodermie, kastanienbraune Flecken auf den Nägeln, Hypochromie und Ochronose49–52. Arbutin, ein Prodrug von Hydrochinon, ist ein Naturprodukt und reduziert oder hemmt die Melaninsynthese durch Hemmung der Tyrosinase. Natürliche Formen von Arbutin sind jedoch chemisch instabil und können Hydrochinon freisetzen, das zu Benzol-Metaboliten abgebaut wird, was möglicherweise toxisch für das Knochenmark ist53. Die Verwendung von Kojisäure in Kosmetika ist aufgrund ihrer Karzinogenität und ihrer Instabilität während der Lagerung begrenzt54. L-Ascorbinsäure ist hitzeempfindlich und wird leicht abgebaut 55. Ellagsäure ist unlöslich und daher schlecht bioverfügbar56, und für Tranexamsäure bleibt der melanogene Weg ungeklärt 47. Daher besteht ein großer Bedarf an der Entwicklung neuer Tyrosinase-Inhibitoren mit medikamentöser Wirkung. wie Eigenschaften.


Pilz-Tyrosinase-Hemmer
Chalkone und Flavanon-Inhibitoren
In einer anderen Studie wurden die aus Morus australis isolierten Chalkone 2a–2d auf ihre Hemmwirkung auf Pilztyrosinase unter Verwendung von L-Tyrosin als Substrat 58 untersucht. Die Ergebnisse zeigten, dass alle vier Chalkonderivate im Vergleich zur Standardverbindung äußerst wirksame Hemmstoffe für Tyrosinase waren Arbutin (Abbildung 5(a), 2a–2d). Insbesondere Verbindung 2a zeigte im Vergleich zu Arbutin eine 700-fach starke Hemmung. Die Analyse der Struktur-Aktivitäts-Beziehung (SAR) zeigte, dass die Resorcin-Konstruktion sowohl am Ring A als auch am Ring B der Grund für die starke Tyrosinase-Hemmung sein könnte. Darüber hinaus spielt die Substitution an den 30 Positionen von Ring A eine wichtige Rolle bei der Steigerung der Hemmwirkung. Beispielsweise verringerte der sterisch anspruchsvolle Substituent am Ring A von 2c die Wirksamkeit im Vergleich zum unsubstituierten 2a, was auf die Chelatbildungsfähigkeit gegenüber den Kupferionen zurückzuführen ist. Interessanterweise zeigte Verbindung 2d eine stärkere inhibitorische Aktivität als 2a und 2c, was darauf hindeutet, dass die 4--Hydroxy--1-pentengruppe an der 30 --Position von 2d für die Verstärkung verantwortlich ist. Darüber hinaus wurden die Auswirkungen von Chalkonen auf die Melaninsynthese in melaninproduzierenden B16-Mäuse-Melanomzellen getestet, und die Verbindungen 2a, 2b und 2d wurden stark gehemmt und zeigten nur eine geringe oder keine Zytotoxizität.
Kürzlich berichteten Radhakrishnan et al. über eine Bibliothek von Aza-Chalkonen und59 es wurde die hemmende Wirkung auf Pilztyrosinase unter Verwendung von L-DOPA als Substrat untersucht. Unter den in der Studie untersuchten Verbindungen erwiesen sich zwei Verbindungen 3a und 3b, Kongenere (Carbonylreduktion) der Pyridylazachalkone, als wirksamere Enzyminhibitoren als Kojisäure (IC50¼27,30 lM) (Abbildung 5(a), 3a–3b). ). Darüber hinaus ergab die kinetische Analyse, dass sowohl 3a als auch 3b kompetitive Inhibitoren mit Ki-Werten von 2,62 bzw. 8,10 μM waren. Die Struktur-Funktions-Analyse zeigte, dass das Stickstoffatom im Pyridingerüst der Inhibitoren mit den im aktiven Zentrum der Tyrosinase vorhandenen Kupferionen komplex sein könnte. Dieselbe Forschungsgruppe hat über eine weitere Chalkonreihe mit Oximfunktionalität als Inhibitor der Tyrosinase- und Melaninbildung in Melanom-B16-Zellen berichtet.60 Zwei der Verbindungen (4a: IC50¼4,77 lM und 4b: IC5057,89 lM) zeigten eine starke Tyrosinase-Inhibition Aktivitäten (Abbildung 5(a), 4a–4b) als die Kojisäure (IC50522,25 lM). Kinetische Studien ergaben kompetitive Inhibitoren mit Ki-Werten von 5,25 und 8,33 µM. In durch a-Melanozyten-stimulierendes Hormon (a-MSH) induzierten B16-Melanomzellen hemmten diese beiden Verbindungen 4a und 4b die Melaninbildung und Tyrosinase ohne Zytotoxizität. Im Hinblick auf die SAR-Analyse wurde festgestellt, dass das Vorhandensein von ortho-Methoxy mit para-Nitro-Substituenten (Ring B) für die starke Tyrosinase-Hemmung verantwortlich war (4a). Darüber hinaus zeigte ein elektronenschiebender para-Dimethylaminoring (Ring B) die zweitstärkste Hemmung (4b).
In einer anderen Studie wurde über eine neuartige Reihe von 2,3-dihydro-1H-inden-1-one-chalkonähnlichen Derivaten berichtet.61 Zwei davon, 5a und 5b, wurden als wirksam identifiziert Inhibitoren der Diphenolaseaktivität von Tyrosinase mit IC50-Werten von 12,3 und 8,2 lM (Abbildung 5(a)). Bei weiteren Untersuchungen des Mechanismus wurde festgestellt, dass beide Inhibitoren 5a und 5b reversibel und kompetitiv sind.

Wang et al. isolierte Dihydrochalkone (Abbildung 5(a), 6a–6c) und Flavanone (Abbildung 5(b), 7a–7c) aus Flemingia philippinensis und untersuchten ihre inhibitorischen Aktivitäten auf Tyrosinase62. Die Ergebnisse zeigten, dass sie die Mycophenolat- (IC50=1,01 bis 18,4 µM) und Diphenol-Wirkung (IC50=5,22 bis 84,1 µM) der Tyrosinase hemmen. Insbesondere Dihydrochalcon (6c) hemmte wirksam sowohl die Mycophenolat- als auch die Diphenolaktivitäten der Tyrosinase mit IC50-Werten von 1,28 bzw. 5,22 µM. Die SAR-Analyse ist sehr interessant, da das Pharmakophor nicht mit der Tyrosinase-Hemmung verbunden ist und ihm das a,b-ungesättigte Ketonmotiv fehlt, das in den meisten Inhibitoren vorhanden ist. Im Fall von Flavanonen waren Verbindungen mit der Resorcingruppe (7a) kompetitiv und hemmten Mycophenolat (IC50=1,79 lM) und Diphenole (IC50=7,48 lM) der Tyrosinase signifikant.
Bei der Suche nach neuen Tyrosinase-Hemmern wurde festgestellt, dass die Extrakte von Camylotropis hirtella eine Tyrosinase-Hemmung zeigen63. Nach der erfolgreichen Reinigung und Isolierung von vierzehn Verbindungen zeigten vier Verbindungen (Abbildung 5(b), 8a–8d) starke inhibitorische Aktivitäten gegen Tyrosinase. Als wirksamste Verbindung erwies sich Neorauflavan 8c mit IC50-Werten von 30 und 500 nM gegen die Monophenolase- und Diphenolase-Aktivität von Tyrosinase. Darüber hinaus war 8c im Vergleich zu Kojisäure (13,2 lM) 400-fach wirksamer gegen die Mycophenolataktivität von Tyrosinase. Die zweitstärkste Verbindung war geranyliertes Isoflavon 8a, das Mycophenolat und Diphenole mit IC50-Werten von 2,9 bzw. 128,2 μM inhibierte und als kompetitiver und reversibler Inhibitor identifiziert wurde. Darüber hinaus reduzierten die Verbindungen 8a und 8c effizient den Melaningehalt in a-MHS-induzierten B16-Melanomzellen, ohne die Lebensfähigkeit der Zellen zu beeinflussen. Aus struktureller Sicht verbessert die Reduktion der Geranylseitenkette die Tyrosinase-Hemmaktivität.


Resveratrol-Analoga
Resveratrol (3,5,40 -Trihydroxy-trans-Stilben, 9), ein in der Natur weit verbreitetes Stilbenoid, beispielsweise in Weintrauben, zeigte eine hemmende Wirkung gegen Pilztyrosinase durch den Mechanismus der Kcat-Hemmung (Suizidsubstrat)64. Bei einer In-vitro-Analyse in a-MSH-stimulierten B16-Mäuse-Melanomzellen hemmte Resveratrol die zelluläre Melaninproduktion durch Unterdrückung von Melanogenese-bezogenen Proteinen wie Tyrosinase, TRP-1, TRP-2 und Mikrophthalmie-assoziierter Transkription Faktor (MITF)-Expression65 ohne jegliche Zytotoxizität bis zu 200 lM.64 Die hemmende Wirkung von Resveratrol wurde in einem In-vivo-Modell mit UVB-bestrahlten bräunlichen Meerschweinchen bestätigt. In dieser Studie verringerte die Behandlung mit Resveratrol mit UVB-bestrahlter Rückenhaut von Meerschweinchen die Hyperpigmentierung optisch.
Kürzlich wurde über eine Reihe von Azo-Resveratrol (13a–13e und 13 g) und Azo-Oxyresveratrol (13f) berichtet (Abbildung 6) 69. Unter diesen Verbindungen zeigten 13a und 13b eine hohe Tyrosinase-Hemmaktivität von 56,25 Prozent bzw. 72,75 Prozent 50 lM bzw. 69. Die 4-Hydroxyphenyl-Einheit erwies sich als wesentlich für eine stärkere Hemmung und 3,5-Dihydroxyphenyl- oder 3,{20}}Dimethoxyphenyl-Derivate zeigten eine bessere Tyrosinase-Hemmung als 2,5-Dihydroxyphenyl- oder 3,{20}}Dimethoxyphenyl-Derivate. 5-Dimethoxyphenyl-Derivate. Insbesondere die Einführung einer Hydroxyl- oder Methoxygruppe in die 4-Hydroxyphenyl-Einheit verringerte oder reduzierte die Tyrosinasehemmung von Pilzen erheblich. Unter den synthetisierten Azoverbindungen war Azo-Resveratrol (13b) mit einem IC50-Wert von 36,28 µM die stärkste Hemmung der Pilztyrosinase. Die Ergebnisse deuten darauf hin, dass Azo-Resveratrol mit einem hohen Log-p-Wert Resveratrol bei der Entwicklung von Aufhellern und Arzneimitteln zur Behandlung von Hyperpigmentierung überlegen sein könnte.
Cumarin-Derivate
Cumarine sind eine große Familie von Benzopyronverbindungen natürlichen und synthetischen Ursprungs mit unterschiedlichen pharmakologischen Aktivitäten70. In jüngsten Studien wurde nachgewiesen, dass nur wenige Cumarine die Tyrosinase von Pilzen hemmen, zu denen Aesculetin und Umbelliferon mit stärkerer Tyrosinase-Hemmwirkung gehören71,72. In einer kontinuierlichen Anstrengung haben Matos et al. eine Reihe von Cumarin-Resveratrol-Hybridverbindungen nachgewiesen, nämlich 3-Phenylcumarine mit Hydroxyl- oder Alkoxy- und Bromsubstituenten an verschiedenen Positionen im Gerüst73 (Abbildung 7). In der Serie wurde eine Verbindung mit einem Bromatom und zwei Hydroxylgruppen in der 3-Phenylcumarin-Einheit (14) mit einem IC50-Wert von 215 µM als bester Inhibitor identifiziert. Diese Verbindung ist ein nichtkompetitiver Tyrosinase-Inhibitor mit einem Ki-Wert von 0,189 mM.

In einer anderen Studie wurde über eine Reihe von Umbelliferon-Analoga wegen ihrer hemmenden Wirkung auf die Pilztyrosinase berichtet74. Insbesondere die Verbindungen 15a und 15b, die über ein 3,4--Dihydroxy- und ein 3,4,5--Dihydroxy-Phenylgerüst verfügen, zeigten stärkere Hemmwirkungen gegen die Aktivität der Pilztyrosinase (Abbildung 7). Asthana et al. demonstrierten eine Reihe von Hydroxycumarinen (16a–16d) 75 (Abbildung 7). Die SAR-Studien legten nahe, dass die Position des Hydroxylsubstituenten am Cumarin eine Rolle bei der enzymatischen Hemmung spielt; Die aromatisch hydroxylierten Verbindungen 6-Hydroxycumarin (16c) und 7-Hydroxycumarin (16d) erwiesen sich als schwache Substrate des Enzyms. Insbesondere 7-Hydroxycumarin hemmte die Dopachromkonzentration im Bereich von 0.3 - 0.9 mM stark. Bei einer maximalen 7-Hydroxycumarin-Konzentration erreichte die Hemmung 88 Prozent. Die Autoren fanden heraus, dass das Phänomen auf die spezifische Hemmung der L-Tyrosin-Umwandlung zurückzuführen ist. Andererseits waren die Verbindungen mit hydroxyliertem Pyron, 3-Hydroxycumarin (16a) und 4-Hydroxycumarin (16b), keine Substrate der Tyrosinase. Es wurde festgestellt, dass 3-Hydroxycumarin (16a) Tyrosinase hemmt, nicht jedoch die Verbindung mit 4-Hydroxycumarin (16b), was darauf hinweist, dass der Pyronring nicht durch Tyrosinase hydroxyliert werden kann.
Kürzlich wurde eine Reihe von Phosphonsäurediamiden auf ihre Tyrosinase-Hemmwirkung untersucht76. Die Ergebnisse zeigten, dass der an C-5 gebundene Substituent und die Stereochemie der beiden Stereozentren (C-5 und Phosphoratom) für die Tyrosinase-Hemmung wichtig sind (17a–17d). Diastereomere mit unsubstituiertem Phenyl zeigten keine inhibitorische Aktivität gegen Tyrosinase (17a und 17a0). Im Gegensatz dazu zeigten Verbindungen mit einem substituierten Phenyl verschiedene Auswirkungen auf die Tyrosinaseaktivität. Beispielsweise hemmte Verbindung 17b mit p-Chlorphenyl (80,65 Prozent Tyrosinasehemmung) die Tyrosinase mäßig, ihr Diastereomer 17b0 16 ,5 Prozent Tyrosinasehemmung) war inaktiv. In einem anderen Fall zeigten 17c (58,54 Prozent Tyrosinase-Hemmung) und 17c0 mit p-Methylphenyl (61,80 Prozent Tyrosinase-Hemmung) eine gute Tyrosinase-Hemmung. Verbindung 17d, bestehend aus einem 2-Pyridinyl-Fragment (97,40 Prozent Tyrosinase-Hemmung), erwies sich in der obigen Studie als der wirksamste Tyrosinase-Inhibitor.

Inhibitoren mit b-Phenyl-a,b-ungesättigter Carbonylfunktion
Kürzlich wurde berichtet, dass Benzylidenhydantoin 18a, Benzylidenpyrrolidindion 18b und Benzylidenthiazolidin-2,4-dion 18c (Abbildung 8(a)) potenzielle Tyrosinaseinhibitoren sind und dass die Verbindungen in vivo untersucht wurden haben sich als wirksame Hautaufheller erwiesen77–80. Sie zeigten stärkere Hemmwirkungen als Kojisäure und Arbutin. Die Verbindung 18a wurde durch Nachahmung der chemischen Struktur der L-Tyrosin- und L-DOPA-Tyrosinase-Substrate entworfen. Die SAR-Studien ergaben, dass das Amid NH an der 1--Position von Hydantoin 18a Wasserstoffbrückenbindungen mit Aminosäuren am aktiven Zentrum der Tyrosinase bilden kann. Darüber hinaus ahmt die Imidogruppe von 18a die Carbonsäuregruppe der Substrate nach. Vor diesem Hintergrund haben Kim et al. haben kürzlich eine Reihe von 5-(Hydroxyl- oder Alkoxy-substituierten Benzyliden)thiohydantoin-Analoga mit b-Phenyl-a,b-ungesättigten Carbonylgerüsten synthetisiert und untersucht.81 Unter ihnen zeigten drei Verbindungen, 19a–19c, hohe inhibitorische Aktivitäten als Kojisäure oder Resveratrol (Abbildung 8(a)). Insbesondere 2,4-Dihydroxybenzyliden-2-thiohydantoin 19c (IC50¼1,07 lM) erwies sich in dieser Studie als der beste Inhibitor. Darüber hinaus hemmte 19c die zelluläre Tyrosinaseaktivität in B16-Zellen ohne nennenswerte Zytotoxizität.
In einer Fortsetzung wurden (E)-2-Benzoyl-3-(substituierte Phenyl)acrylonitrile (BPA-Analoga) mit einem linearen b-Phenyl-a,b-ungesättigten Carbonylgerüst synthetisiert und als potenzielle Tyrosinase-Inhibitoren bewertet82. Unter ihnen hemmten drei Verbindungen 20a–20c wirksam die Pilztyrosinaseaktivität (Abbildung 8(a)). Insbesondere Verbindung 20c unterdrückte die Melaninbiosynthese signifikant und hemmte die intrazelluläre Tyrosinaseaktivität in B16-Zellen, ohne die Lebensfähigkeit der Zellen zu beeinflussen. Die SAR-Analyse ergab, dass alle Wirkstoffe eine 4--Hydroxygruppe am Phenylring haben und dass die Substitution von Br an der 3--Position oder an der 3- und 5--Position mit einer starken Tyrosinase verbunden ist hemmende Wirkung.
Kürzlich untersuchte dieselbe Forschungsgruppe weiterhin die SAR von 3-(substituierten Phenyl)acrylonitrilen. Dementsprechend zeigte eine Reihe von (E)-2-Cyano-3-(substituierten Phenyl)acrylamid-Derivaten mit einem linearen b-Phenyl-a,b-ungesättigten Carbonylgerüst eine hemmende Wirkung gegen Pilztyrosinase83. Unter den Verbindungen übten 21a und 21b eine hemmende Wirkung gegen Pilztyrosinase aus (Abbildung 8(a)). Insbesondere Verbindung 21a zeigte eine hervorragende Hemmwirkung. In B16-Zellen unterdrückte 21a die Tyrosinaseaktivität dosisabhängig signifikant, ohne dass es einen Einfluss auf die zytotoxische Wirkung hatte. Aus struktureller Sicht spielt ein „lineares“ b-Phenyl-a,b-ungesättigtes Carbonylgerüst eine wesentliche Rolle bei der Entfaltung einer anti-melanogenen Wirkung durch die direkte Hemmung des Tyrosinase-Enzyms.
0
Es ist seit langem bekannt, dass Zimtaldehyd die L-DOPA-Oxidation durch Pilztyrosinase hemmen kann84. Kürzlich haben Cui et al. berichteten über eine Reihe a-substituierter Derivate von Zimtaldehyd-Derivaten85. Die SAR-Studien zeigten, dass die Verbindungen a-Bromzimtaldehyd 22a, a-Chlorzimtaldehyd 22b und a-Methylzimtaldehyd 22c sowohl die Mycophenolat- als auch die Diphenolaseaktivität auf Tyrosinase reduzierten (Abbildung 8(a)). Die IC50-Werte von 22a–22c betrugen 0.075, {{20}}.140 und 0,440 mM für Mycophenolat und 0,049, 0,110 bzw. 0,450 mM auf Diphenolen. Darüber hinaus wurde vermutet, dass das a-substituierte Zimtaldehyd-Derivat im Vergleich zu Zimtaldehyd wirksamer sei.
In letzter Zeit haben Thio/Barbiturate auf dem Gebiet der Tyrosinase-Inhibitoren Aufmerksamkeit erregt86, aufgrund ihrer attraktiven Struktureinheit aus b-Phenyl-a,b-ungesättigtem Carbonylgerüst, die für die Tyrosinase-Inhibitorfunktion verantwortlich ist. In der Literatur gab es nur wenige 5-Benzyliden(thio)barbiturate mit Hydroxylsubstituenten an der 4--Position des Phenylrings, die hervorragende Hemmwirkungen aufwiesen, zum Beispiel hemmten 23a und 23b mit IC50-Werten von 13,98 und 14,49 µM. bzw.87 (Abbildung 8(b)). Inspiriert durch diese Arbeit untersuchten Chen et al. kürzlich den SAR von Thio-/Barbituraten und betonten dabei die Position und die Anzahl der Hydroxylsubstituenten für den Einfluss der Tyrosinase-Hemmaktivität. Dementsprechend wurde über eine Reihe von Hydroxy- oder Methoxy-substituierten 5-Benzyliden(thio)barbituraten wegen ihrer hemmenden Wirkung auf die Diphenolaktivität der Pilztyrosinase88 berichtet. Die Ergebnisse zeigen, dass Verbindungen (23c–23 g) im Vergleich zu Kojisäure (IC50=18.25 lM) starke Tyrosinase-hemmende Aktivitäten hatten. Insbesondere eine Verbindung mit 3,4-Dihydroxysubstituenten 23e wurde mit einem IC50-Wert von 1,52 lM als bester Inhibitor identifiziert. Die SAR-Studien ergaben, dass Barbiturate wirksamer waren als Thiobarbiturate und 3,{30}}Dihydroxylgruppen am Phenylring die Wirksamkeit verbesserten. Darüber hinaus wurde festgestellt, dass diese Inhibitoren vom reversiblen Typ sind.
Für weitere Informationen: david.deng@wecistanche.com WhatApp:86 13632399501






