Die Urinsedimentbefunde waren bei Patienten mit COVID-19-assoziierten Nierenschäden milder als bei Patienten mit nicht-COVID-19-assoziierten Nierenschäden
Dec 13, 2023
Abstrakt
Hintergrund:Akute Nierenschädigungist eine wichtige Komplikation vonCoronavirus Krankheit 2019(COVID-19). Sowohl COVID-19-spezifische Mechanismen, wie zSchädigung des Nierenparenchymsvondirekte Infektion, Undunspezifische Mechanismen, so wie diePränierenschädigungsfaktoren, wurden vorgeschlagenan COVID-19-assoziierten Nierenschäden beteiligt. In dieser Studie wollten wir das klärenMerkmale von COVID-19-damit verbundenenNierenverletzungen,Der Schwerpunkt liegt hauptsächlich auf Urinsedimentbefunden. Methoden: Wir verglichen die Urinsedimentbefunde und ihre Assoziationen mit Nierenfunktionen oder klinischen Harnparametern zwischen Probanden mitCOVID-19und Themen ohneCOVID-19 mit akuten Nierenschäden. Ergebnisse: Wir fanden heraus, dass die Anzahl der Urinsedimentpartikel und die Spiegel von N-Acetyl- -D-Glucosaminidase, 1-Mikroglobulin, fettsäurebindendem Protein vom Lebertyp und Neutrophilen-Gelatinase-assoziiertem Lipocalin miteinander verbunden waren mit der Schwere von COVID-19. Darüber hinaus beobachteten wir, dass die Anzahl der körnigen Zylinder, Epithelzylinder, Wachszylinder und die Konzentration chemischer Marker im Urin bei den Probanden mit COVID-19 niedriger war als bei Probanden ohne COVID-19 mit akuten Nierenschäden Die Probanden wurden nach ihrer Nierenfunktion klassifiziert. Schlussfolgerungen: Diese Ergebnisse legen nahe, dass prärenale Verletzungsfaktoren maßgeblich an der Pathogenese von beteiligt sein könntenCOVID-19-assoziierte Nierenschädenim Vergleich zu nicht-COVID-19-assoziiertenNierenverletzungeninfolge einer Operation oder einer Sepsis entstehen.

WIE LANGE DAUERT ES, BIS CISTANCHE WIRKT?
Einführung
Coronavirus-Krankheit 2019 (COVID-19), die verursacht wird durchschweres akutes respiratorisches SyndromDas Coronavirus 2 (SARS-CoV-2) hat sich rasch zu einer globalen Pandemie entwickelt. Personen mit COVID-19 entwickeln häufig eine Lungenentzündung, die zu hypoxämischem Atemversagen führen kann. Darüber hinaus können verschiedene zusätzliche Komplikationen auftreten. Darunter können Patienten mit COVID-19 an Nierenkomplikationen leiden, insbesondere an einer akuten Nierenschädigung (AKI). AKI ist eine häufige Komplikation bei Patienten mit kritisch schwerem COVID-19, und ein Metaanalysebericht hat gezeigt, dass die durchschnittliche Inzidenz von AKI bei allen Probanden mit COVID-19 11 % und bei kritisch Kranken 23 % betrug Patienten (Gabarre et al., 2020). Da Patienten mit COVID-19 und einer Nierenerkrankung Berichten zufolge ein höheres Risiko haben, im Krankenhaus zu sterben (Cheng et al., 2020), könnte die frühzeitige Diagnose von Nierenverletzungen die Prognose verbessern.

Derzeit sind die detaillierten Mechanismen von COVID-19-assoziierten Nierenschäden nicht geklärt; obwohl mehrere Mechanismen vorgeschlagen wurden. Angiotensin-Converting-Enzym 2 (ACE2) und Transmembran-Serinprotease 2 (TMPRSS2), die Schlüsselproteine beim Eintritt von SARS-CoV-2 in menschliche Zellen sind (Hoffmann et al., 2020), werden in Podozyten gut exprimiert und die proximalen Tubuli in der Niere (Pan et al., 2020), und SARS-CoV- 2 kann die Niere direkt infizieren und schädigen (Yeung et al., 2016). Eine aktuelle Studie hat gezeigt, dass eine hohe SARS-CoV-2-Viruslast mit Nierenkomplikationen und der Schwere von COVID-19 verbunden ist (Caceres et al., 2021). Komplikationen wie Thrombosen und Endotheline werden auch häufig bei Patienten mit COVID-19 beobachtet (Li et al., 2020 Shimura et al. 2021; Xiong et al., 2020;); Theoretisch könnten solche Komplikationen zu einer Nierenfunktionsstörung führen. Darüber hinaus wurden auch andere Mechanismen vorgeschlagen, die nicht spezifisch für COVID-19 sind. Mechanische Beatmung aufgrund von akutem Lungenversagen (Vieillard-Baron et al., 2007), Rechtsherzinsuffizienz aufgrund von Myokardinfarkt (Bradley et al., 2020, Edler et al., 2020) oder Myokarditis (Bradley et al., 2020) oder Rhabdomyolyse (Gamboa et al., 1979), die zu AKI führen kann (Legrand et al., 2013), könnten ebenfalls an COVID-bedingten Nierenschäden beteiligt sein. Da sowohl COVID{30}}spezifische als auch unspezifische Mechanismen möglich sind, wird der Vergleich der Urinparameter zwischen Patienten mit durch COVID-19 verursachten Nierenschäden und Patienten mit durch andere Krankheiten verursachten Nierenschäden wichtig für das Verständnis der charakteristischen pathophysiologischen Zustände COVID-19-assoziierte Nierenschäden. Bisher haben postmortale pathologische Untersuchungen der Nieren ergeben, dass der histologische Grad der akuten tubulären Schädigung weniger schwerwiegend ist als der auf der Grundlage des Kreatinin-Anstiegs vorhergesagte Wert (Santoriello et al., 2020), was darauf hindeutet, dass COVID-19-mit Nierenschäden verbunden ist könnten im Vergleich zu nicht-COVID-19-assoziierten Nierenschäden einzigartige Merkmale aufweisen.
Urinanalysen und Urinsedimentuntersuchungen sind die ältesten und am häufigsten durchgeführten Tests zur Beurteilung des pathophysiologischen Zustands des Nieren-/Harnröhrensystems. Urinanalysebefunde wie Proteinurie, Hämaturie und Leukozyturie werden Berichten zufolge mit COVID-19-assoziierten Nierenschäden und der Schwere von COVID-19 in Verbindung gebracht (Allemailem et al., 2021 Chan et al., 2020; Liu et al ., 2020; Ouahmi et al., 2021; Pei et al., 2020; Yang et al., 2020;) und mehrere chemische Biomarker im Urin wie N-Acetyl- -D-Glucosaminidase (NAG), { {11}}Mikroglobulin (1-MG) und Neutrophilen-Gelatinase-assoziiertes Lipocalin (NGAL) sollen mit AKI bei hospitalisierten Patienten mit COVID in Zusammenhang stehen-19 (Fukao et al., 2021 Huart et al., 2021; Husain-Syed et al., 2020; Luther et al., 2021;). Allerdings wurden die Eigenschaften der Urinsedimentbefunde im Zusammenhang mit COVID-19 noch nicht ausreichend untersucht. Bisher wurden nur ein Fallbericht und eine Studie über Urinsedimentbefunde bei Patienten mit COVID-19 berichtet und auf einen möglichen Zusammenhang zwischen körnigen Zylindern und der Schwere von COVID-19 hingewiesen (Allemailem et al., 2021). , Fujimaru et al., 2020). Im Allgemeinen können Urinsedimentbefunde eine nicht-invasive Abschätzung des Schweregrads und/oder der Ursache einer Nierenschädigung ermöglichen. Beispielsweise ist das Vorhandensein von renalen tubulären Epithelzellen (RTEs) und körnigen Zylindern nützlich für die Unterscheidung zwischen Nierenschädigung und prärenaler Schädigung (Perazella et al., 2008), und wachsartige Zylinder werden Berichten zufolge mit Nierenversagen in Verbindung gebracht (Spinelli et al., 2013).
Vor diesem Hintergrund wird davon ausgegangen, dass Urinsedimentbefunde für die indirekte Beurteilung des Ausmaßes von Nierenschäden bei Personen mit COVID-19 nützlich sein werden. Daher untersuchten wir in der vorliegenden Studie den Zusammenhang zwischen klinischen Serum- oder Urinparametern und Urinsedimentbefunden bei Probanden mit COVID-19 und Probanden ohne COVID-19, um die Eigenschaften von Urinsedimenttests aufzuklären und abzuschätzen die zugrunde liegenden Mechanismen für COVID-19-assoziierte Nierenschäden.

Materialen und Methoden
Fächer
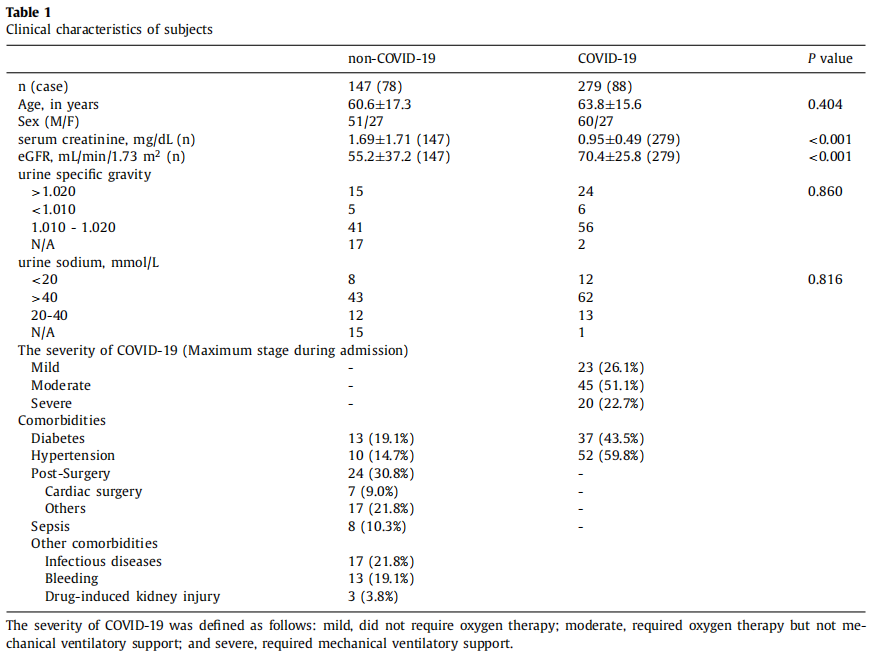
Resturinproben wurden von 88 Probanden mit COVID-19 (insgesamt: 279 Proben; Durchschnitt: 3 Proben pro Patient; Bereich: 1–16 Proben) gesammelt, die mittels RT-PCR diagnostiziert wurden. Der Schweregrad von COVID-19 wurde wie folgt definiert: mild, erforderte keine Sauerstofftherapie; mäßige, erforderliche Sauerstofftherapie, jedoch keine mechanische Beatmungsunterstützung; und schwere, erforderliche mechanische Beatmungsunterstützung. Wir haben auch Urinproben von 78 Probanden (insgesamt: 147 Proben; Durchschnitt: 2 Proben pro Patient; Bereich: 1–9 Proben) mit akuten Nierenschäden, die durch Nicht-COVID-Faktoren verursacht wurden und die in einen Notfall eingeliefert wurden, gesammelt oder Intensivstation (ICU). Restharnproben wurden nach routinemäßigen Labortests gesammelt und der Überstand bei -80 Grad gelagert. Die Eigenschaften der Probanden sind in Tabelle 1 beschrieben.
Die vorliegende Studie wurde in Übereinstimmung mit den ethischen Richtlinien der Deklaration von Helsinki durchgeführt. Von einigen Patienten wurde eine schriftliche Einverständniserklärung zur Probenanalyse eingeholt. Für die übrigen Teilnehmer, von denen keine schriftliche Einverständniserklärung eingeholt werden konnte, weil sie aus dem Krankenhaus entlassen oder verlegt wurden, wurde die Einverständniserklärung in Form eines Opt-outs auf einer Website wie folgt eingeholt. Patienten wurden auf der Website über die Studie informiert, diejenigen, die nicht an der Studie teilnehmen wollten, wurden ausgeschlossen. Das Studiendesign wurde von der Ethikkommission des Medizinischen Forschungszentrums der Universität Tokio genehmigt, die auf die Notwendigkeit einer schriftlichen Einverständniserklärung verzichtete, wenn eine schriftliche Einverständniserklärung nicht eingeholt werden konnte, weil archivierte Proben verwendet wurden und alle Daten, die in dieser retrospektiven Studie verwendet wurden, bereits verwendet worden waren aus Krankenakten abgerufen (3683, 3333-101, 3333-140 und 2020206NI).

Urinanalyse
Die Urinsedimentuntersuchung wurde mittels manueller Mikroskopie durchgeführt und entsprach den Vorgaben des japanischen Komitees für klinische Laborstandards (JCCLS). RTEs wurden pro Hochleistungssichtfeld (/HPF) gezählt und Harnzylinder wurden in hyaline Zylinder (HyaC), körnige Zylinder (GraC), epitheliale Zylinder (RTEC) und wachsartige Zylinder (WaxC) eingeteilt und ihre Anzahl wurde gezählt pro ganzem Feld (/WF). Für die Messung klinischer Urinmarker verwendeten wir die folgenden Reagenzien: Urinkreatinin (uCr) wurde mithilfe eines Enzymtests gemessen (L-Typ Wako CRE • M; FUJIFILM Wako Pure Chemical, Osaka, Japan); Gesamtprotein (TP) (Mikro-TP-Test Wako; FUJIFILM Wako) wurde mit der Pyrogallolrot-Methode gemessen; Mikroalbumin (μAlb) (Auto Wako Mikroalbumin; FU JIFILM Wako) wurde unter Verwendung eines turbidimetrischen Immunoassays (TIA) gemessen; NAG (Ltype Wako NAG; Wako, Japan) wurde unter Verwendung eines Enzymassays gemessen; 1-MG (LZtest 'Eiken' 1-M; Eiken Chemical, Japan) wurde mittels Latex-Agglutinationsturbidimetrie gemessen; Das fettsäurebindende Protein vom Lebertyp (L-FABP) (NORUDIA L-FABP; SEK ISUI MEDICAL, Japan) wurde mittels Latexagglutinationsturbidimetrie gemessen; und NGAL (U-NGAL Abbott; Abbott, Japan) wurde unter Verwendung eines Chemilumineszenz-Immunoassays (CLIA) gemessen. Das spezifische Gewicht des Urins (SG) wurde mit einem automatischen chemischen Urinanalysator US-3500 (Eiken Chemical, Japan) gemessen und das Natrium im Urin wurde mit der Elektrodenmethode gemessen. Die Beteiligung der prärenalen Schädigung wurde bestätigt, wenn der SG 1,020 oder höher oder der Natriumgehalt im Urin 20 mmol/L oder weniger betrug, wohingegen die Beteiligung einer Nierenschädigung geschätzt wurde, wenn der SG 1,010 oder niedriger oder der Natriumgehalt im Urin 40 mmol/L betrug. L oder höher.
statistische Analyse
Die Datenanalyse wurde mit SPSS (Chicago, IL) durchgeführt. Der Kruskal-Wallis-Test wurde verwendet, um die Anzahl der Urinsedimentpartikel und Urinmarker entsprechend dem Schweregrad der Probanden mit COVID-19 zu vergleichen. Der Chi-Quadrat-Test und der Mann-Whitney-U-Test wurden verwendet, um die Urinmarker und die Anzahl der Urinsedimentpartikel zwischen Probanden mit und ohne COVID-19 zu vergleichen, und der Spearman-Korrelationstest wurde verwendet, um den Zusammenhang zu analysieren zwischen den Urinmarkern und den Urinsedimentpartikeln bei den Probanden. Statistische Signifikanz wurde als P-Wert < 0.05 angesehen.
Unterstützender Service von Wecistanche – dem größten Cistanche-Exporteur in China:
E-Mail:wallence.suen@wecistanche.com
WhatsApp/Tel:+86 15292862950
Weitere Spezifikationen finden Sie im Shop:
https://www.xjcistanche.com/cistanche-shop
ERHALTEN SIE NATÜRLICHEN BIO-CISTANCHE-EXTRAKT MIT 25 % ECHINACOSID UND 9 % ACTEOSID BEI NIERENINFEKTIONEN







