Charakterisierung des Nierenabstoßungsrisikos vor und nach der Transplantation durch Sequenzierung des B-Zell-Immunrepertoires
Mar 16, 2022
Kontakt:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791
Die Untersuchung des Immunrepertoires im Zusammenhang mit Organtransplantationen liefert wichtige Informationen darüber, wie die adaptive Immunität zur Transplantatabstoßung beitragen und diese modulieren kann. Hier charakterisieren wir das periphere Blutimmunrepertoire von Individuen vorher und nachherNiereTransplantation unter Verwendung von B-Zell-Rezeptorsequenzierung in einer klinischen Längsschnittstudie. Personen, die nach der Transplantation eine Abstoßung entwickeln, haben vor der Transplantation ein vielfältigeres Immunrepertoire, was auf eine Prädisposition für ein Abstoßungsrisiko nach der Transplantation hindeutet. Darüber hinaus zeigen Patienten, die eine Abstoßung entwickeln, über einen Zeitraum von 2 Jahren eine spezifische Gruppe von expandierten Klonen, die nach der Abstoßung bestehen bleiben. Während es eine allgemeine Verringerung der peripheren B-Zell-Diversität gibt, wahrscheinlich aufgrund einer erhöhten allgemeinen Immunsuppressions-Exposition in dieser Kohorte, unterstützt der Nachweis der spezifischen Verwendung von IGHV-Genen bei allen abstoßenden Patienten, dass ein gemeinsamer Pool immunogener Antigene die Abstoßung nach der Transplantation vorantreiben kann. Unsere Ergebnisse können klinische Auswirkungen auf die Vorhersage und das klinische Management der Abstoßung von Nierentransplantaten haben.
NiereTransplantation ist die bevorzugte Behandlung von Nierenerkrankungen im Endstadium (ESRD) und chronischNiereErkrankung. Auch wenn es signifikante Verbesserungen bei den Technologien und beim Gewebeabgleich basierend auf Histokompatibilitätstests für Spender-/Empfänger-Human-Leukozyten-Antigene (HLA)1 gegeben hat, ist die Vorhersage des Transplantatergebnisses immer noch ein ungelöstes Problem. Gemessene Gewebefehlpaarungen an anderen kleineren Nicht-HLA-Loci23 können auch zu Alloimmunschäden mit akuter und chronischer Abstoßung führen, was zu schlechten langfristigen Transplantatergebnissen führt4. Darüber hinaus rund 50 Prozent derNiereAllotransplantate ohne größere HLA-Fehlpaarungen gehen dennoch innerhalb von 10 Jahren nach der Transplantation² verloren. Wir haben zuvor die Hypothese aufgestellt, dass Nicht-HLA-Loci die Immunantwort des Empfängers gegen seine beeinflussen könnenNieredonor graft6. More research needs to be done to better understand and predict the recipient's risk of rejection to substantially improve long-term patient and graft outcomes. Nevertheless, the diversity of the immune response to various immunogenic epi-topes is as yet, poorly understood. The role of T cells in organ transplant rejection has been demonstrated, but there is increasing appreciation of the additional role of B cells and antibodies in triggering this process8. In this regard, B-cell receptor sequencing(BCRSeq)is a promising high-throughput technique that allows the sequencing of millions of Immunoglobulin (Ig)regions in parallel to study the immune response. The key feature of B cells is their enormous diversity. Each individual is capable of producing >1013 verschiedene Antikörper0, wodurch sie eine Vielzahl fremder Antigene erkennen können. Menschliche BCRs oder Ig bestehen aus zwei identischen schweren Ketten (I), die von fünf Isotypen gebildet werden: IgM, IgD, IgA, IgE und IgG, und zwei leichten Ketten. Der intakte Antikörper enthält eine variable und eine konstante Domäne. Die Antigenbindung erfolgt in der variablen Domäne, die durch Rekombination eines Satzes von variablen (V), Diversitäts- (D) und verbindenden (J) Gensegmenten erzeugt wird, die das B-Zell-Immunrepertoire bilden, und ihre Diversität konzentriert sich hauptsächlich auf die komplementär bestimmende Region 3 (CDR3). Während des Prozesses der Affinitätsreifung tritt in der variablen Region eine somatische Hypermutation (SHM) auf. Eine starke adaptive Immunantwort hängt von der Expansion von B-Zellklonen und einem als Affinitätsreifung bezeichneten Prozess ab, während dessen somatische Mutationen in die Ig-Genumlagerungen eingeführt werden und B-Zellen mit höherer Affinität für ein bestimmtes Antigen selektiert werden.
Die Untersuchung des Immunrepertoires bei Organtransplantationen ist entscheidend, um zu verstehen, was den Abstoßungsprozess auslöst und aufrechterhält und wie er schließlich den Weg zum Transplantatversagen beschleunigen kann. Mit den Fortschritten der Sequenzierung der nächsten Generation und robusten Computeransätzen können wir die VDJ-Region im Detail untersuchen,12. Bis heute T-Zell-Immunrepertoire-Analyse inNiereEine Transplantation wurde bei einer sehr begrenzten Anzahl von Patienten durchgeführt13-15, und obwohl BCRSeq bei anderen Krankheiten und menschlichen Immunantworten angewendet wurde, wie z. B. Multiple Sdlerosis6, Influenza-Impfstoffl7oder Immunschwächekrankheiten8, gibt es einen Mangel an Studien zur Transplantation Ablehnung. In einemNiereTransplantation, BCRSeq wurde nur im Rahmen der Toleranz durchgeführt, HLA-sensibilisiertNiereTransplantationskandidaten, die sich einer Desensibilisierungstherapie unterziehen20, und B-Zell-Infiltration im Vergleich zur klonalen Expansion im Blut und Transplantat2l. Eine weitere Anwendung von BCRSeq in der Transplantation wurde zuvor in einer kleinen Kohorte von 12 Empfängern von Herztransplantaten veröffentlicht.
In Anbetracht der Bedeutung des humoralen Arms der Immunantwort bei später Transplantatabstoßung und chronischem Transplantatversagen charakterisieren wir das periphere Blut-Immunrepertoire mit BCRSeq in einer prospektiven Längsschnittstudie. Wir finden, dass die Diversität des Immunrepertoires vor der Transplantation bei denjenigen Personen höher ist, die das abstoßenNierewas auch die Expansion bestimmter Klone und IGHV-Gene entlang der 24-monatigen Nachbeobachtung zeigt. Diese Ergebnisse können helfen, das Abstoßungsrisiko vor der Transplantation vorherzusagen, und können klinische Auswirkungen auf den Nachweis bestimmter Antigene haben, die die Abstoßung antreiben.

Cistanche ist gut für die Nierenfunktion
Ergebnisse
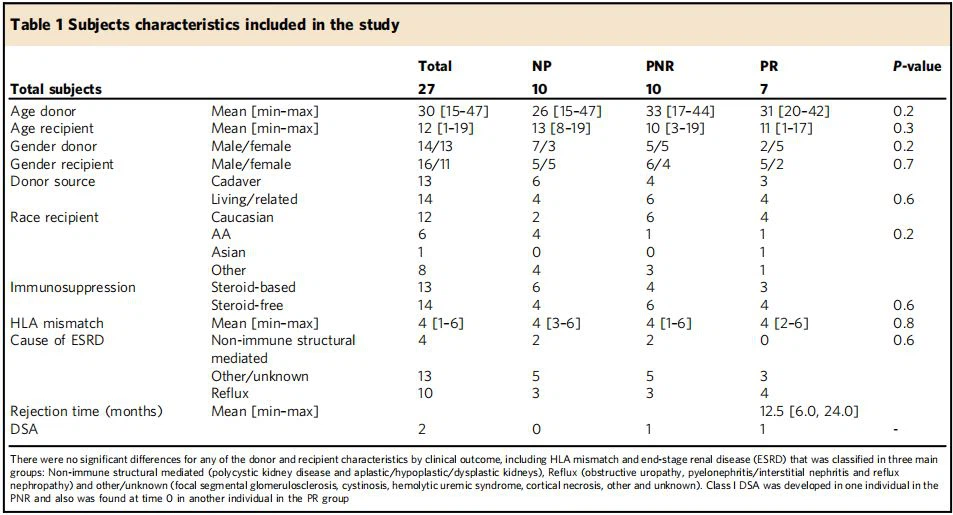
Studienfächer. Wir haben BCRSeq in 83 peripheren Blutproben von 27 einzelnen Patienten durchgeführt und die in Abb. 1 gezeigte analytische Pipeline ausgeführt. In dieser Studie wurden drei klinische Phänotypgruppen berücksichtigt, die durch verblindete zentrale pathologische Ablesungen von seriellen Allotransplantat-Biopsien, bewertet nach den Banff-Kriterien23,24, und dem Chronic Allotransplant Damage Index (CADI)-Score, in dieser Studie berücksichtigt wurden: Non-Progressors (NP; n=10) hatten einen niedrigen nicht inkrementellen CADI-Score ohne akute Abstoßung, Progressoren ohne Abstoßung (PNR;n=10) hatten einen inkrementellen CADI-Score über 2 Jahre ohne Abstoßung und Progressoren mit Abstoßung (PR; n=7) hatten inkrementelle hohe CADI-Scores über 2 Jahre mit Abstoßungsepisoden. Demographie, Ursachen vonNiereTherapieversagen und Anwendung der Immunsuppression sind in Tabelle 1 aufgeführt. Es ist wichtig, einige Merkmale dieser Patienten hervorzuheben. Die Elternstudie, aus der diese Patienten rekrutiert wurden, wies eine insgesamt niedrige Rate (17 Prozent) an biopsiebestätigter akuter Abstoßung auf (mittlere {min, max}=12 {6,24} Monate Abstoßungszeit). Diese Patienten hatten alle ein geringes immunologisches Abstoßungsrisiko (Peak-Panel-reaktiver Antikörper-Sensibilisierungsstatus).<20%), and="" also="" had="" low="" rates="" of="" generation="" of="" donor-specific="" antibody(dsa)and="" only="" two="" of="" the="" rejection="" phenotype="" patients="" included="" in="" the="" analysis="" had="" dsa.="" the="" generation="" of="" dsa="" to="" hla="" and="" mica="" was="" measured="" in="" all="" serial="" sera="" throughout="" the="" study25.="" national="" experience="" with="" similar="" immunosuppressive="" protocols="" in="" similar="" patient="" cohorts="" have="" confirmed="" similar="" good="" clinical="" outcomes="" and="" low="" rejection="">
Sequenzierung des B-Zell-Immunrepertoires. BCRSeq wurde an genomischen DNA(gDNA)-Proben durchgeführt, die aus Blutgerinnseln an 81 Proben von 27 extrahiert wurdenNiereTransplantatempfänger zu drei Zeitpunkten (0, 6, 24 Monate). Die Sequenzierung ergab eine Gesamtzahl von 327.703 Reads (Mittelwert 4045/Probe) nach der Qualitätskontrolle (siehe Methodenabschnitt). Zur Validierung der Ergebnisse und zur weiteren Bewertung jedes Isotyps extrahierten wir zusätzlich RNA aus übereinstimmenden PBMC, die für 55 Proben verfügbar waren, die gleichzeitig mit dem Blutgerinnsel gesammelt wurden, und führten eine komplementäre DNA(cDNA)-Sequenzierung mit größerer Tiefe durch, um 1.773.330 Reads zu erhalten für IgD (Mittelwert 31.667/Probe), 1.708.227 Reads für IgM (Mittelwert 30.504/Probe), 973.444 Reads für IgA (Mittelwert 17.383/Probe), 139.7345 Reads für IgG (Mittelwert 24.953/Probe) und 29,{{27 }} liest für IgE (Mittelwert 5178/Probe) (ergänzende Abb. 1). Bibliotheken für jeden Isotyp wurden separat amplifiziert und dann für die Sequenzierung gepoolt; daher ist eine vergleichende Kreuzisotypanalyse nicht durchführbar.
Wie in Abb. 1b gezeigt, haben wir einen Klon als eine Gruppe von Zellen definiert, die von einem gemeinsamen Vorfahrenmolekül abstammen, das dasselbe IGHV- und IGHJ-Segment, dieselbe CDR3-Länge und 90-prozentige Nukleotididentität zwischen CDR3s aufweist, wie zuvor in Studien zu adaptivem B definiert -Zellantworten'8. Diese Definition ermöglicht es, Diversität, gemeinsame oder gemeinsame Zapfen und klonale Expansion im Zusammenhang mit Alloimmunität zu untersuchenNiereTransplantationen. Die Anzahl der eindeutigen Zapfen pro Person zu jedem Zeitpunkt ist im Zusatzmaterial als Balkendiagramm dargestellt (Ergänzungs-Abb. 1). Für die Stringenz der Datenanalyse haben wir die Proben mit rabattiert<100 clones="" (69="" samples="" from="" gdna="" and="" 55="" samples="" from="" cdna="" were="" left="" for="" further="" study.="" ige="" isotype="" was="" discarded="" completely="" due="" to="" a="" very="" small="" number="" of="" reads).="" in="" addition,="" we="" filtered="" outpatient="" 8="" in="" the="" np="" group="" from="" subsequent="" analysis,="" as="" we="" recognized="" after="" the="" run,="" that="" he="" had="" developed="" ebv+post="" transplant="" lymphoproliferative="" disease(ptld)at="" 2.2="" years="" post="">NiereTransplantation, gekennzeichnet durch die Proliferation von Epstein Barr
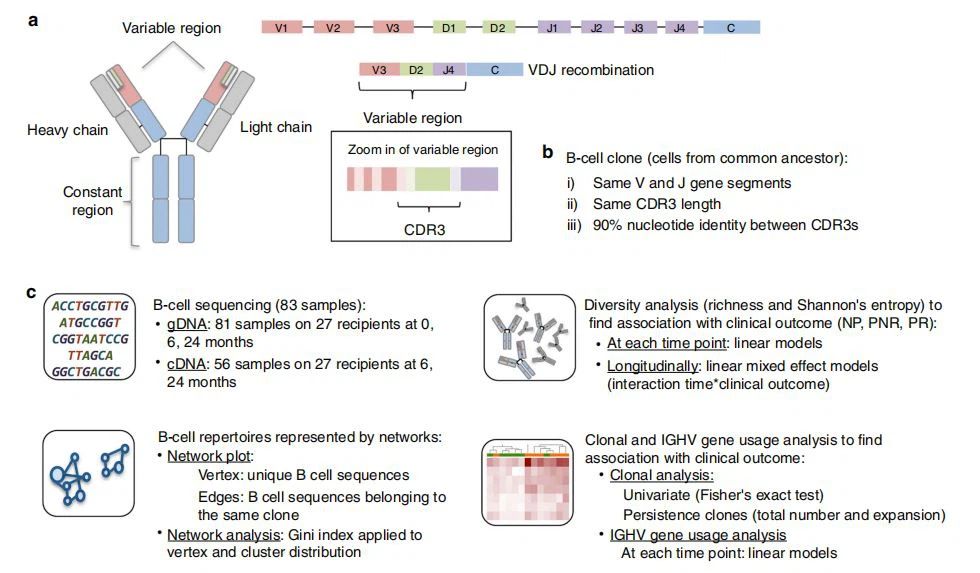
Abb. 1Gesamtstudienpipeline.a Schematische Darstellung der Antikörperstruktur und des Prozesses der VDJ-Rekombination, die für die im Immunrepertoire produzierte Diversität verantwortlich sind.b B-Zellklon, definiert als Zellen eines gemeinsamen Vorfahren und c Analysepipeline der Studie: B-Zelle Sequenzierung für gDNA und cDNA, Diversitätsanalyse unter Berücksichtigung der Anzahl der Klone (Reichtum) und der Häufigkeit jedes Klons (Shannon-Entropie), Netzwerkanalyse sowie Klon- und IGHV-Genanalyse
Virus (EBV) infizierte B-Zellen. Wir beobachteten eine erhöhte Anzahl von Klonen zum Zeitpunkt 6 bei diesem Patienten, mit geringerer klonaler Diversität zuvorNiereTransplantation und 24 Monate nach der Nierentransplantation. Da Bibliotheken aus einer unveränderlichen Matrizenmenge amplifiziert wurden, kann ein höherer Anteil an B-Zellen im Blut zu einer größeren Anzahl von Klonotypen geführt haben, die in den sequenzierten Produkten vertreten sind. Aufgrund des ausgeprägten und einzigartigen pathologischen Prozesses bei diesem Patienten wurde diese Probe von der zukünftigen Analyse ausgeschlossen.
B-Zell-Diversität vor der Transplantation ist mit Abstoßung verbunden. Wie in Abb. 1c gezeigt, untersuchten wir die Diversität des B-Zell-Immunrepertoires unter Berücksichtigung des Artenreichtums (Anzahl einzigartiger Klone) und der Shannon-Entropie (Gleichung (1) aus Methoden) über Zeitpunkte und klinische Ergebnisse hinweg unter Verwendung eines linearen Regressionsmodells unter Berücksichtigung der Anzahl von Klonen oder Entropie als abhängige Variable und klinisches Ergebnis oder SHM als unabhängige Faktorvariable. Das Repertoire vorherNiereTransplantation in PR war signifikant vielfältiger als in NP (Reichtum: P-Wert=0,005, Entropie: P-Wert=0,01), wobei der gleiche Trend 6 Monate danach anhieltNiereTransplantation (Reichtum: P-Wert=0.02, Entropie: P-Wert=0.02) und ohne unterscheidbare Gruppenunterschiede 2 Jahre nach der Transplantation (Abb. 2a und ergänzende Abb. 2). cDNA-Sequenzierungsdaten nach der Transplantation zeigten 6 Monate nach der Transplantation den gleichen Trend in größerer Repertoirediversität, hauptsächlich für die IgD-Isotypen (Reichtum: P-Wert=0,02, Entropie: P-Wert=0). 03) (Abb. 2b und ergänzende Abb. 2). Es gab keine verwirrenden Auswirkungen auf die Daten aus verschiedenen demografischen und klinischen Variablen, wie z. B. Alter, Geschlecht, Rasse, Spenderquelle, Art der Immunsuppression, HLA-Fehlpaarung und Ursache des Nierenversagens. Da die B-Zell-Antwort eines 1--Jährigen (das Mindestalter in den Daten) und eines 19--Jährigen (das Höchstalter in den Daten) sehr unterschiedlich sein kann, haben wir eine Sensitivität durchgeführt Analyse ohne diese beiden Patienten und die Ergebnisse blieben signifikant (NP vs. PR zum Zeitpunkt 0: Reichhaltigkeit: P-Wert=0,01, Entropie: P-Wert=0,03). In einem weiteren Maß für die Vielfalt des Immunrepertoires bewerteten wir die SHM, definiert als die Häufigkeit von Mutationen in jedem V-Gensegment, und fanden einen Trend zu einer höheren Anzahl von SHM für PR vor der Transplantation und einen Trend zu einer höheren SHM im IgD-Isotyp in PR 6 Monate nach der Transplantation (P-Wert=0,06).
Die B-Zell-Diversität ändert sich im Laufe der Zeit durch das klinische Ergebnis. Um herauszufinden, ob sich die Diversität des Immunrepertoires im Laufe der Zeit durch das klinische Ergebnis ändert, modellierten wir die Längsschnittdaten unter Verwendung von linearen Mixed-Effect-Modellen unter Berücksichtigung der Wechselwirkung zwischen klinischem Ergebnis und Zeit. Wir fanden heraus, dass sich NP und PR im Laufe der Zeit nach der Transplantation unterschiedlich verhielten, was eine Zunahme der Diversität in NP und eine Abnahme der Diversität in PR zeigte, während die Diversität für PNR im Laufe der Zeit unverändert blieb. Dies wurde für gDNA (Reichtum: P-Wert=0.007, Entropie: P-Wert=0.001, Abb. 3a) und alle Isotypen für cDNA beobachtet, wobei die signifikantesten Unterschiede in der Entropie waren für IgM- und IgD-Isotypen (IgA: P-Wert=0.07, IgD: P-Wert=0.02, IgG: P-Wert=0.05, IgM: P-Wert=0.04, Abb. 3b). Die Diagramme für den Reichtum mit den entsprechenden P-Werten sind in der ergänzenden Abb. 3 dargestellt. Wie in den Diagrammen beobachtet, hat eine Person zum Zeitpunkt 32 Monate eine zusätzliche Probe, was die Ergebnisse verzerren könnte, daher wurde eine Sensitivitätsanalyse unter Ausschluss dieser Probe durchgeführt die Analyse und Beobachtung ähnlicher Ergebnisse mit Ausnahme der IgG- und IgM-Isotypen, bei denen die Signifikanz verloren geht (gDNA-Entropie: P-Wert=0.004. cDNA-Entropie: IgA: P-Wert=0.1 , IgD: P-Wert=0,05, IgG: P-Wert=0,08, IgM: P-Wert=0,1).
Diversity-Maßnahmen können durch biologische und technische Probenahmen beeinträchtigt werden. Die Diversität einer Probe kann sich deutlich von der Gesamtdiversität in einem Repertoire unterscheiden, da nur ein Bruchteil von Milliarden von Zellen repräsentiert wird, was als Missing-Species-Problem bekannt ist. Es kann eine technische Probenahme geben, da jede Probe in der Sequenzierungstiefe und einem gewissen Grad an experimentellen Fehlern variieren kann. Um das Problem fehlender Arten zu lösen, haben wir das Recon-Tool (Rekonstruktion geschätzter Klone aus beobachteten Zahlen)29 verwendet, das die Gesamtverteilung der Klongröße schätzt. Recon gibt genaue und robuste Schätzungen einer Reihe von Diversitätsmaßen aus, einschließlich Reichhaltigkeit und Entropie, was robuste Vergleiche der Diversität zwischen Individuen ermöglicht. Um mit der Sequenzierungstiefe und einem gewissen Grad an experimentellen Fehlern fertig zu werden, haben wir eine Downsampling-Strategie durchgeführt; eine sehr verbreitete Strategie in der Immunrepertoireanalyse11,17,30. In der Recon-Analyse (Ergänzende Abb. S4: A–E) wurden sowohl Reichtum als auch Vielfalt für die gDNA-Daten repliziert. In den cDNA-Daten zeigt der IgD-Isotyp zum Zeitpunkt 6 den Trend, erreichte jedoch keine Signifikanz, obwohl die Längsschnittergebnisse für IgA-, IgD- und IgG-Isotypen repliziert wurden. In der Downsampling-Analyse (ergänzende Abb. S4: F–J) wird alles repliziert, aber die Zeit ist 0 für gDNA-Daten. Dies könnte eine Folge der Einschränkung sein, die das Downsampling hat
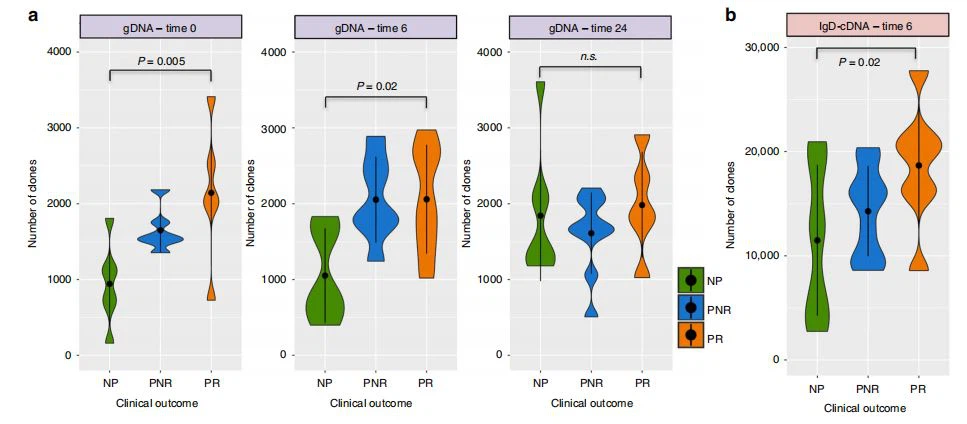
Abb. 2 Violin-Plots, die die Anzahl der Klone (Reichtum) über die drei klinischen Ergebnisse hinweg zeigen. eine Reihe von Klonen zu den Zeiten 0, 6 und 24 aus gDNA-Proben. b Anzahl der Klone zum Zeitpunkt 6 für den IgD-Isotyp aus cDNA-Proben. Die P-Werte werden aus der Anpassung eines linearen Regressionsmodells erhalten, wobei die Anzahl der Klone als abhängige Variable und das klinische Ergebnis als unabhängige Faktorvariable berücksichtigt werden (n=27 Stichproben). Violinplots repräsentieren die Wahrscheinlichkeitsdichte der Daten bei jedem Wert. Die Punktmarkierung repräsentiert den Medianwert mit dem Interquartilsabstand. Quelldaten werden als Quelldatendatei bereitgestellt

Abb. 3 Längsschnittdaten aufgetragen mit der angepassten Linie für jedes klinische Ergebnis. a Diversität, gemessen anhand der Shannon-Entropie, dargestellt über die Zeitpunkte durch die drei klinischen Endpunkte (NP, PNR, PR) in gDNA. b Diversität, gemessen anhand der Shannon-Entropie, dargestellt über die Zeitpunkte durch die drei klinischen Ergebnisse (NP, PNR, PR) nach Isotypen in cDNA. Die P-Werte entsprechen dem Interaktionsterm, definiert durch Zeit × klinisches Ergebnis, angepasst an ein lineares Mixed-Effect-Modell (n=27 Proben). Jeder Punkt repräsentiert die Entropie pro Abtastwert über die Zeit mit seiner angepassten Linie und seinem Konfidenzintervall. Quelldaten werden als Quelldatendatei bereitgestellt
Strategien impliziert, insbesondere bei den gDNA-Daten, wo die Anzahl der Sequenzen viel geringer ist als bei den cDNA-Daten. Bei gDNA haben wir die Analyse auf Personen mit mindestens 10 Klonen beschränkt, um genügend Sequenzen zu erhalten. Das Downsampling wurde auf ein Minimum von 1062 Klonen im Vergleich zu 62.173 Klonen in cDNA durchgeführt. Trotz dieser Einschränkung beobachteten wir den Trend zum Zeitpunkt 0, bewahrten die Signifikanz für die Längsschnittanalyse in gDNA und replizierten alle Assoziationen in cDNA. In beiden Analysen (Recon und Downsampling) replizierten wir die Ergebnisse trotz einiger hier hervorgehobener Einschränkungen, was die Gültigkeit der zuvor gemeldeten Ergebnisse zeigt.
B-Zell-Netzwerke zeigen Unterschiede in der klonalen Expansion. Das B-Zell-Repertoire kann auf natürliche Weise als Netzwerk basierend auf Sequenzdiversität dargestellt werden31. In unseren Daten haben wir für jede Probe ein visuelles Netzwerk entwickelt (Abb. 4 und ergänzende Abb. 5–7), in dem jeder Scheitelpunkt einen eindeutigen BCR darstellt und die Anzahl identischer BCRs basierend auf ihren Nukleotidsequenzen die Scheitelpunktgröße definiert. Zwischen Scheitelpunkten existiert eine Kante, wenn sie zu demselben Klon gehören, sodass Cluster von B-Zellen als Gruppen von miteinander verbundenen Scheitelpunkten gezeigt werden können, die einen Klon bilden. Um das Netzwerk zu quantifizieren, haben wir den Gini-Index verwendet, bei dem es sich um ein Ungleichmäßigkeitsmaß handelt, das auf die Scheitelpunkt- und Clusterverteilungen angewendet wurde. Bei Anwendung auf die Vertexgröße Gini(V) wird die klonale Gesamtnatur dargestellt. Wenn Gini(V) näher an 1 liegt, sind die Eckpunkte ungleich und zeigen die Ausdehnung einiger von ihnen, andernfalls näher an 0. Bei Anwendung auf die Clustergröße Gini(C) wird klonale Dominanz dargestellt. Wenn näher an 1, sind die Cluster ungleich und stellen daher dominante Klone dar, wenn näher an 0, sind alle Cluster gleich groß.
In Abb. 4 zeigen wir ein Beispiel für die deutlichen visuellen und quantitativen Unterschiede zwischen repräsentativen B-Zell-Repertoires aus jeder der drei klinischen Ergebnisgruppen über die drei verschiedenen Zeitpunkte (vor der Transplantation und nach der Transplantation 6 und 24 Monate) . Im PR-Repertoire gibt es eine Fülle von B-Zell-Sequenzen, die im Vergleich zu NP mehr und größere Kloncluster bilden, während PNR dazwischen liegt. Im Laufe der Zeit zeigt die PR-Gruppe im Vergleich zu NP eine Abnahme der Anzahl von BCR und eindeutigen Klonen. Die detaillierten B-Zell-Netzwerke jeder Person in der Studie sind in den ergänzenden Abbildungen angegeben. 5–7. Es ist interessant, das sehr unterschiedliche Muster des B-Zell-Netzwerks bei dem Individuum zu beobachten, das PTLD in der NP-Gruppe entwickelt hat (ergänzende Abb. 5), ohne B-Zell-Expansion vor der Transplantation, gefolgt von einer Zunahme von B-Zellen nach 6 Monate und eine deutliche klonale Expansion begleitet von einer Abnahme der Diversität 24 Monate nach der Transplantation.
Bei der weiteren Auswertung des Gini-Index-Messwerts (Abb. 5) zeigte die PR-Gruppe durchweg signifikant höhere Messwerte sowohl für den Vertex als auch für das Cluster gegenüber der NP-Gruppe, was darauf hindeutet, dass die Patienten der PR-Gruppe zu Studienbeginn eine höhere klonale Expansion aufwiesen.

Abb. 4 B-Zell-Repertoire-Netzwerke von drei Personen, die die drei klinischen Ergebnisse über die Zeitpunkte hinweg darstellen. Jeder Scheitelpunkt stellt einen einzigartigen BCR dar, wobei die Scheitelpunktgröße durch die Anzahl identischer BCRs unter Berücksichtigung der Nukleotidsequenzen definiert ist. Zwischen Scheitelpunkten existiert eine Kante, wenn sie wie zuvor definiert zu demselben Klon gehören, also sind Cluster Gruppen von miteinander verbundenen Scheitelpunkten, die einen Klon bilden. Jede Probe zeigt den für die Scheitelpunktgröße (Gini(V)) und die Clustergröße (Gini(C)) erhaltenen Gini-Index. BCR spiegelt die Gesamtzahl der B-Zell-Rezeptoren für diese spezifische Probe wider und Klone spiegeln die Gesamtzahl einzigartiger Klone wider. Quelldaten werden als Quelldatendatei bereitgestellt
und weitere Expansion nach der Transplantation einer Teilmenge dominanter Klone (P-Wert [lineare Regression] < 0.05,="" fig.="" 5).="" die="" pnr-gruppe="" fällt="" wie="" zuvor="" gezeigt="" zwischen="" np="" und="" pr,="" obwohl="" sich="" diese="" zeit="" signifikant="" von="" der="" np-gruppe="" zum="" zeitpunkt="" 24="" unterscheidet="" (p-wert="" [lineare="" regression]="">< 0,05).="" obwohl="" die="" daten="" für="" fig.="" 5="" aus="" den="" gdna-daten="" generiert="" wurden,="" zeigte="" der="" igm-isotyp="" für="" cdna="" die="" gleichen="" unterschiede="" (p-wert="" [lineare="" regression]="0,05)" (ergänzende="" fig.="">
Bestimmte Klone und IGHV-Gene sind an der Abstoßung beteiligt.
Obwohl unser Hauptaugenmerk darauf lag, das B-Zell-Repertoire nach klinischen Ergebnisgruppen zu charakterisieren, um ein globales Bild der Immunantwort vor und nach der Transplantation zu liefern, ermöglichten uns unsere Daten auch, Ig-sequenzspezifische Analysen am Klon und am IGHV durchzuführen Genebene.
Für die Klonanalyse bewerteten wir die Assoziation des Vorhandenseins oder Fehlens jedes bestimmten Klons (insgesamt 118.223 Klone) mit dem klinischen Ergebnis (PR, PNR, NR) zu jedem Zeitpunkt. Unter Anwendung des exakten Tests von Fisher fanden wir 8, 4 und 21 Klone, die nominell mit klinischen Ergebnissen nach 0, 6 bzw. 24 Monaten assoziiert waren (Ergänzungstabelle 1). Während keiner die mehrfache Testkorrektur bestand, hauptsächlich aufgrund mangelnder Power, da wir eine begrenzte Stichprobengröße bei der Analyse mit Tausenden von Parametern (Klonen) haben, konnten wir beobachten, dass die wenigen Klone, die sich der Signifikanz näherten (P-Wert < {{="" 11}}.05)="" wurden="" von="" patienten="" nur="" in="" der="" pr-gruppe="" geteilt="" und="" 24="" monate="" nach="" der="" transplantation="">
Wir haben auch berücksichtigt, ob einige Klone innerhalb jedes klinischen Ergebnisses länger als andere über die Probenahmezeit bestehen blieben (Ergänzende Abb. 9). Wir berücksichtigen zwei verschiedene Maße: (1) die Anzahl der persistenten Klone und (2) die klonale Expansion. Wir beobachteten, dass die Klone, die im PR persistent waren, signifikant stärker expandiert waren (P-Wert [lineare Regression]=0.01, PR vs. NP) und einen Trend zu einer höheren Anzahl persistenter Klone zeigten (P- Wert [lineare Regression]=0.09). Wir untersuchten ferner, ob diese persistenten Klone innerhalb jedes klinischen Ergebnisses auch von verschiedenen Personen gemeinsam genutzt wurden. Von den 263 nachgewiesenen persistenten Klonen wurden 23 von Individuen geteilt. Fünf wurden innerhalb desselben PNR und sechs innerhalb der PR-Gruppe geteilt und keine Klone wurden zwischen der NP-Gruppe geteilt. Insgesamt waren 12 gemeinsame Klone in beiden Patientengruppen mit fortschreitender chronischer Transplantationsverletzung und Fibrose im Laufe der Zeit (PR und PNR) verbreitet. Die Liste der von Einzelpersonen gemeinsam genutzten Klone ist im ergänzenden Material (Ergänzungstabelle 2) enthalten.
Als nächstes führten wir eine IGHV-Genanalyse durch und betrachteten die IGHV-Gennutzung pro Probe, definiert als die Häufigkeit, mit der jedes IGHV-Gen verwendet wurde, normalisiert durch die Anzahl der Klone (um eine Stichprobenverzerrung bestimmter IGHV-Gene zu vermeiden) und filterten niedrig exprimierte aus

Abb. 5 Vertex-Gini-Index aufgetragen gegen Cluster-Gini-Index. Das Streudiagramm stellt jede Probe zu den Zeitpunkten 0, 6 und 24 dar. Boxplots zeigen die Gini(V)- und Gini(C)-Unterschiede zum Zeitpunkt 24. Die P-Werte werden aus der Anpassung eines linearen Regressionsmodells erhalten Berücksichtigung von Gini(V) und Gini(C) als abhängige Variable und klinisches Ergebnis als unabhängige Faktorvariable für jeden Zeitpunkt (n=27 Stichproben). Im Boxplot ist nur Zeit 24 gezeigt, aber Zeit 0 und 6 waren auch signifikant für NP vs. PR: Zeit 0: P (Gini (V))=0.1, P ( Gini(C))=0.05; Zeit 6 P (Gini(V))=0.02, P (Gini(C))=0.01; Zeit 24: P (Gini(V))=0.003, P (Gini(C))=0.01. Das Band innerhalb der Box stellt den Medianwert dar, die Box definiert den Interquartilbereich (IQR) und Whisker definieren das erste und dritte Quartil ± 1,5 × IQR. Quelldaten werden als Quelldatendatei bereitgestellt
Gene (IGHV-Gennutzung > {0}}.05 in mindestens 10 Prozent der Proben) und Anwendung eines linearen Regressionsmodells, um die assoziierten Gene zu finden mit jedem klinischen Ergebnis zu jedem Zeitpunkt. Von den 27 IGHV-Genen, die den Niedrigexpressionsfilter passierten, fanden wir signifikante Gene zwischen der PR- und NP-Gruppe (P-Wert < 0.05)="" mit="" drei="" genen="" zum="" zeitpunkt="" 0,="" 7="" zum="" zeitpunkt="" 6="" und="" 16="" um="" zeit="" 24="" (abb.="" 6a–c).="" von="" diesen="" genen,="" 1="" (ighv3-11)="" zum="" zeitpunkt="" 0,="" 5="" gene="" (ighv3-7,="" ighv3-15,="" ighv3-21,="" ighv3-23,="" ighv{="" {22}})="" zum="" zeitpunkt="" 6="" und="" 16="" gene="" (ighv1-8,="" ighv1-18,="" ighv1-46,="" ighv2-="" 5,="" ighv3-7,="" ighv{{="" 30}},="" ighv3-15,="" ighv3-23,="" ighv3-30,="" ighv3-33,="" ighv3-48,="" ighv3-74,="" ighv{{37="" }},="" ighv4-59,="" ighv4-61,="" ighv5-51)="" zum="" zeitpunkt="" 24="" bestanden="" die="" korrektur="" der="" false="" discovery="" rate="" (fdr)="" für="" mehrere="" tests.="" interessanterweise="" fanden="" wir="" heraus,="" dass="" ighv3-23="" zu="" allen="" drei="" zeitpunkten="" im="" np="" vs.="" pr-vergleich="" das="" signifikanteste="" und="" am="" häufigsten="" vorkommende="" gen="" war="" (zeit="" 0:="" p-wert="0.04," zeit="" 6:="" p-="" wert="0.003," zeit="" 24:="" p-wert="0.02)" (abb.="" 6d).="" außerdem="" bewerteten="" wir,="" ob="" die="" ighv3-23-sequenzen="" unter="" den="" gemeinsamen="" sequenzen="" aus="" der="" vorherigen="" klonanalyse="" überrepräsentiert="" waren.="" wir="" fanden="" unter="" verwendung="" einer="" anreicherungsanalyse="" mit="" dem="" exakten="" test="" von="" fisher="" heraus,="" dass="" die="" ighv3-23-sequenzen="" in="" beiden,="" den="" persistenten="" klonen,="" die="" von="" individuen="" geteilt="" wurden,="" signifikant="" überrepräsentiert="" waren="" (ergänzungstabelle="" 2)="" (p-wert="">< 2,2="" ×="" 10="" –="" 16="" )="" und="" die="" mit="" dem="" klinischen="" ergebnis="" assoziierten="" klone="" zum="" zeitpunkt="" 24="" (ergänzungstabelle="" 1)="" (p-wert="">< 2,2="" ×="" 10–16).="" wir="" beobachteten,="" dass="" individuum="" 9="" in="" der="" nr-gruppe,="" von="" dem="" festgestellt="" wurde,="" dass="" es="" einige="" persistente="" klone="" mit="" den="" progressoren="" in="" den="" vorherigen="" analysen="" teilte,="" zu="" allen="" zeitpunkten="" mit="" der="" pr-gruppe="" klassifiziert="" wurde.="" es="" gab="" keine="" verwirrenden="" auswirkungen="" auf="" die="" daten="" aus="" verschiedenen="" demografischen="" und="" klinischen="" variablen,="" wie="" z.="" b.="" alter,="" geschlecht,="" rasse,="" spenderquelle,="" art="" der="" immunsuppression,="" hla-fehlpaarung="" und="" ursache="" des="" nierenversagens.="" darüber="" hinaus="" wurde="" festgestellt,="" dass="" dieses="" gen="" sowohl="" bei="" den="" isotypen="" igm="" (p-wert="" [lineare="" regression]="0.008)" als="" auch="" igd="" (p-wert="" [lineare="" regression]="0.05)" signifikant="" ist="" basierend="" auf="" cdna="" 24="" monate="" nach="" der="" transplantation,="" in="" übereinstimmung="" mit="" den="" vorherigen="" ergebnissen,="" die="" übereinstimmung="" zeigen,="" dass="" diese="" beiden="" isotypen="" in="" der="" pr-gruppe="" am="" stärksten="" angereichert="" sind.="" nur="" drei="" weitere="" gene="" wurden="" in="" der="" cdna-analyse="" als="" signifikant="" befunden,="" und="" alle="" waren="" 24="" monate="" nach="" der="" transplantation="" in="" igd-="" und="" igm-isotypen="" (ighv3-15="" und="" ighv4-="" 61="" in="" igd="" und="" ighv4-39="" in="">

Diskussion
Diversität ist ein wesentliches Merkmal des Immunsystems und bei gesunden Menschen entscheidend gegen Krankheitserreger. Bei der Organtransplantation wird klinisch eine absichtliche therapeutische Manipulation eingeleitet, um zu ermöglichen, dass das fremde Organ vom Immunsystem des eigenen Patienten aktiv ignoriert oder akzeptiert wird, um keine Alloimmunantwort auszulösen, die zu einer Abstoßung führt. B-Zellen sind eine wichtige Komponente dieses Prozesses und es wurde von unserer Gruppe und anderen gezeigt, dass sie sowohl bei der Antigenpräsentation32,33 als auch bei der Alloantikörperproduktion34,35 eine zentrale Rolle spielen. In dieser Arbeit haben wir Hochdurchsatz-B-Zell-Sequenzierung verwendet, um die Diversität und Klonalität von B-Zellen besser zu verstehenNieredes Kreislaufs des Transplantatempfängers, sowohl vor der Transplantation als auch nach 24 Monaten Nachbeobachtung, mit einer Längsschnittbewertung des B-Zell-Immunrepertoires. Insgesamt zeigt unsere Analyse eine höhere B-Zell-Diversität vor der Transplantation, Unterschiede in Längsrichtung mit einer Abnahme der Diversität, begleitet von einer klonalen Expansion, und eine Zunahme der Verwendung bestimmter IGHV-Gene bei denjenigen, die die Transplantate später ablehnen.
Ein wichtiger unerfüllter klinischer Bedarf an Organtransplantationen ist das Fehlen einer nicht-invasiven, empfindlichen und genauen Vorhersage von Transplantationsverletzungen und schlechten Ergebnissen. Diese Aufgabe wird durch die Tatsache erschwert, dass es verschiedene Faktoren gibt, die das Überleben des Transplantats beeinflussen36. In dieser Studie fanden wir heraus, dass stabile Personen vor der Transplantation eine geringere Diversität des B-Zell-Immunrepertoires aufwiesen als diejenigen, die das Organ abgestoßen hatten. Der nächste Schritt sollte darin bestehen, den Vorhersagewert der Diversität des B-Zell-Repertoires zu demonstrieren, wodurch potenziell bessere Biomarker für die Vorhersage der Abstoßung vor der Transplantation und die Möglichkeit der Implementierung in die klinische Versorgung und die Auswahl der Immunsuppression vor und nach der Transplantation bereitgestellt werdenNiereTransplantation. Wenn dieses Merkmal das Ergebnis eines Faktors ist, der zur Abnahme der Diversität bei stabilen Individuen beiträgt, wie z. B. Umwelt- oder genetische Faktoren, könnten wir die Abstoßung nicht nur vorhersagen, sondern auch verhindern. In der Tat zeigten jüngste Erkenntnisse, dass die Veränderung des Immunsystems durch umweltbedingte, mentale und genetische Faktoren angetrieben wird37,38. In unserer Studie konnten wir keinen Zusammenhang mit irgendwelchen demografischen oder anderen klinischen Patientenmerkmalen (Alter, Geschlecht, ethnische Zugehörigkeit, Immunsuppression, Organquelle, HLA-Fehlpaarungen und ESRD) feststellen. In dieser Hinsicht benötigen wir eine neue Analyse, um zu bestätigen, ob spezifische Faktoren die Diversität des B-Zell-Repertoires und die Transplantationsergebnisse beeinflussen.
Ein weiterer interessanter Befund unserer Studie zeigt, dass sich das Immunrepertoire je nach klinischer Outcome-Gruppe über die Zeit unterschiedlich verhält. Bei denjenigen, die nach der Transplantation eine Abstoßung des Organs zeigen, ist die B-Zell-Diversität anfangs höher und nimmt dann im Laufe der Zeit ab, während der umgekehrte Diversitätstrend bei Patienten zu sehen ist, die keine Abstoßung oder chronische Transplantatverletzung entwickeln. Obwohl alle Personen nach der Transplantation die gleiche Immunsuppressionslast erhielten, könnte eine mögliche Erklärung für die verringerte Diversität bei den Patienten, die eine Abstoßung entwickeln, mit der Tatsache zusammenhängen, dass diese Patienten eine vorübergehend stark erhöhte Immunsuppressionslast zur Behandlung der Abstoßung und dann erhalten werden auf der höheren Grundlinie gehalten. Obwohl dies die Verringerung der B-Zell-Diversität im Laufe der Zeit und den Unterschied 24 Monate nach der Transplantation erklären könnte, ist dies unwahrscheinlich, dass dies die Ursache ist, wie dies bei der verringerten Diversität in der PR-Gruppe der Fall ist

Abb. 6 Heatmap und Boxplot für die IGHV-Gennutzungsanalyse. Heatmap mit den als nominell signifikant ausgewählten IGHV-Genen (P-Wert < 0.05)="" zum="" zeitpunkt="" 0="" (a),="" 6="" (b)="" und="" 24="" (c)="" für="" np="" gegen="" pr.="" die="" rote="" farbskala="" repräsentiert="" die="" expression="" jedes="" gens="" über="" die="" proben="" hinweg.="" die="" bänder="" oben="" zeigen="" das="" klinische="" ergebnis="" und="" die="" ursache="" der="" esrd.="" boxplot="" mit="" ighv3-23-ausdruck="" über="" zeitpunkte="" für="" np="" vs.="" pr="" (zeit="" 0:="" p-wert="0.04," zeit="" 6:="" p-wert="0.003," zeit="" 24:="" p="" -wert="0.02)" (d).="" das="" band="" innerhalb="" der="" box="" stellt="" den="" medianwert="" dar,="" die="" box="" definiert="" den="" interquartilbereich="" (iqr)="" und="" whisker="" definieren="" das="" erste="" und="" dritte="" quartil="" ±="" 1,5="" ×="" iqr.="" p-werte="" werden="" aus="" der="" anpassung="" eines="" linearen="" regressionsmodells="" erhalten,="" das="" die="" v-gene="" als="" abhängige="" variable="" und="" das="" klinische="" ergebnis="" als="" unabhängige="" variable="" berücksichtigt.="" (n="12" proben).="" quelldaten="" werden="" als="" quelldatendatei="">
auch 6 Monate nach der Transplantation zu sehen, zu einem Zeitpunkt, an dem die Patienten noch keine Abstoßung entwickelt haben, was darauf hindeutet, dass wahrscheinlich andere aktive Prozesse beteiligt sind. Die Beobachtung einer selektiven klonalen Expansion mit dominanteren Klonen nur bei Patienten, die sowohl eine Abstoßung als auch/oder eine fortschreitende chronische Erkrankung entwickelnNiereTransplantationsverletzung, legt eine biologisch relevante, Alloantigen-gesteuerte Selektion, Persistenz und Expansion bestimmter Klone im Laufe der Zeit nahe, was für die allgemeine Verringerung der zeitlichen Diversität verantwortlich ist. Obwohl wir die Hypothese aufstellen können, dass die Expansion dieser Klone wahrscheinlich mit einer alloimmunen Verletzung des Transplantats verbunden ist, erfordert ein direkter Beweis, dass die Expansion dieser Klone alloimmun ist, zusätzliche In-vitro- und Tierstudien.
Die akute Abstoßung bleibt der stärkste negative Faktor für das langfristige Überleben des Transplantats trotz der raschen Verbesserungen bei den Immunsuppressionstherapien39,40. Diese Studie findet auch einen Zusammenhang zwischen der Verwendung einiger IGHV-Gene und Abstoßung, obwohl der kausale Zusammenhang in zukünftigen Studien untersucht werden sollte. Das IGHV3-23 ist das interessanteste Gen in der gDNA-Analyse, da es bei Patienten, die zu allen gemessenen Zeitpunkten eine Abstoßung entwickeln, signifikant häufiger verwendet wird und in den persistenten Klonen, die von Einzelpersonen geteilt werden, und den angereicherten Klonen überrepräsentiert ist abgelehnte Patienten 24 Monate nach der Transplantation. Dieses Gen wird auch 24 Monate nach der Transplantation sowohl im IgD- als auch im IgM-Isotyp in der cDNA-Analyse validiert. IGHV3-23 wurde umfassend mit einer schlechten Prognose bei chronischer lymphatischer Leukämie in Verbindung gebracht41 und es wurde gezeigt, dass die überwiegende Mehrheit der IGHV3-23-Sequenzen die Fähigkeit zur Vermittlung von Superantigen-Wechselwirkungen beibehielt42. B-Zell-Superantigene werden von Viren und Bakterien produziert, von denen bekannt ist, dass sie außerhalb der herkömmlichen Antigen-Bindungsstellen an Immunglobuline binden43. Begegnungen von B-Zellen mit einem Superantigen führen nachweislich zu Proliferation, Aktivierung, Migration und Deletion44. Im transplantiertenNierebesteht die Möglichkeit einer kontinuierlichen Exposition gegenüber dem Virus und bakteriellen Antigenen, die sich entweder auf die Ätiologie eines primären vesikoureteralen Refluxes als Ursache der ESRD oder eines sekundären Harnrefluxes nach Reimplantation des transplantierten Harnleiters oder eines Refluxes nach einer Harnwegsinfektion beziehen die bei Exposition gegenüber chronischer Immunsuppression nach der Transplantation erhöht ist. Wir haben die Analyseergebnisse neben anderen klinischen und demografischen Faktoren um die Ursache des Nierenversagens angepasst; Die zuvor diskutierten Ergebnisse bleiben signifikant, obwohl wir feststellten, dass der fehlklassifizierte NP-Patient in der Analyse (Abb. 6) eine Refluxkrankheit hatte. Chenget al. haben auch zuvor festgestellt, dass Klone in Biopsiegewebe von Empfängern von Nierentransplantaten, die von B-Zellen infiltriert wurden, unter anderem eine Dominanz des IGHV3-23-Gens aufwiesen45. Grover et al.46 zeigten, dass die Antikörper für dieses spezielle Gen keine Spender-HLA-Antigene erkannten, sondern spezifisch für E. coli waren, und Modena et al.47 zeigten, dass die Belastung durch die Anzahl der Bakterien im Urin bei Patienten mit interstitielle Fibrose und tubuläre Atrophie als diejenigen mit gut funktionierenden Transplantaten. Wir erweitern diese Erkenntnisse und zeigen, dass die Verwendung des IGHV3-23-Gens bei mehrfach abstoßenden Patienten im peripheren Blut signifikant höher ist und bestimmte gemeinsame Antigene bei der Auslösung der Abstoßung implizieren kann. In Zukunft könnte die Expression von IGHV3-23 potenziell zur Überwachung der Immunantwort gegenüber dem Transplantierten verwendet werdenNiere.

Indem wir unsere Studie mithilfe der cDNA-Sequenzierung erweiterten, konnten wir den Großteil unserer Ergebnisse in zwei der Isotypen (IgM und IgD) replizieren, die eine geringere Diversität vor der Transplantation im NP zeigten, wobei die beiden in der Längsschnittanalyse mit größerer Expansion und Dominanz am signifikantesten waren Klone in der Netzwerkanalyse und auch die Replikation des IGHV3-23-Gens. Die ersten Antikörper, die bei einer humoralen Immunantwort produziert werden, sind immer IgM und entwickeln sich schnell zur Produktion all der verschiedenen Isotypen, IgD, IgA, IgG und IgE, aber besonderes Interesse erfordert den IgD-Isotyp48. IgD wird zusammen mit IgM exprimiert und sezerniertes IgD existiert und hat eine Funktion in Blut, Schleimhautsekreten und auf der Oberfläche von angeborenen Immuneffektorzellen wie Basophilen49. Basophile sind weiße Blutkörperchen, die Viren, Bakterien, Parasiten und Pilze bekämpfen und an Nierenerkrankungen und Transplantatabstoßung beteiligt sind50. Somit ein weiterer Beweis, der die B-Zell-Antworten mit dem Abstoßungsprozess bei Viren und Bakterien in Verbindung bringt.
Zukünftige Studien müssen zeigen, dass diese Aktivierung auf Unterschiede im Empfängermikrobiom mit Auswirkungen auf Diagnostik und Therapie zurückzuführen ist.
Diese Studie ermöglichte es uns, die Relevanz einiger dieser BCR-Klone zu identifizieren, die klinisch relevanten BCR-Klone mit Allotransplantat-Abstoßung zu identifizieren und zu zeigen, dass es eine wahrscheinliche Relevanz dieser Klone mit heterologer Immunität gibt, angesichts der Anreicherung dieser Klone bei Patienten mit kolonisierte Harnwege vor der Transplantation und ihre biologische Relevanz für die Reaktion von Krankheitserregern. Ein besseres Verständnis des Verhaltens des Immunrepertoires inNiereTransplantationen wären ohne die Anwendung von BCRSeq in Kombination mit einer robusten Implementierung von Berechnungs- und Statistik-Pipelines nicht möglich gewesen. Dennoch gibt es mehrere Einschränkungen unseres Ansatzes, die beachtet werden sollten: Erstens ist unsere Stichprobengröße in einer Gruppe von pädiatrischen Patienten sehr ausgewählt und relativ klein, und obwohl wir in unserer Analyse eine statistische Signifikanz erreicht und in zwei verschiedenen Datenquellen validiert haben, Weitere Analysen sind erforderlich, um unsere Ergebnisse zu bestätigen. Zweitens sind unsere Ergebnisse nicht von dem Einfluss ausgenommen, den biologische und technische Probenahmen auf unsere Analyse haben können. Diversitätsmaße hängen von mehreren Faktoren ab: der Tatsache, dass nur ein Bruchteil von Milliarden Zellen in einem Repertoire in einer Probe vertreten ist, Unterschiede in der Sequenzierungstiefe und mögliche experimentelle Fehler. Wir haben all diese Probleme ausgiebig kontrolliert, erstens im Labor, indem wir die gleiche Menge Blut für jede Probe in derselben Charge analysierten, und zweitens, rechnerisch und statistisch, indem wir ein Recon-Tool anwendeten, um das Gesamtrepertoire abzuschätzen, und ein Downsampling durchführten, um die Sequenzierungstiefe zu kontrollieren und Versuchsfehler. Drittens haben wir BCRSeq mit zwei verschiedenen Quellen durchgeführt, gDNA und cDNA. Die Sequenzierung von gDNA erleichtert die Abschätzung der Klonalität einer bestimmten Ig-Sequenz, da die Anzahl der Sequenz-Reads proportional zur Anzahl der gDNA-Moleküle ist. Die Sequenzierung von cDNA liefert eine Schätzung des relativen Expressionsniveaus verschiedener Ig-Sequenzen im Repertoire. Es hat sich gezeigt, dass bei T-Zell-Rezeptoren die auf cDNA durchgeführte Klonotyp-Charakterisierung nicht so gut ist wie bei gDNA, was zeigt, dass der relative Anteil einzelner Klone sehr unterschiedlich ist15 oder dass die Verfolgung von HIV-spezifischen Klonen nur mit gDNA erfolgreich ist, aber nicht mRNA51. Viertens kann der Einfluss der Immunsuppression ein Störfaktor bei dieser Art von Analyse sein. In dieser Studie stammen alle Proben aus einer klinischen Studie, in der alle Patienten nach der Transplantation dieselbe immunsuppressive Belastung erhielten. Trotzdem haben wir die beiden Arten von Steroid-basierten und Steroid-freien kontrolliert, um sicherzustellen, dass dies kein Problem war, und keine Unterschiede in den Ergebnissen beobachtet. Schließlich ist die Kohorte, die wir hier präsentieren, die der pädiatrischen Transplantationen. Die Mehrheit der transplantierten klinischen Aspekte ist bei Kindern und Erwachsenen ähnlich. Die verwendete Immunsuppression und Therapien sind ähnlich, Kreatinin ist der Hauptserum-Biomarker, akute Abstoßung wird hauptsächlich mittels Biopsie unter Verwendung der Banff-Kriterien bestimmt, und die Abstoßungsmechanismen derNiereTransplantat sind im Allgemeinen ähnlich52, daher kann der Großteil der Forschung, die bei Erwachsenen oder Kindern durchgeführt wurde, für beide gelten. Andere Aspekte wie die Nichteinhaltung/Nichteinhaltung der Immunsuppression, immunologische Aspekte, die primären Nierenerkrankungen, die zu Nierenversagen führen, oft verbunden mit urologischen Problemen, und die vor der Transplantation erforderlichen Immunisierungen können jedoch abweichen, daher sind weitere Analysen erforderlich eine erwachsene Population wird notwendig sein, um diese Ergebnisse zu verallgemeinern.
Trotz dieser Einschränkungen zeigen unsere Daten, dass bei Personen, die das Organ später abstoßen, eine höhere Diversität vor der Transplantation beobachtet wird, was auf eine Veranlagung zur Abstoßung hindeutet, die zukünftige Auswirkungen auf die Vorhersage des Abstoßungsrisikos vor der Transplantation, die Wahl der Immunsuppression und die klinische Versorgung haben könnte Praktiken Methoden Ausübungen. Nach 24 Monaten Nachbeobachtung wird in der Abstoßungsgruppe im Laufe der Zeit eine allgemeine Verringerung der Diversität beobachtet, die von der Persistenz und Expansion bestimmter Klone und einer höheren Verwendung mehrerer IGHV-Gene begleitet wird, was dazu führen kann, dass bestimmte gemeinsame Antigene die Abstoßung fördern. Besonderes Interesse wird an der vermehrten Verwendung des IGHV3-23-Gens bei Abstoßungspatienten beobachtet, da es zuvor damit in Verbindung gebracht wurdeNiereTransplantation und könnte eine Schlüsselkomponente sein, um den Abstoßungsprozess voranzutreiben. Diese Arbeit stellt eine Längsschnittanalyse des B-Zell-Immunrepertoires bei Organtransplantationen vor und fördert weitere Studien zur Bestätigung dieser Ergebnisse, da sie klinische Auswirkungen auf die Vorhersage, Kontrolle, Überwachung und Behandlung haben könnenNiereAblehnung.
Methoden
Studiendesign. Wir untersuchten 81 Proben auf gDNA und 56 übereinstimmende Proben auf cDNA im Längsschnitt zu den Zeiten 0, 6 und 24 Monaten von insgesamt 27 pädiatrischen Empfängern, die eine Grundschulung erhieltenNiereTransplantation. Die Probanden in dieser Studie stammen aus einer klinischen Studie (SNSO1 multizentrische Studie), in der die Probanden randomisiert (1:1) einem traditionellen niedrig dosierten Steroid-basierten Immunsuppressionsschema (Steroide, standardmäßige Daclizumab-Induktion bis zum zweiten Monat nach der Transplantation, und Erhaltungs-Immunsuppression mit Tacrolimus (Prograf, Astellas Pharma) und MMF (CellCept, Hoffman-La Roche) oder einem steroidfreien Immunsuppressionsregime (verlängerte Daclizumab-Induktion bis zum sechsten Monat nach der Transplantation, Tacrolimus und MMF). Eingeschrieben nach IRB-Zulassung und Einwilligung nach Aufklärung In dieser Studie erhielten 14 Patienten ein Steroidvermeidungsschema, während 13 ein Steroid-basiertes immunsuppressives Regime erhielten53 und keiner dieser Patienten erhielt eine Immunsuppression vor der Transplantation, da dies eines der Ausschlusskriterien war bestand aus drei Impulsen mit intravenösem Kortikosteroid (10 mg/kg) und einer Intensivierung der Immunsuppression zu Studienbeginn.
Alle in der Studie verwendeten Proben hatten eine zugehörige serielle Allotransplantat-Biopsie, die von einem zentralen Pathologen unter Verwendung halbquantitativer histologischer Bewertungen gelesen wurde. Klinische akute Abstoßung wurde als akute Abstoßungsepisode definiert, die mit einer Funktionsstörung des Transplantats verbunden war, basierend auf einem Anstieg des Serumkreatinins um mehr als 10 Prozent gegenüber den Ausgangswerten, und bestätigt durch eine zentrale pathologische Ablesung der Biopsien gemäß der aktualisierten Banff-Klassifikation23,24. Chronische Allograft-Verletzungen wurden unter Verwendung des Chronic Allograft Damage Index (CADI)-Score definiert. Die Patienten wurden in drei klinische Endpunkte eingeteilt, die durch CADI-Score und Abstoßungsepisoden definiert wurden. Non-Progressors (NP) hatten einen niedrigen, nicht inkrementellen CADI-Score bei drei seriellen Biopsien über 2 Jahre, ohne akute Abstoßung, Progressive ohne Abstoßung (PNR) hatten einen höheren CADI Score auf ihren seriellen Biopsien über 2 Jahre und inkrementell über die Zeitpunkte ohne Abstoßung und Progressoren mit Abstoßung (PR) hatten inkrementell hohe CADI-Scores auf ihren seriellen Biopsien über 2 Jahre mit Abstoßungsepisoden. Diese Patienten wurden sehr sorgfältig aus einer größeren Kohorte von 120 Patienten ausgewählt, die hinsichtlich demografischer Variablen und für alle NP und PNR übereinstimmen, um keine Anzeichen einer Entzündung bei der Biopsie oder einer subklinischen Verletzung zu haben, gemessen an fehlenden spenderspezifischen Antikörpern. Keiner hatte HLA oder ein haploidentisches Transplantat, da dies ein Ausschlusskriterium für die Aufnahme war54. Alle Proben wurden zwischen 2004 und 2006 aus 12 verschiedenen pädiatrischen Transplantationsprogrammen in den USA nach vom IRB genehmigten Protokollen entnommen. Die Studie wurde auch vom Human Research Protection Program (HRPP) der University of California, San Francisco, und der Stanford University genehmigt, um eine Analyse von Biobankproben zu ermöglichen. Alle Patienten/Erziehungsberechtigten gaben ihre informierte Zustimmung zur Teilnahme an der Studie unter vollständiger Einhaltung der Deklaration von Helsinki. Die berichteten klinischen und Forschungsaktivitäten stehen im Einklang mit den Grundsätzen der Erklärung von Istanbul, wie sie in der Erklärung von Istanbul über Organhandel und Transplantationstourismus dargelegt sind.
Isolierung von gDNA und RNA. Blutproben (4,5 ml) wurden in einem 5-ml-Röhrchen mit rotem Verschluss gesammelt und 30 min lang bei Raumtemperatur inkubiert, bis sich das Gerinnsel gebildet hatte. Die Probe wurde dann bei 2000 × g für 5 min unter Verwendung eines Schwingbecherrotors zentrifugiert. Die obere Serumschicht wurde dann in ein anderes Kryoröhrchen überführt und das Gerinnsel bis zur Verwendung im selben Röhrchen bei –80 Grad gelagert. Genomische DNA aus Vollblutgerinnseln wurde unter Verwendung von Clotspin Baskets und dem Gentra PuregeneBlood Kit (Qiagen, Valencia, CA) extrahiert.
Für die RNA-Extraktion ausNiereNadelbiopsie (Qiagen, Valencia, CA) und bei –80 Grad gelagert; Gesamt-RNA wurde unter Verwendung einer Mastermischung aus 790 &mgr;l TRIzol und 10 &mgr;l Glykogen extrahiert. Gewebeproben wurden homogenisiert, bei 15 bis 25 Grad für 5 min inkubiert und 160 &mgr;l Chloroform wurden zur Phasentrennung zugegeben. Die Mischung wurde erneut bei 25 Grad für 2 Minuten inkubiert, gefolgt von einer Zentrifugation bei 4 Grad, und für die RNA-Extraktion unter Verwendung des RNeasy Micro Kits (Qiagen Katalog Nr. 4004) verwendet. RNA-Menge und -Integrität wurden mit dem NanoDrop ND-2000 UV-Vis-Spektrophotometer von Thermo Scientific bzw. dem Agilent Bioanalyzer bestimmt.
B-Zell-Sequenzierung. Genomische DNA-Matrizen-PCR-Reaktionen wurden hergestellt
aus 1{17}}0 ng gDNA-Aliquots zur Erstellung von sechs unabhängigen barcodierten Bibliotheken pro Probe. Multiplex-Primer zu den IgH J- oder FR1- oder FR2-Framework-Regionen gemäß dem BIOMED-2-Design wurden verwendet55. 10-Nukleotid-„Barcodesequenzen“ in den Primern wurden verwendet, um die Probenidentität und die Identität der replizierten Bibliothek für jede PCR-Reaktion anzuzeigen. PCR wurde mit AmpliTaq Gold (Roche) Polymerase mit dem folgenden Programm durchgeführt: 94 Grad für 5 min; 35 Zyklen von (94 Grad für 30 s, 60 Grad für 45 s, 72 Grad für 90 s); und Endverlängerung bei 72 Grad für 10 min. Eine zweite PCR-Reaktion wurde durchgeführt, um sicherzustellen, dass die Bibliotheken vor der Gelreinigung und Sequenzierung nicht bis zur Sättigung amplifiziert wurden. Insgesamt dienten 0,4 ul jedes ersten PCR-Produkts als Matrize für die zweite PCR-Reaktion unter Verwendung externer Primer, die für die 454 Linkersequenzen spezifisch sind; die verstärkung wurde mit dem programm durchgeführt: 94 grad für 15 min, 12 zyklen (94 grad für 30 s, 60 grad für 45 s, 72 grad für 90 s) und abschließende verlängerung bei 72 grad für 10 min. Die Fehlerrate des AmpliTaq Gold sollte eine minimale Auswirkung auf die Identifizierung klonal verwandter Sequenzen oder die Schätzung somatischer Mutationsraten in Sequenzen haben, wie an anderer Stelle diskutiert56. cDNA wurde aus insgesamt 300 ng RNA mit Priming durch zufällige Hexamere synthetisiert. Die Matrizen wurden durch PCR unter Verwendung von Biomed IGHV-Primern in Gerüst 1 (FR1) und Isotyp-spezifischen Primern, die sich im ersten Exon der konstanten Regionen befinden, amplifiziert. Diese Primer18,57 kodierten auch ungefähr die Hälfte der Illumina-Linkersequenzen, die für die Clustererzeugung und Sequenzierung auf dem MiSeq-Instrument benötigt werden. Die Probenidentität wurde durch Acht-Nukleotid-Multiplex-Identifikator-Barcodes in jedem Primer kodiert. Für die Erkennung von Illumina-Clustern wurden vier randomisierte Nukleotide in den Primern unmittelbar nach der Illumina-Linkersequenz in den Primern der konstanten Region kodiert. Jeder Antikörper-Isotyp für jede Probe wurde in einer separaten PCR-Reaktion amplifiziert, um die Bildung von chimären Kreuz-Isotyp-PCR-Produkten zu verhindern. Die PCR wurde mit AmpliTaq Gold (Roche) gemäß den Anweisungen des Herstellers durchgeführt und verwendete ein Programm von 94 Grad für 7 Minuten, 35 Zyklen von (94 Grad für 30 Sekunden, 58 Grad für 45 Sekunden, 72 Grad für 120 Sekunden) und abschließend Verlängerung bei 72 Grad für 10 min. Ein zweiter PCR-Schritt wurde verwendet, um den verbleibenden Teil der Illumina-Linker zu den Amplifikaten hinzuzufügen, und wurde mit dem Qiagen Multiplex-PCR-Kit (Qiagen) gemäß den Anweisungen des Herstellers durchgeführt, wobei 0,4 Mikroliter des ersten PCR-Produkts als Matrize in a verwendet wurden 30 Mikroliter Reaktion. Das PCR-Programm für den zweiten PCR-Schritt war 94 Grad für 15 Minuten, 12 Zyklen von (94 Grad für 30 Sekunden, 60 Grad für 45 Sekunden, 72 Grad für 90 Sekunden) und abschließende Verlängerung bei 72 Grad für 10 Minuten. Die Produkte jeder PCR-Reaktion wurden in geschätzten äquimolaren Mengen gepoolt, auf Agarosegelen einer Elektrophorese unterzogen und mit QIAquick-Kits (Qiagen) gelextrahiert. Die Hochdurchsatz-Sequenzierung von genomischen DNA-Matrizenbibliotheken wurde auf der 454-Plattform (Roche) unter Verwendung von Titanchemie durchgeführt. Die cDNA-Bibliothekssequenzierung wurde auf einem Illumina MiSeq-Instrument unter Verwendung von 600--Zyklus-Sequenzierungskits durchgeführt. Eine vollständige Liste der Primer, die mit MiSeq (M154 und M155) und 454 Titanium (T7) verwendet werden, ist in Supplementary Data 1 enthalten.
Sequenzierungs-Reads wurden wie folgt verarbeitet: Paired-End-Reads wurden mit FLASH58 zusammengeführt, wonach die Sequenzen demultiplext und von Barcodes und IGHV-Primersequenzen getrimmt wurden. Die V-, D- und J-Regionen und V-D- (N1), D-J- (N2) Übergänge wurden mit dem Alignment-Programm IgBLAST59 identifiziert. Sequenzen wurden gefiltert, um Nicht-IGH-Artefakte, Sequenzen mit V-Gen-Insertion oder -Deletionen, chimäre Sequenzen und nicht-funktionelle Sequenzen zu entfernen. Auf Stichprobenebene haben wir diejenigen mit ausgeschlossen<100 clones="" (defined="" by="" same="" v="" and="" j="" segments,="" same="" cdr3="" length,="" and="" 90%="" nucleotide="" identity)="" as="" a="" control="" for="" bad="" quality="" samples.="" after="" quality="" control,="" for="" gdna,="" we="" had="" complete="" longitudinal="" data="" for="" 69="" samples="" at="" times="" 0,="" 6,="" and="" 24="" with="" a="" total="" number="" of="" 327,703="" reads="" (mean="" 4045="" per="" sample).="" for="" cdna,="" we="" had="" complete="" data="" for="" 55="" matched="" samples,="" although="" no="" time="" 0="" samples="" were="" further="" available.="" in="" this="" case,="" we="" had="" isotype-="" specific="" information="" (1,773,330="" reads="" for="" igd="" (31,667="" per="" sample),="" 1,708,227="" reads="" for="" igm="" (30,504="" per="" sample),="" 973,444="" reads="" for="" iga="" (17,383="" per="" sample),="" 139,7345="" reads="" for="" igg="" (24,953="" per="" sample),="" and="" 29,000="" reads="" for="" ige="" (5,178="" per="">
Diversitätsanalyse. Die Vielfalt wird anhand des Artenreichtums unter Berücksichtigung der Anzahl der Klone pro Probe gemessen. Dieses Maß berücksichtigt nicht die Häufigkeit jeder Art, daher haben wir auch die Shannon-Entropie (H) verwendet, um die Bereitstellung von Diversität zu messen
Informationen über die Größenverteilung der Arten in der Population. H ist definiert als:
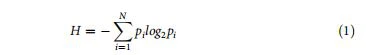
wobei N die Anzahl einzigartiger Klone und pi die Häufigkeit von Klon i ist. H reicht von 0 (Probe mit nur einem Klon) bis Hmax ¼ log2N (Probe mit einer gleichmäßigen Verteilung von Klonen).
Dann verwendeten wir ein allgemeines lineares Modell, um den Zusammenhang zwischen Reichhaltigkeit und Entropie mit dem klinischen Ergebnis zu den verschiedenen Zeitpunkten zu finden. Wir haben dieses Modell durch alle in Tabelle 1 gezeigten verfügbaren klinischen Variablen angepasst, um sicherzustellen, dass eines der Merkmale des Patienten ein verwirrender Faktor war
Um die Längskomponente der Daten zu modellieren, haben wir ein lineares Modell mit gemischten Effekten unter Berücksichtigung eines bedingten Wachstumsmodells angewendet, wie in der ergänzenden Abb. 10 gezeigt. Um dieses Modell anzuwenden, haben wir das lme4-Paket in R unter Berücksichtigung der Wechselwirkung zwischen klinischem Ergebnis und Zeit bis verwendet Finden Sie Assoziationen mit Reichtum und Vielfalt, wobei die Zeit ein zufälliger Effekt ist.
Um der Tatsache Rechnung zu tragen, dass Diversitätsmaße durch das Problem fehlender Arten (nur ein Bruchteil von Milliarden Zellen in einem Repertoire sind vertreten) und Sequenzierungs- und experimentelle Fehler beeinträchtigt werden können, haben wir zusätzlich zur vollständigen Datenanalyse zwei Strategien durchgeführt. Zuerst haben wir das Recon-Tool (Rekonstruktion geschätzter Klone aus beobachteten Zahlen)29 verwendet, um das Problem fehlender Arten zu lösen. Recon ist eine modifizierte Maximum-Likelihood-Methode, die die Gesamtdiversität eines Repertoires aus Messungen an einer Probe ausgibt. Recon gibt genaue und robuste Schätzungen einer Reihe von Diversitätsmaßen aus, einschließlich Reichhaltigkeit und Entropie, was robuste Vergleiche der Diversität zwischen Individuen ermöglicht. Zweitens haben wir eine Downsampling-Strategie durchgeführt, bei der eine zufällige Teilmenge von Lesevorgängen für jede Probe gleich der kleinsten Sequenzierungsgröße genommen wurde, gefolgt von der Neuberechnung der B-Zell-Klone, um sie an die Sequenzierungstiefe anzupassen und mögliche experimentelle Fehler zu beheben. Für gDNA gibt es Proben mit sehr niedrigen Reads (< 1000),="" und="" um="" zu="" vermeiden,="" dass="" viele="" sequenzen="" und="" die="" realität="" der="" daten="" verloren="" gehen,="" haben="" wir="" insgesamt="" neun="" proben="" ausgeschlossen,="" bei="" denen="" dies="" der="" fall=""><1000 reads.="" in="" the="" case="" of="" cdna,="" this="" was="" not="" necessary.="" we="" generated="" ten="" random="" subsamples="" to="" account="" for="" possible="" stochastic="" effects="" and="" performed="" the="" diversity="" analysis="" at="" each="" time="" point="" and="" the="" longitudinal="" data="" analysis="" on="" the="" mean="" value="" of="" ten="" independently="" downsampled="" diversity="">
Netzwerkanalyse. Der Netzwerkgenerierungsalgorithmus ist dem zuvor definierten sehr ähnlich31. Kurz gesagt repräsentiert jeder Scheitelpunkt eine B-Zellsequenz, wobei die Größe durch alle identischen Sequenzen definiert wird. Kanten werden unter Verwendung der Klondefinition (gleiche V- und J-Segmente, gleiche CDR3-Länge und 90-prozentige Nukleotididentität zwischen CDR3s) berechnet, und Cluster repräsentieren jeden Klon im Repertoire. Die Analyse wurde mit dem Grafikpaket in R durchgeführt, wobei das Layout_mit_graphopt-Option zum Generieren des Diagramms verwendet wurde.
Um das Netzwerk zu quantifizieren, haben wir den Gini-Index für Scheitelpunktgröße und Clustergröße berechnet. Der Gini-Index ist ein Maß für die Ungleichmäßigkeit, das häufig zur Messung der Vermögensverteilung verwendet wird. Es misst die Ungleichheit zwischen Werten der Häufigkeitsverteilung. Wir haben die Gini-Funktion aus einem Paket in R verwendet, um den Gini-Koeffizienten für die Knotengrößen- und Clustergrößenverteilung zu berechnen. Ein Gini-Koeffizient von Null drückt vollkommene Gleichheit aus und ein Gini-Koeffizient von 1 drückt maximale Ungleichheit aus.
Klonale Analyse. Um die spezifischen Klone im Zusammenhang mit klinischen Ergebnissen zu untersuchen, haben wir eine Matrix mit allen Klonen erstellt, die in mehr als einer Probe (Gesamtzahl=118, 223) von allen Proben zu jedem Zeitpunkt vorhanden sind. Wir untersuchten dann die Assoziation mit dem klinischen Ergebnis jedes einzelnen Klons, indem wir eine Variable pro Klon als vorhanden/nicht vorhanden definierten. Schließlich haben wir Fishers exakten Test angewendet, um die Signifikanz in den 2 × 3-Tabellen für jeden Klon zu jedem Zeitpunkt zu berücksichtigen. Wir haben auch die Persistenzklone untersucht, die durch die Klone definiert sind, die in jedem Individuum zu mehr als einem Zeitpunkt vorhanden sind. Um Unterschiede durch das klinische Ergebnis zu berücksichtigen, haben wir dann ein lineares Modell angewendet, das als abhängige Variable die Anzahl der Klone (um Unterschiede in der Persistenz zu messen) und die Anzahl der Zählungen jedes Klons (um die klonale Expansion zu messen) und das klinische Ergebnis als definiert ein unabhängiger Prädiktor.
IGHV-Gennutzungsanalyse. Um die IGHV-Gene zu untersuchen, bewerteten wir die IGHV-Gennutzung pro Probe als die Häufigkeit, mit der jedes Gen verwendet wird, normalisiert durch die Anzahl der Klone, um eine Überrepräsentation bestimmter IGHV-Gene zu vermeiden. Für die statistische Analyse haben wir die Gene mit sehr geringer Expression (IGHV-Nutzung/Klone < {{0}}.05)="" in="" mindestens="" 10="" prozent="" der="" proben="" herausgefiltert.="" insgesamt="" analysierten="" wir="" 27="" ighv-gene,="" die="" 63="" proben="" entsprechen.="" dann="" wendeten="" wir="" ein="" lineares="" modell="" an,="" um="" die="" gene="" zu="" finden,="" die="" zu="" jedem="" zeitpunkt="" mit="" dem="" klinischen="" ergebnis="" assoziiert="" waren,="" und="" korrigierten="" diese="" ergebnisse="" durch="" multiples="" testen="" unter="" verwendung="" von="" benjamini="" und="" hochberg="" fdr="">< 0,05.="" wir="" haben="" dieses="" modell="" durch="" alle="" in="" tabelle="" 1="" gezeigten="" verfügbaren="" klinischen="" variablen="" angepasst,="" um="" sicherzustellen,="" dass="" eines="" der="" merkmale="" des="" patienten="" ein="" verwirrender="" faktor="">
Zusammenfassung der Berichterstattung. Weitere Informationen zum Forschungsdesign finden Sie in der mit diesem Artikel verlinkten Nature Research Reporting Summary.

Verweise
1.Cai, J. & Terasaki, PI Antikörperüberwachung nach Transplantation und HLA 1. (Antikörper-Epitop-Identifikation. Curr.Opin.Immunol. 20,602-606(2008).
2. Sigdel, TKet al. Nicht-HLA-Antikörper gegen immunogene Epitope sagen die Entwicklung einer chronischen renalen Transplantatverletzung voraus.J. Bin. Soc. Nephrol.23,750-763 (2012).
3. Li, L. et al. Kompartimentelle Lokalisation und klinische Relevanz von MICA-Antikörpern nach Nierentransplantation. Transplantation 89,312-319(2010).
4. Lamb, KE, Lodhi, S. & Meier-Kriesche, H.-U. Langfristiges Überleben von allogenen Nierentransplantaten in den Vereinigten Staaten: Eine kritische Neubewertung. Am.J. Transplantation. 11, 450-462(2011).
5. Das Wissenschaftliche Register der Transplantatempfänger. Verfügbar unter: https://rtr. transplant.hrsa.gov/annual_reports/2012/Default.aspx.(Zugriff:24. Mai 2018)Pineda, S. et al. Neuartige Nicht-Histokompatibilitäts-Antigen-Mismatched-Varianten
6. Verbesserung der Fähigkeit zur Vorhersage des Antikörper-vermittelten Abstoßungsrisikos bei Nierentransplantationen. Vorderseite. Immunol. 8,1687 (2017).
7. Valuiskikh, A. Baldwin, WM & Fairchild, RL. Jüngste Fortschritte und neue Perspektiven bei der Untersuchung von T-Zell-Antworten auf Allotransplantate. Am.J. Transplantation.10, 117-1125 (2010).
8. Zarkhin, V, Chalasani, G. & Sarwal, MM Das Yin und Yang von B-Zellen bei Transplantatabstoßung und -toleranz. Transplantation. Rev.24,67-78(2010).
9. Georgiou, G.et al. Das Versprechen und die Herausforderung der Hochdurchsatz-Sequenzierung des Plus-Antikörper-Repertoires. Nat. Biotechnol.32,158-168(2014).
10. Schroeder, HW Ähnlichkeit und Divergenz in der Entwicklung und Expression des Antikörper-Repertoires von Maus und Mensch. Entwickler Komp. Immunol. 30,119-135(2006).
11. Yaari, G. & Kleinstein, SH Praktische Richtlinien für die B-Zell-Rezeptor-Repertoire-Sequenzierungsanalyse. Genom Med.7,121 (2015).
12. Shugay, M. et al. VDJtools: Vereinheitlichende Nachanalyse von T-Zell-Rezeptor-Repertoires. PLOS-Berechnung. Biol.11, e1004503 (2015).
13. Alachkar, H.et al. Quantitative Charakterisierung des T-Zell-Repertoires und Biomarker bei der Abstoßung von Nierentransplantaten. BMC Nephrol.17,181(2016). 14. Morris, H. et al. Tracking von Spender-reaktiven T-Zellen: Hinweise auf klonale Deletion bei toleranten Nierentransplantationspatienten. Wissenschaft. Übers. Med.7,272ral0 (2015).
15. Dziubinau, M. et al. Die TCR-Repertoireanalyse durch Next-Generation-Sequencing ermöglicht eine komplexe Differentialdiagnose von T-Zell-assoziierten Pathologien. Bin. J.Transplantation.13,2842-2854 (2013).
16. Palanichamy, A. et al. Immunglobulin-class-switched B-Zellen bilden bei Multipler Sklerose eine aktive Immunachse zwischen ZNS und Peripherie. Wissenschaft. Übers. Med.6, 248ra106-248ra106 (2014).
17. Strauli, NB & Hernandez, RD Statistische Inferenz einer konvergenten Antikörper-Repertoire-Antwort auf Influenza-Impfstoff. Genom Med. 8,60 (2016).
18. Roskin, KM et al. IgH-Sequenzen bei gemeinsamer variabler Immunschwäche zeigen eine veränderte Entwicklung und Selektion von B-Zellen. Wissenschaft. Übers. Med.7,302ra135 (2015).
19. Massart, A., Ghisdal, L., Abramowicz, M. & Abramowicz, D. Operative Toleranz bei der Nierentransplantation und damit verbundene Biomarker. Klin. Erw. Immunol.189,138-157(2017).
20. Beausang, JFet al.B-Zell-Repertoires bei HLA-sensibilisierten Nierentransplantationskandidaten, die sich einer Desensibilisierungstherapie unterziehen.J. Übers. Med.15, 9 (2017).
21. Ferdmann, J. et al. Expansion und somatische Hypermutation von B-Zell-Klonen in abgelehnten menschlichen Nierentransplantaten. Transplantation 98, 766-772 (2014).
22. Vollmers, C. et al. Überwachung der pharmakologisch induzierten Immunsuppression durch Sequenzierung des Immunrepertoires zum Nachweis einer akuten Allotransplantatabstoßung bei Herztransplantationspatienten: Eine Proof-of-Concept-Diagnosegenauigkeitsstudie.PLOS Med. 12,e1001890 (2015).
23. Solez, K. et al. Banff'05 Meeting Report: Differentialdiagnose chronischer Allotransplantat-Verletzungen und Beseitigung chronischer Allotransplantat-Nephropathie (CAN). Bin. J. Transplant.7,518-526(2007). Immunsuppression bei Nierentransplantation: Ist es an der Zeit, sie als Standardtherapie in Betracht zu ziehen? Kidney Int.76, 825-830 (2009).
28. Legendre, C. et al. Drei-Jahres-Ergebnisse bei Nierentransplantationspatienten, die randomisiert einer steroidfreien Immunsuppression oder einem Steroidentzug mit magensaftresistent beschichtetem Mycophenolat-Natrium und Cyclosporin zugeteilt wurden: die Infinity-Studie. J. Transplantation.2014,1-8(2014).
29. Kaplinsky, J. & Arnaout, R. Robuste Schätzungen der gesamten Immunrepertoire-Diversität aus Hochdurchsatzmessungen an Proben. Nat. Commun.7, 11881(2016).
30. Stern, JNHet al. B-Zellen, die das Multiple-Sklerose-Gehirn bevölkern, reifen in den drainierenden zervikalen Lymphknoten. Wissenschaft. Übers. Med.6,248ra107 (2014).
31. Bashford-Rogers, RJMet al. Netzwerkeigenschaften, die aus der Tiefensequenzierung menschlicher B-Zell-Rezeptor-Repertoires stammen, beschreiben B-Zell-Populationen. Genomres.23, 1874-1884 (2013).
32. Sarwal, Metal. Molekulare Heterogenität bei akuter renaler Transplantatabstoßung
identifiziert durch DNA-Microarray-Profiling. N.Engl.J. Med.349,125-138(2003). 33. Zarhin, V., Lovelace, PA, Li, L., Hsieh, S.-C. & Sarwal, MM Phenotypische Bewertung von B-Zell-Untergruppen nach Rituximab zur Behandlung der akuten Abstoßung von Nierentransplantaten bei pädiatrischen Empfängern. Transplantation 91, 1010-1018 (201).
34. Clatworthy, MR& Targeting, B. Zellen und Antikörper bei der Transplantation.Amm. J. Transplantation.11, 1359-1367 (2011).
35. Dijke, EIet al. Bcells in transplantation.J. Herz-Lungen-Transplantation.35,704-710(2016).
36. Nankivell, BJ & Kuypers, DRDiagnose und Prävention von chronischem Verlust von Nierentransplantaten. Lancet 378,1428-1437(2011).
37. Patin, E. et al. Die natürliche Variation der Parameter angeborener Immunzellen wird vorzugsweise durch genetische Faktoren bestimmt. Nat.Immunol.19,302-314(2018). 38. Liston, A. & Goris, A. Die Ursprünge der Vielfalt in der menschlichen Immunität.Nat. Immunol. 19,209-210(2018).
39. Meier-Kriesche, H.-U, Schold, JD, Srinivas, TR& Kaplan, B. Fehlende Verbesserung des Überlebens von Nierentransplantaten trotz eines deutlichen Rückgangs der akuten Abstoßungsraten in der jüngsten Zeit.Am.J. Transplantation.4, 378-383 (2004).
40. Keith, DS, Vranic, G. & Nishio-Lucar, A. Transplantatfunktion und mittelfristige Ergebnisse von Nierentransplantationen verbesserten sich im letzten Jahrzehnt: Analyse der Nierentransplantationsdatenbank der Vereinigten Staaten. Transplantation. direkt 3,el66 (2017).
41. Bomben, R. et al. Die Expression mutierter IGHV3-23-Gene bei chronischer lymphatischer Leukämie identifiziert eine Krankheitsuntergruppe mit besonderen klinischen und biologischen Merkmalen. Klin. Krebsres. 16,620-628(2010).
42. Levinson, AI, Kozlowski, L, Zheng, Y. & Wheatley, L. B-cell superantigens: definition and potential impact on the immune response.J. Clin.Immunol.15, 26S-36S(1995.
43. Silverman, GJ & Goodyear, CSA model B-Cell superantigen and the immunobiology of B lymphocytes. Clin. Immunol.102,117-134(2002).
44. Silverman, GJ & Goodyear, CSConfounding B-Zell-Abwehr: Lehren aus einem Staphylokokken-Superantigen. Nat. Rev. Immunol.6,465-475(2006). 45. Cheng, J. et al. Ektopische B-Zell-Cluster, die transplantierte menschliche Nieren infiltrieren, sind klonal. Proz. Natl Acad. Wissenschaft. 108, 5560-5565 (2011).
46. Grover, RKet al. Das costimulatorische Immunogen LPS induziert die B-Zell-Klone, die transplantierte menschliche Nieren infiltrieren. Proz. Natl Acad. Wissenschaft. USA 109, 6036-6041(2012).
47,Modena,BDet al. Veränderungen der Mikrobiompopulationen im Urin korrelieren bei Nierentransplantationen mit interstitieller Fibrose und tubulärer Atrophie, die in frühen Überwachungsbiopsien dokumentiert wurden. Bin. J. Transpl.17, 712-723 (2017).
48. Chen, K. & Cerutti, A. Neue Einblicke in das Rätsel des Immunglobulins D. Immunol. Rev. 237, 160-179 (2010).
49. Chen, K. et al. Immunglobulin D verbessert die Immunüberwachung, indem es antimikrobielle, entzündungsfördernde und B-Zell-stimulierende Programme in Basophilen aktiviert. Nat. Immunol. 10, 889-898(2009).
50. Mack, M. & Rosenkranz, AR Basophile und Mastzellen bei Nierenverletzung. KidneyInt.76, 1142-1147 (2009).
51. Nixon, DFet al. Molekulare Verfolgung eines menschlichen Immunschwächevirus
nef-spezifischer zytotoxischer T-Zell-Klon zeigt eine Persistenz der klonspezifischen T-Zell-Rezeptor-DNA, aber nicht der mRNA nach einer frühen antiretroviralen Kombinationstherapie.Immunol. Lett.66,219-228(1999).
52. Dharnidharka, VR, Fiorina, P. & Harmon, WEKidney transplantation in children.N.Engl. J.Med. 371,549-558(2014).
53. Sarwal, M. Met. al. Die vollständige Vermeidung von Steroiden ist bei Kindern mit Nierentransplantationen wirksam und sicher: Eine multizentrische randomisierte Studie mit dreijähriger Nachbeobachtung. Am.J.Transplant.12,2719-2729(2012).
24. Solez, K. et al. Banff 07 Klassifikation der Nierentransplantatpathologie: Aktualisierungen und zukünftige Richtungen. Am.J.Transplant.8, 753-760 (2008).
54. Li, L. et al. steroidfreie Immunsuppression seit 1999:129 pädiatrische Nierentransplantationen mit nachhaltigem Transplantat- und Patientennutzen. Am.J. Transpl. 9, 1362-1372(2009).
25. Chaudhuri, A. et al. Die klinische Auswirkung der humoralen Immunität bei der pädiatrischen Nierentransplantation.J. Bin. Soc.Nephrol.24, 655-664 (2013).






