Krankheitsmodellierung mit Nierenorganoiden
Sep 01, 2023
Abstrakt:NierenerkrankungenOft fehlt es an optimalen Behandlungen, was jedes Jahr zu Millionen von Todesfällen führt. Daher werden geeignete Modellsysteme für die Untersuchung entwickeltmenschliche Nierenerkrankungist von größter Bedeutung. Einige der vielversprechendsten menschlichen Nierenmodelle sind Organoide oder kleine organähnliche Gewebekollektive, die aus vom Menschen induzierten pluripotenten Stammzellen (hiPSCs) abgeleitet sind. Sie ähneln jedoch eher einem ersten Trimesterfetale Niereals eine erwachsene Niere. Daher sind neue Strategien erforderlich, um ihre Reife voranzutreiben. Sie haben ein großes Potenzial für die Krankheitsmodellierung und schließlich für die Hilfstherapie, wenn sie die Reife einer Krankheit erreichen könnenerwachsene Niere. In diesem Aufsatz werden wir den aktuellen Stand von Nierenorganoiden im Hinblick auf ihre Ähnlichkeit mit der menschlichen Niere und ihre bisherige Verwendung als Krankheitsmodellierungssystem diskutieren. Wir werden dann mögliche Wege besprechen, um das voranzutreibenReife der NiereOrganoide, die einer erwachsenen Niere entsprechen, um eine genauere Modellierung menschlicher Krankheiten zu ermöglichen.
Schlüsselwörter: Organoide;Niere; Entwicklung; Metanephros; Harnleiter; Tubulus; Chip; Nephrologie; Krankheitsmodellierung

KLICKEN SIE HIER, UM CISTANCHE FÜR CNI-BEHANDLUNGEN ZU ERHALTEN
1. Einleitung
Bis vor kurzem wurden menschliche Krankheiten auf zwei Arten modelliert: mit Tieren oder mit zweidimensionalen Zellkulturen. Tiermodelle ermöglichen die Untersuchung von Krankheitsverläufen und der Arzneimittelentwicklung in ganzen Organismen, sie berücksichtigen jedoch nicht die genetische und anatomische Ausstattung des Menschen. Andererseits ermöglicht die menschliche Zellkultur Wissenschaftlern die Untersuchung menschenspezifischer Krankheitsmechanismen und die Bewertung von Behandlungen bis zu einer großen und präzisen molekularen Tiefe. Allerdings rekapituliert die Zellkultur nicht die komplexe dreidimensionale Struktur und Physiologie eines Organs.
Menschliche Organoide sind vereinfachte Versionen menschlicher Organe mit realistischer dreidimensionaler Mikroanatomie und Funktionen auf Organebene (z. B. Tränenproduktion bei Milchorganoiden und Haarwachstum bei Hautorganoiden) [1,2]. Durch Selbstorganisationsprozesse werden sie in vitro aus Gewebezellen oder pluripotenten Stammzellen gewonnen. Induzierte pluripotente Stammzellen (iPSCs), 2008 von Takahashi und Yamanaka erfunden, sind die beliebtesten Zellen für die Organoidbildung [3]. Dies ist auf mehrere überzeugende Vorteile zurückzuführen, die iPSCs bieten. Erstens stellen sie eine unbegrenzt erneuerbare Zellquelle dar und können sich in mehrere Zelltypen differenzieren. Noch wichtiger ist, dass sie die zugrunde liegende genetische Zusammensetzung von Patienten darstellen. Daher können von Patienten stammende menschliche iPSCs (hiPSCs) verwendet werden, um Krankheiten anhand von Organoiden auf individueller Ebene zu untersuchen, was Fortschritte in der personalisierten Medizin ermöglicht. Bisher wurden Organoidmodelle verschiedener menschlicher Organe wie des Herzens und des Gehirns zur Untersuchung von Krankheiten verwendet. In diesem Aufsatz konzentrieren wir uns auf Nierenorganoide und diskutieren, wie sie zur Modellierung der menschlichen Niere und der damit verbundenen Krankheiten, zum Screening auf Arzneimitteltoxizität und möglicherweise zur Ergänzung der Nierenfunktion verwendet werden können.

Nierenerkrankungen betreffen 10 % der Weltbevölkerung [4]. Obwohl die zugrunde liegende genetische Ursache für viele Formen von Nierenerkrankungen identifiziert wurde, gibt es keine optimalen Therapien für deren Behandlung. Diese unglückliche Situation spiegelt das Fehlen von In-vitro-Modellsystemen wider, die menschliche Nierenerkrankungen für die gezielte therapeutische Entwicklung rekapitulieren. Nierenorganoide bieten eine menschenbasierte, personalisierbare 3-D-Forschungsplattform zur Untersuchung genetischer Nierenerkrankungen, Nierenschäden und Arzneimitteltoxizität. Neben seiner Fähigkeit, als Modellsystem zu dienen, besitzt ein Nierenorganoid das Potenzial, die Transplantationsmedizin voranzutreiben. Um sein Potenzial in beiden Bereichen zu maximieren, muss das Nierenorganoid daher der Struktur und Funktion der erwachsenen menschlichen Niere ähneln. Hier werden wir den aktuellen Stand des aus pluripotenten Zellen gewonnenen menschlichen Nierenorganoids, seine möglichen Verwendungsmöglichkeiten und Verbesserungsmöglichkeiten besprechen.
2. Die menschliche Niere vs. Nierenorganoide
HiPSCs dienen als Stellvertreter für embryonale PSCs. Die Bildung eines Nierenorganoids aus hiPSCs erfordert daher die Replikation der menschlichen embryonalen Nierenentwicklung. Im Folgenden werden wir untersuchen, wie sich das Nierenorganoid entwickelt, und es mit der menschlichen Niere vergleichen.
2.1. Entwicklung der menschlichen Niere
Während der Embryonalentwicklung wird das Blut in drei verschiedenen Phasen gefiltert. In der ersten Phase entwickelt sich im 4- Wochen alten menschlichen Embryo eine Struktur namens Pronephros, die bis etwa zur fünften Woche Blut im Halsbereich verarbeitet [5]. Als nächstes bilden sich die Mesonephrose im Brustbereich des Embryos und filtern das Blut vom Beginn der fünften Woche bis etwa zur zehnten Woche der Embryonalentwicklung. Während der Mesonephros das Blut filtert, ist das letzte Filtersystem, das schließlich zum Blut wirderwachsene Niere, beginnt sich zu bilden (Abbildung 1). Es besteht aus den folgenden zwei Teilen: dem metanephrischen Mesenchym und der Ureterknospe. Das metanephrische Mesenchym bildet alle Teile des Nephrons mit Ausnahme des Sammelrohrs, während die Ureterknospe das Sammelrohr bildet. Diese Strukturen durchlaufen einen reziproken Induktionszyklus, bei dem das metanephrische Mesenchym und die Ureterknospe das gegenseitige Wachstum anregen und verschmelzen, wodurch eine Struktur namens Metanephros entsteht. Die neu gebildeten Metanephroi filtern das Blut von den Beckenästen bis hinunter in die Beckenregion. Gleichzeitig gabelt sich die Ureterknospe und verzweigt sich weiter, um innerhalb der Niere viele Sammelrohre zu bilden [6,7]. Anschließend steigen diese verschmolzenen metanephrischen Strukturen in die Bauchregion des Embryos auf, während dieser sich entwickelt, und sorgen für die Blutversorgung aus der primitiven Aorta. Diese Prozesse sind in Abbildung 1 zusammengefasst. Es ist wichtig zu beachten, dass metanephrische Mesenchym- und Ureterknospenzellen primitiv sind und somit ein multipotentes Potenzial behalten, während adulte differenzierte Nierenzellen ihrer jeweiligen Abstammungslinie verpflichtet sind [8].
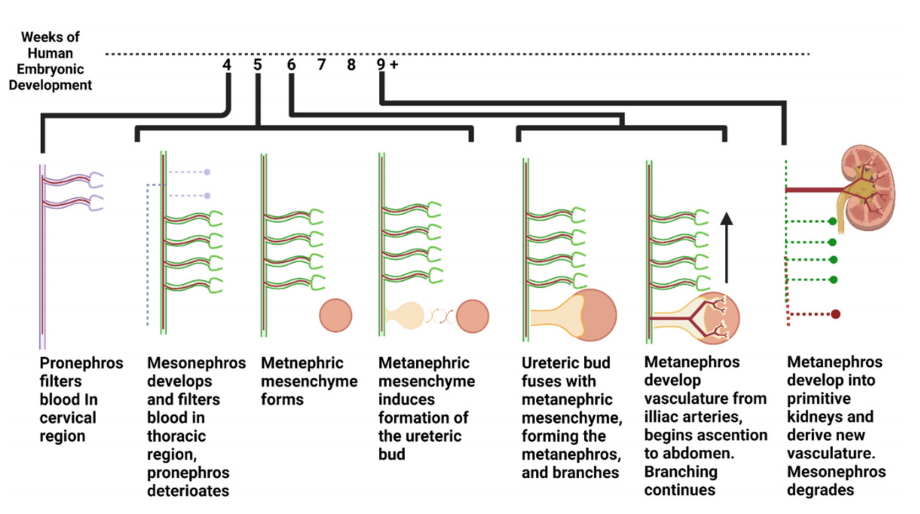
Abbildung 1. Entwicklung des menschlichen Harnsystems von Woche 4 bis 9 im Mutterleib.
2.2. Protokolle zur Erzeugung von Nierenorganoiden
Nierenorganoide können aus aus Gewebe gewonnenen differenzierten Zellen oder pluripotenten Stammzellen gebildet werden. Um ein Nierenorganoid aus aus Gewebe gewonnenen Zellen zu entwickeln, kann man die differenzierten adulten Zellen ex vivo im dreidimensionalen Raum anordnen, um die menschliche Organarchitektur nachzuahmen [9]. Organoidprotokolle für aus Gewebe gewonnene differenzierte Zellen werden an anderer Stelle behandelt. In diesem Aufsatz konzentrieren wir uns auf aus Stammzellen gewonnene Nierenorganoide. Um diese Systeme zu schaffen, können Wissenschaftler pluripotente Stammzellen in Gegenwart nierenspezifischer endogener Morphogene und extrazellulärer Komponenten kultivieren. Stammzellen können sich dann selbst zu nierenähnlichen Strukturen zusammensetzen und so die embryonale Nierenentwicklung nachahmen. Organe wie der Darm beherbergen endogene Stammzellpopulationen im erwachsenen Gewebe, mit denen Wissenschaftler Organoide herstellen können [10]. Da es jedoch keine eindeutigen Beweise dafür gibt, dass eine erwachsene menschliche Niere eine Stammzellnische enthält, müssen aus Stammzellen gewonnene Nierenorganoide aus pluripotenten Stammzellen (entweder embryonalen oder hiPSC) hergestellt werden [11].

Aus Stammzellen gewonnene Nierenorganoide können in die folgenden zwei Kategorien eingeteilt werden: Nephron-Vorläuferorganoide (NP) und Ureterknospenorganoide (UB). Beide Arten von Organoiden haben sich als Krankheitsmodelle gut etabliert. NP-Organoide ähneln dem metanephrischen Mesenchym, das multipotente NP-Zellen enthält. Tatsächlich kann eine einzelne metanephrische mesenchymale Zelle alle Epithelzellen des Nephrons mit Ausnahme des Sammelrohrs hervorbringen [8]. Methoden zur Erzeugung von hiPSC-abgeleiteten NP-Organoiden umfassen eine 2D-Kultur mit anschließender Aggregation in einer porösen Transwellplatte (z. B. Takasato et al. (2016), Morizane et al. (2015)) oder eine 3D-Kultur in einem Hydrogel (z. B. Freedman et al . (2015)) [12–14]. Diese Organoide entwickeln glomeruläre und röhrenförmige Strukturen. NP-Organoide, die aus zwei der beliebtesten NP-Protokolle von Takasato und Morizane abgeleitet wurden, wurden in einer umfassenden Omics-Analyse von Wu et al. verglichen. (2018) [15]. Sie fanden heraus, dass das Takasato-Protokoll etwa 11 % Podozyten-ähnliche Zellen und 21 % Off-Target-Zellen pro Organoid erzeugt, während das Morizan-Protokoll etwa 28,5 % Podozyten-ähnliche Zellen und 14,3 % Off-Target-Zellen erzeugt [15]. Takasatos Organoide scheinen ebenfalls eine kleine Menge UB-ähnlicher Regionen zu entwickeln, imitieren jedoch überwiegend das metanephrische Mesenchym und klassifizieren sie daher als NP-Organoide [12]. Darüber hinaus haben Morizane et al. (2015) und Takasato et al. (2016) fehlt eine extrazelluläre Hydrogelumgebung, die in der Arbeit von Freedman et al. (2015) vorhanden ist [14]. Garreta et al. (2019) argumentieren, dass das Vorhandensein eines Hydrogels bei der Organoidbildung die Bildung der Nierenstruktur verbessert und die Produktion von frühen IM-Markern, hinteren IM-Markern und vorderen IM-Markern steigert [16].
Im Gegensatz zu NP-Organoiden imitieren UB-Organoide die Ureterknospe, wodurch das Sammelrohrsystem entsteht. Methoden zur Erzeugung von UB-Organoiden wurden in jüngerer Zeit entwickelt und umfassen die Kultivierung von Embryoidkörpern und die anschließende Aggregation in Vertiefungen mit geringer Adhäsion [17]. Diese Organoide haben Röhren- und Sammelrohrstrukturen. Schließlich wurden auch NP- und UB-Organoide kombiniert, um Co-Kulturstrukturen höherer Ordnung zur Rekapitulation erwachsener Menschen zu erzeugenNierenphänotypen[17]. Die beliebtesten Protokolle fürNierenorganoidsind in Abbildung 2 unten zusammengefasst [12–14,17–19].
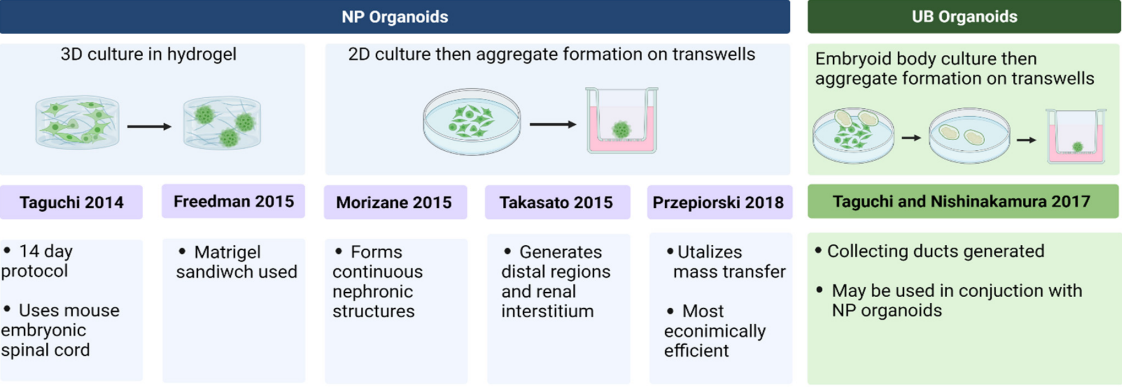
Abbildung 2. Zusammenfassung der beliebtesten Protokolle zur Organoidbildung
2.3. Wie sie sich schlagen: Nierenorganoide vs. menschliche Nieren
Die oben beschriebenen Protokolle beinhalten in erster Linie die Selbstorganisation von hiPSCs zu Organoiden. Sie ahmen fetale Zustände nach, um hiPSCs dazu zu bringen, sich in nierenspezifische Abstammungslinien zu differenzieren und nierenspezifische Strukturen zu bilden. Der erste fetale Zustand, den sie reproduzieren, ist die Primitivstreifen-Signalisierung. Der Primitivstreifen ist ein Abschnitt des Embryos, der sich entwickelt, bevor sich die drei Keimschichten trennen. Die meisten Protokolle nutzen dazu den WNT-Signalagonisten CHIR. Als nächstes muss für die Ableitung der NP-Linie das posterior-intermediate Mesoderm (PIM) induziert werden, und für die UB-Linie muss das anterior-intermediate Mesoderm (AIM) induziert werden [17]. Interessanterweise haben Takasato et al. (2015) fanden heraus, dass je länger der Zeitraum der CHIR-Verabreichung war, desto mehr posterior-ähnliches Mesoderm sich entwickelte, während je kürzer der Zeitraum, desto mehr anterior-ähnliches Mesoderm entwickelte [20]. Somit führt eine längere WNT-Signalisierungsdauer zu einer stärkeren Bildung glomerulärer und proximaler Strukturen, während eine verringerte WNT-Signalisierungsdauer zu einer stärkeren Bildung distaler Strukturen führt.
Nach Abschluss des NP-Protokolls entwickeln sich Organoide mit sowohl glomerulären als auch tubulären Regionen. Sie sind jedoch unreif. Studien haben gezeigt, dass von hiPSC abgeleitete Nierenorganoide den Fötus im ersten Trimester nachahmen [20]. Eine der umfangreichsten Analysen zu diesem Thema wurde von Subramanian et al. durchgeführt. (2019), der RNA-seq nutzte, um Nierenorganoide mit 8-Wochen-, 17-Wochen- und erwachsenen menschlichen Nieren zu vergleichen. Sie kamen zu dem Schluss, dass Nierenorganoide in den Wochen 8 und 17 beim Fötus den menschlichen Nieren ähnlicher sind als bei erwachsenen Nieren [21]. Darüber hinaus zeigen Nierenorganoide eine Färbung primitiver multipotenter Marker wie SIX2+ in der gesamten Niere, wohingegen die erwachsene differenzierte menschliche Niere solche Marker nicht exprimiert [22]. Um das Nierenorganoid als Stellvertreter für die erwachsene menschliche Niere zur Untersuchung von Krankheiten verwenden zu können, muss das Gestationsalter daher voranschreiten.
Nierenorganoide imitieren möglicherweise nicht nur den frühen Metanephros besser als die richtige erwachsene menschliche Niere, sondern ähneln möglicherweise sogar noch mehr dem Mesonephros als dem Metanephros, wenn die Morphogenkonzentration nicht ordnungsgemäß reguliert wird [23]. Um diese Bedenken auszuräumen, haben Tsujimoto et al. (2020) untersuchten in vitro die Differenzierung von hiPSC in mesonephrische NPs, metanephrische NPs und UB-Zellen [24]. Diese Studie identifizierte mehrere Faktoren, die diese drei Abstammungslinien unterscheiden und könnte daher auf die zukünftige Untersuchung dieser drei unterschiedlichen Systeme angewendet werden [24]. Weitere wichtige Fortschritte bei der Reifung von Organoiden sind NP-UB-Wechselwirkungen und Vaskularisierung. Einige der bemerkenswertesten Studien zur Lösung dieser Probleme wurden von Taguchi und Nishinakamura (2017) sowie Tsujimoto et al. durchgeführt. (2020) [17,24]. Diese Studien erzeugten MM-UB-kokultivierte Organoide und transplantierten sie in Mäuse, wo sie vaskularisiert wurden. Die Erzeugung dieser metanephrischen Strukturen höherer Ordnung hat die Ähnlichkeit der aus Stammzellen gewonnenen Nierenstruktur mit echten menschlichen Nieren erheblich verbessert. Allerdings waren selbst diese fortschrittlichen Systeme nicht in der Lage, die umfassendere UB-Verzweigung zu rekapitulieren, die im zweiten und letzten Trimester in vivo auftritt [24]. Diese Ergebnisse unterstreichen die Notwendigkeit, endogene reife Nierenfunktionen und Interaktionen zu reproduzieren, die aktuellen Organoiden fehlen, wie beispielsweise der Flüssigkeitsfluss.
3. Nierenorganoide als Modellsysteme
Die Ähnlichkeit von Nierenorganoiden mit menschlichen Nieren macht sie für die Modellierung von Krankheiten und das Screening von Arzneimitteln geeignet. Sie können in weniger als einem Monat hergestellt, individuell auf eine Person zugeschnitten und in großen Mengen hergestellt werden [12–14,17–19]. Darüber hinaus können sie in vitro kultiviert oder in Mäuse, Ratten oder Hühnereier transplantiert werden, um vollständige In-vivo-Modelle zu bilden. Im Folgenden werden wir Analysen untersuchen, die mit Nierenorganoiden durchgeführt werden können, sowie aktuelle und zukünftige Verwendungen von Nierenorganoiden in der biomedizinischen Forschung.
3.1. Nierenorganoidanalyse
3.1.1. In-vitro-Assays
An Nierenorganoiden können verschiedene physiologische, molekulare und funktionelle Tests durchgeführt werden. Im Hinblick auf molekulare Tests wurden verschiedene transkriptomische Analysen erfolgreich an Nierenorganoiden durchgeführt [25]. Beispielsweise haben Takasato et al. (2015) extrahierten RNA aus Organoiden und führten RNA-Sequenzierung und qRTPCR-Analysen durch [20].
Andere, wie Wu et al. (2018) haben zusätzlich zur DropSeg-scRNA-Sequenzierung in Nierenorganoiden eine Kernisolierung und snRNA-Sequenzierung durchgeführt. Zusätzlich zu den RNA-Spiegeln wurden verschiedene Proteinspiegel aus Nierenorganoid-Lysat mittels Immunoblot quantifiziert und verglichen (z. B. Cruz et al., 2017; Morais et al., 2022) [26,27]. Darüber hinaus wurden routinemäßig immunzytochemische Analysen an Nierenorganoiden durchgeführt, um spezifische Nephronstrukturen zu untersuchen. Dies wird häufig als Färbung ganzer Organoide durchgeführt; Alternativ wurden auch Gewebeschnitte zur Untersuchung verwendet (z. B. Takasato et al., 2015; Cruz et al., 2017) (20,26). Diese Studien haben gezeigt, dass Nierenorganoide Glomeruli, proximale Tubuli, distale Tubuli, Basalmembranen usw. aufweisen Sammelrohranordnung (20,27). Abbildung 3 unten zeigt ein Beispiel von in Paraffin eingebetteten und geschnittenen menschlichen Nierenorganoiden, die mit dem Protokoll von Takasato et al. (2016) erstellt wurden (12). Der Schnitt ist für glomeruläre, proximale und distale Tubuli gefärbt Tubulus-Markerproteine und weist durchgehende glomeruläre bis distale tubuläre nephronische Strukturen auf. Neben diesen Strukturen ist bekannt, dass die Organoide der Niere auch ein Gefäßsystem aufweisen. Dieses ist jedoch begrenzt, bildet sich schnell zurück und ist nicht wie in einer typischen Niere organisiert (28).
An Nierenorganoiden können auch mehrere Funktionstests durchgeführt werden. Wie beispielsweise von Freedman et al. (2022) können Nierenorganoide Pulse-Chase-Assays unterzogen werden, bei denen den Medien verschiedene fluoreszierende Moleküle zugesetzt werden können, bevor sie durch neue Medien ohne Fluoreszenz ersetzt werden [29]. Organoide können dann auf die Aufnahme dieser Moleküle analysiert werden, und die resultierenden Informationen können verwendet werden, um Informationen über Akkumulation, Schwellung, Filtration, endokrine oder Verletzung abzuleiten [29]. Eines der Probleme bei diesem Assay in organoiden Plattformen besteht jedoch darin, dass Moleküle von außen in geschlossene röhrenförmige Strukturen eingeführt werden können, anstatt durch die apikale Oberfläche, wie dies in vivo der Fall wäre. Daher können fluoreszierende Moleküle von der äußeren basolateralen Membran absorbiert werden, da es keine Möglichkeit gibt, zu kontrollieren, wohin diese Moleküle gelangen, wenn sie grob in das Medium gelangen. Darüber hinaus kann der Transport von Molekülen durch die Diffusion innerhalb von Organoiden eingeschränkt werden, was zu unterschiedlichen Akkumulationstrends innerhalb desselben Organoids führt.
Darüber hinaus kann die Nierenreparatur auch auf Organoidplattformen bewertet werden, was Einblicke in die Umkehrmechanismen von Nierenschäden und die genetischen Grundlagen ermöglicht, die Patienten für eine Nierenerkrankung prädisponieren können. Studien wie Gupta et al. (2022) haben Genwege untersucht, die bei einmaliger oder mehrfacher Exposition gegenüber Cisplatin, einem Nierenschädigungsmolekül, in Organoidplattformen der Niere hochreguliert wurden [30]. Schließlich kann die Zystenbildung in Organoiden analysiert werden, um die polyzystische Nierenerkrankung (PKD) über die cAMP-Aktivierung zu untersuchen [26]. Zysten können dann gemessen, quantifiziert und als Ersatz für menschliche Nierenzysten behandelt werden.
3.1.2. In-vivo-Analyse
Ein wesentlicher Nachteil der Verwendung von In-vitro-Nierenorganoiden als Modellsystem ist ihr mangelndes Zusammenspiel mit dem Rest des Organismus. Eine Vielzahl von Erkrankungen, die entfernte Körperteile betreffen, können sich auf die Niere auswirken und umgekehrt. Beispielsweise können Veränderungen des Blutdrucks den glomerulären Druck drastisch verändern, den wiederum die Niere regulieren kann. In vitro berücksichtigen organoide Systeme diese systemischen Wechselwirkungen jedoch nicht. Daher wurden Transplantationsansätze untersucht, die vom Menschen stammende Nierenorganoide bei Mäusen, Ratten und Hühnereiern umfassen. In solchen Studien werden menschliche und tierische Gewebe durch Immunfärbung des humanen Kernantigens oder Y-Chromosomen-Leseausrichtung anhand der kombinierten Genomreferenz unterschieden [21]. Darüber hinaus können Organoide über ein Gerüst (z. B. Seide) transplantiert werden, um ein höheres Maß an struktureller Integrität zu gewährleisten [31]. Dieser Ansatz ermöglicht möglicherweise einfachere organoidgewebespezifische Analysen nach der Transplantation.
Ein wesentlicher Vorteil der Transplantation von Nierenorganoiden besteht darin, dass Organoide den Urin vaskularisieren, reifen und sogar filtern können. Van den Berg et al. (2018) haben gezeigt, dass nach einer subkapsulären Nierentransplantation bei Mäusen die organoiden Glomeruli und Tubuli der Niere deutlich reifen [32]. In einer anderen Studie haben Subramanian et al. (2019) haben gezeigt, dass die Transplantation von hiPSC-abgeleiteten Organoiden in Mäuse zu einer erhöhten Reifung der proximalen und distalen Tubuli und einer verringerten Präsenz von Off-Target-Zellpopulationen innerhalb des Organoids führt [21]. Noch wichtiger ist, dass Nierenorganoide nach der Transplantation die ultimative Funktion der Niere erfüllen können, nämlich Blut zu filtern. Nach subkutaner Transplantation in Mäusen bildeten Nierenorganoide urinfilternde Strukturen, was durch die Übertragung von FITC-markiertem Dextran belegt wurde [33]. Somit ermöglicht eine Transplantation nicht nur die Untersuchung der Auswirkungen einer Mutation in einem Nierenorganoid in vivo, sondern verbessert auch die Ähnlichkeit des Organoids mit der menschlichen Niere und macht es zu einem einigermaßen funktionsfähigen System.
Während immundefiziente Mäuse häufig für die Organoidtransplantation von hiPSC-Nieren verwendet werden, wurden auch andere Wirte, wie z. B. Chorioallantoismembranen (CAM) von Küken, verwendet. Ein CAM ist von Natur aus immundefizient und fördert die Vaskularisierung des Organoids [16]. Allerdings fehlen ihm typische Organsysteme von Säugetieren, sodass die Organoide der Niere anders als bei Mäusen von anderen Systemen abgekoppelt sind. Trotz wirtsbedingter Rückschläge ermöglicht die Chimärenerzeugung mit vom Menschen stammenden Nierenorganoiden eine umfassende In-vivo-Untersuchung menschlicher Nierenerkrankungen auf einer äußerst wirkungsvollen Plattform.
3.2. Bisher durchgeführte Krankheitsmodellierungsstudien
3.2.1. Nierenorganoide als genetische Krankheitsmodelle
Nierenorganoide wurden zur Untersuchung tubulärer und glomerulärer genetischer Nierenerkrankungen eingesetzt [26,34,35]. Zu den häufigsten tubulären Erkrankungen beim Menschen gehören die pädiatrische polyzystische Nierenerkrankung (PKD), die aus autosomal-rezessiven Mutationen im fibrozystischen Gen (PKHD1) resultiert, und die adulte PKD, die aus autosomal-dominanten Mutationen im Polycystin-1 resultiert -2-Gene [36–38]. Diese Mutationen können durch Gen-Editing-Technologien wie das CRISPR-Cas-9-System künstlich in hiPSCs eingeführt werden. Die bearbeiteten hiPSCs können anschließend in PKD-modellierende menschliche Nierenorganoide gezüchtet und mittels Proteinfärbung und RNA-Profilierung analysiert werden. Freedman et al. (2015) und Cruz et al. (2017) haben mithilfe des CRISPR/Cas9-Systems Polycystin-Gene in hiPSC-Linien ausgeschaltet und anschließend Organoide abgeleitet, die den in vivo bei erkrankten Patienten gefundenen zystischen Phänotyp nachahmen [14,26]. Diese Studien zeigen, dass Nierenorganoide als leicht beobachtbare, krankheitsrelevante Plattformen zur Untersuchung von PKD verwendet werden können. Darüber hinaus ermöglichen Organoide aus patienteneigenen Zelllinien Einblicke in patientenspezifische Mutationen und die Wahrscheinlichkeit der Krankheitsentwicklung. Beispielsweise haben Low et al. (2019) entwickelten Nierenorganoide von Patienten mit PKHD1-Mutationen und verglichen sie mit Wildtyp-Organoiden [39]. Die erkrankten Organoide zeigten eine deutlich stärkere Zystenbildung, was das Potenzial von Nierenorganoiden zeigt, die Krankheitsmanifestation anhand des Genotyps vorherzusagen [39]. In einer anderen Studie haben Hernandez et al. (2021) leiteten hiPSCs von Patienten mit Mutationen im Tuberous Sclerosis Complex-2-Gen ab, was den Patienten anfällig für die Entwicklung von Nierentumoren macht [40]. Anschließend korrigierten sie die Mutation des Patienten mit dem CRISPR/Cas9-System. Nierenorganoide aus diesen korrigierten isogenen Mutantenlinien zeigten im Vergleich zu den erkrankten Organoiden eine verringerte Zystenbildung und wiederhergestellte Genwege, was die Nützlichkeit von Nierenorganoiden bei der Untersuchung der nachgeschalteten funktionellen Auswirkungen spezifischer Mutationen in isogenen organähnlichen Systemen demonstriert.
Forscher haben auch von Patienten gewonnene Organoide verwendet, um Einblicke in genetische Krankheiten zu gewinnen, die das Glomerulus betreffen. Beispielsweise haben Hale et al. (2018) konzentrierten sich auf das NPHS1-Gen (Nephrin), das, wenn es mutiert ist, eine fehlerhafte Bildung des Podozyten-Fußfortsatzes und eine undichte Urinfiltration induziert, was zu einer Nierenerkrankung führt [34]. Hale et al. (2018) verwendeten von Patienten stammende mutierte NPHS1-hiPSCs, um Nierenorganoide abzuleiten, die diese fehlerhaften Podozyten-Fußprozesse modellierten, einschließlich verringerter Mengen an Podozyten-spezifischen Proteinen, Nephrin und Podocin [34]. Ebenso haben Freedman et al. (2015) schalteten das glomeruläre Gen PODXL in hiPSCs aus und fanden heraus, dass Organoide eine fehlerhafte Podozyten-Podozyten-Architektur aufweisen [14].
Ein weitgehend ungenutztes Potenzial von Nierenorganoiden ist ihre Fähigkeit, embryonale und fetale Defekte zu modellieren. Derzeit streben Forscher danach, die erwachsene menschliche Niere mit dem Nierenorganoid zu modellieren. In seinem aktuellen Zustand im ersten und zweiten Trimester kann das Nierenorganoid jedoch zur Untersuchung entwicklungsbedingter Nierendefekte verwendet werden [41]. Entwicklungsstörungen des Harnsystems, wie z. B. Nierendysplasie, gehören zu den häufigsten und schwerwiegendsten Entwicklungsstörungen [42]. Da viele dieser Krankheiten bereits in der 11. Woche erkannt werden können, eignen sich Nierenorganoide besonders gut für die Untersuchung angeborener Nierenschäden. Wir verfügen nicht nur über metanephrische Nierenorganoide des ersten und zweiten Trimesters, sondern auch über primitive mesonephrische Nierenzelllinien (z. B. Tsujimoto et al., 2020), um embryonale und fetale Defekte zu untersuchen [24]. Da nur wenige Systeme die Untersuchung und Manipulation einer sich entwickelnden menschlichen Niere ermöglichen, bietet das Nierenorganoid ein enormes Potenzial für fetale genetische, toxikologische und Entwicklungsstudien.
3.2.2. Nierenorganoide als Modelle für andere Krankheiten
Zusätzlich zu genetischen Erkrankungen wurden Nierenorganoide verwendet, um die Reaktion menschlicher Systeme auf Virusinfektionen, Krebs und Verletzungen zu untersuchen. Beispielsweise haben Jansen et al. (2021) nutzten eine Nierenorganoidplattform, um die Auswirkungen des viralen SARS-CoV-2 auf menschliche Nieren zu bewerten [43]. Diese Gruppe entdeckte, dass eine SARS-CoV-2-Infektion zu einer erhöhten Kollagen-I-Expression in menschlichen Nierenorganoiden führt und lieferte damit eine mechanistische Erklärung für die Nierenschädigung und Fibrose, die oft mit schweren Fällen von langem COVID einhergeht-19 [ 43]. In Bezug auf die Krebsforschung haben Hernandez et al. (2021) transplantierten Nierenorganoide in immundefiziente Ratten, um seltene genetisch beeinflusste Nierentumoren zu modellieren. Hier entwickelten von Patienten stammende Organoide tumorähnliche Läsionen und rekapitulierten so menschliche Nierentumoren [40]. Darüber hinaus nutzten sie Nierenorganoid-basierte Tumormodelle als halbfunktionale, vom Menschen abgeleitete Strukturen und testeten Medikamente und nanopartikelbasierte Therapien. Schließlich haben neuere Studien gezeigt, dass Nierenorganoide verwendet werden können, um die Reaktion auf Nierenverletzungen zu testen. Beispielsweise haben Prezpiorski et al. (2022) zeigten, dass Nierenorganoide Marker für oxidativen Schaden und eine erhöhte Expression von Verletzungsmarkern produzieren, indem sie Nierenorganoiden das Verletzungsmolekül Hämin zusammen mit einem Biosensor verabreichten [44].
3.2.3. Nierenorganoide in der Arzneimittelbewertung
Nierenorganoide liefern nicht nur Einblicke in Krankheiten, sondern werden auch zum Screening von Medikamenten eingesetzt. Insbesondere wurden Nierenorganoide verwendet, um medikamenteninduzierte Nierenschäden (DIKI) zu untersuchen, die eine der Hauptursachen für akute Nierenschäden sind [45]. Bei der Bewertung der Nebenwirkungen von Cisplatin haben Czerniecki et al. (2018) zeigten, dass Nierenorganoide als Hochdurchsatzmodelle für die Prüfung neuer Arzneimittel in einem vielfältigen Bereich der Humangenetik hilfreich sind [46].
Andere, wie Wu et al. (2018) haben zusätzlich zur DropSeg-scRNA-Sequenzierung in Nierenorganoiden eine Kernisolierung und snRNA-Sequenzierung durchgeführt. Zusätzlich zu den RNA-Spiegeln wurden verschiedene Proteinspiegel aus Nierenorganoid-Lysat mittels Immunoblot quantifiziert und verglichen (z. B. Cruz et al., 2017; Morais et al., 2022) [26,27]. Darüber hinaus wurden routinemäßig immunzytochemische Analysen an Nierenorganoiden durchgeführt, um spezifische Nephronstrukturen zu untersuchen. Dies wird häufig als Färbung ganzer Organoide durchgeführt; Alternativ wurden auch Gewebeschnitte zur Untersuchung verwendet (z. B. Takasato et al., 2015; Cruz et al., 2017) (20,26). Diese Studien haben gezeigt, dass Nierenorganoide Glomeruli, proximale Tubuli, distale Tubuli, Basalmembranen usw. aufweisen Sammelrohranordnung (20,27). Abbildung 3 unten zeigt ein Beispiel von in Paraffin eingebetteten und geschnittenen menschlichen Nierenorganoiden, die mit dem Protokoll von Takasato et al. (2016) erstellt wurden (12). Der Schnitt ist für glomeruläre, proximale und distale Tubuli gefärbt Die Organoide der Niere weisen neben diesen Strukturen bekanntermaßen auch ein Gefäßsystem auf. Dieses ist jedoch begrenzt, bildet sich schnell zurück und ist nicht wie in einer typischen Niere organisiert (28).
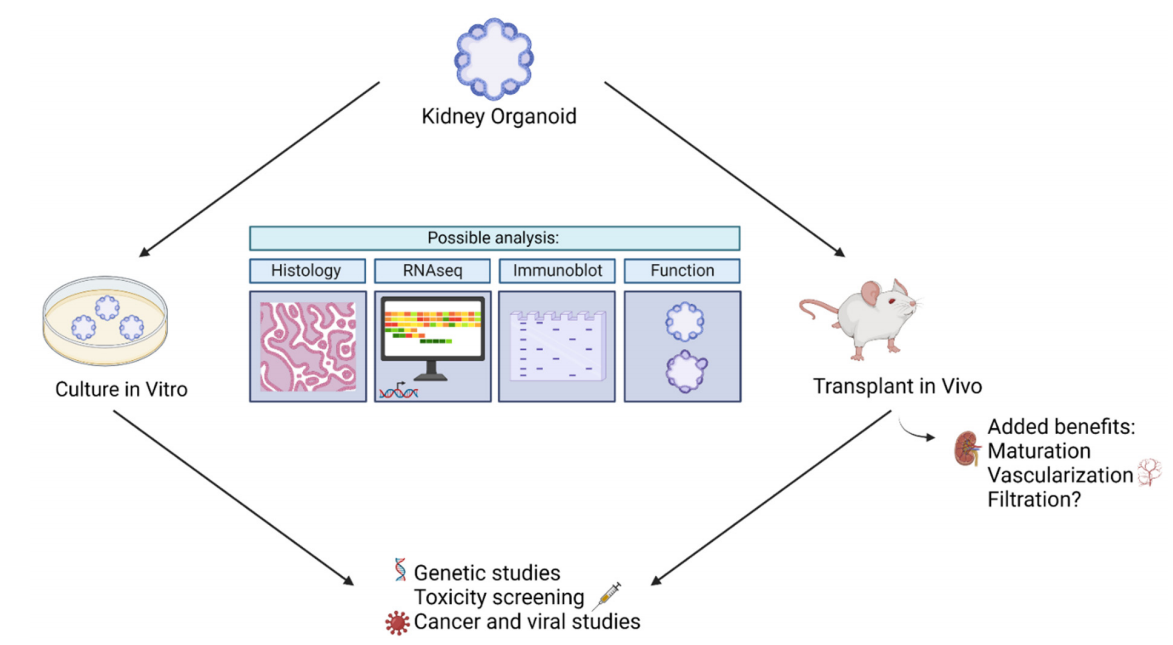
Abbildung 4. Zusammenfassung der Möglichkeiten, wie Nierenorganoide zur Modellierung von Krankheiten verwendet werden können. Zusammenfassung der Möglichkeiten, wie Nierenorganoide zur Modellierung von Di verwendet werden können






