Melatonin als Coadjuvans bei der Behandlung von Patienten mit Fibromyalgie Teil 1
Oct 07, 2023
Abstrakt:Das Fibromyalgie-Syndrom (FMS) ist ein chronisches, weit verbreitetes Schmerzsyndrom, das mit Müdigkeit, Schlafstörungen, Angstzuständen, Depressionen, Konzentrationsschwäche und neurokognitiven Beeinträchtigungen einhergeht. Da die derzeit verfügbaren Medikamente gegen diese Symptome nicht vollständig wirksam sind und häufig mehrere Nebenwirkungen haben, haben sich viele Wissenschaftler auf die Suche nach nicht-pharmakologischen Heilmitteln gemacht. Es wurde vermutet, dass viele der FMS-bedingten Symptome mit einem veränderten Muster des endogenen Melatonins zusammenhängen. Melatonin ist an der Regulierung mehrerer physiologischer Prozesse beteiligt, darunter zirkadiane Rhythmen, Schmerzen, Stimmung sowie das oxidative und immunmodulatorische Gleichgewicht. Vorläufige klinische Studien haben ergeben, dass die Verabreichung unterschiedlicher Melatonindosen an Patienten mit FMS das Schmerzniveau reduzieren und Stimmungs- und Schlafstörungen verbessern kann. Darüber hinaus verbessern sich die gesamte antioxidative Kapazität, der 6-Sulfatoxymelatonin- und Cortisolspiegel im Urin sowie andere biologische Parameter nach der Einnahme von Melatonin. Jüngste Untersuchungen haben einen pathophysiologischen Zusammenhang zwischen mitochondrialer Dysfunktion, oxidativem Stress und FMS vorgeschlagen, indem bestimmte Proteine untersucht wurden, die an der mitochondrialen Homöostase entsprechend der Ätiopathogenese dieses Syndroms beteiligt sind. Diese Verbesserungen wirken sich positiv auf die Lebensqualität von FMS-Patienten aus, was darauf hindeutet, dass der Einsatz von Melatonin als Coadjuvans eine erfolgreiche Strategie zur Behandlung dieses Syndroms sein könnte.
Cistanche kann als Anti-Müdigkeits- und Ausdauerverstärker wirken, und experimentelle Studien haben gezeigt, dass das Abkochen von Cistanche tubulosa die Leberhepatozyten und Endothelzellen, die bei schwimmenden Mäusen unter Belastung geschädigt wurden, wirksam schützen, die Expression von NOS3 hochregulieren und das Leberglykogen fördern kann Synthese und übt so eine Anti-Ermüdungswirkung aus. Phenylethanoidglykosid-reicher Cistanche tubulosa-Extrakt könnte die Kreatinkinase-, Laktatdehydrogenase- und Laktatspiegel im Serum erheblich senken und den Hämoglobin- (HB) und Glukosespiegel bei ICR-Mäusen erhöhen. Dies könnte eine Anti-Müdigkeitsrolle spielen, indem es die Muskelschädigung verringert und Verzögerung der Milchsäureanreicherung zur Energiespeicherung bei Mäusen. Die zusammengesetzten Cistanche Tubulosa-Tabletten verlängerten die Schwimmzeit unter Belastung erheblich, erhöhten die Glykogenreserve in der Leber und senkten den Harnstoffspiegel im Serum nach dem Training bei Mäusen, was ihre Anti-Ermüdungswirkung zeigte. Das Abkochen von Cistanchis kann die Ausdauer verbessern und die Beseitigung von Müdigkeit bei trainierenden Mäusen beschleunigen. Außerdem kann es den Anstieg der Serumkreatinkinase nach Belastungsübungen verringern und die Ultrastruktur der Skelettmuskulatur von Mäusen nach dem Training normal halten, was darauf hinweist, dass es die Wirkung hat zur Verbesserung der körperlichen Stärke und zur Bekämpfung von Müdigkeit. Cistanchis verlängerte auch die Überlebenszeit von mit Nitrit vergifteten Mäusen erheblich und erhöhte die Toleranz gegenüber Hypoxie und Müdigkeit.

Klicken Sie auf COVID-Müdigkeit
【Für weitere Informationen:george.deng@wecistanche.com / WhatsApp:8613632399501】
Schlüsselwörter:Antioxidans; antioxidative Kapazität; Fibromyalgie; Melatonin; schlafen
1. Einleitung
Die Geschichte der Fibromyalgie (FMS) als pathologisches Krankheitsbild ist relativ neu. Im 19. Jahrhundert war sie als Fibrositis, noduläre Fibromyositis oder psychogener Rheuma bekannt, und erst in den 1970er Jahren erhielt sie eine umfassende klinische Beschreibung. 1992 wurde es von der Weltgesundheitsorganisation (WHO) und 1994 von der International Association for the Study of Pain mit dem Code X33.X8a anerkannt. FMS ist jetzt als Diagnose in der zehnten Revision der Internationalen statistischen Klassifikation von Krankheiten und gesundheitsbezogenen Problemen der WHO als Teil der Kategorie „Andere Weichteilerkrankungen, die nicht an anderer Stelle aufgeführt sind“ [1,2] enthalten, obwohl es auch als Diagnose angesehen werden könnte eine Reihe von Erkrankungen mit einem gemeinsamen klinischen Ausdruck und unterschiedlicher Symptomintensität [3].
Die Prävalenz von FMS wird in der Weltbevölkerung auf 2–8 % und in Spanien auf 2,4 % geschätzt [2]. FMS kann sich in jedem Alter entwickeln, tritt jedoch meist im Alter zwischen 20 und 50 Jahren auf, wurde aber auch im Kindesalter festgestellt. FMS tritt bei Frauen mit einem Verhältnis von 10:1 häufiger auf als bei Männern [2]. Niedrige Bildung und sozioökonomisches Niveau gelten als Risikofaktoren für die Entwicklung der Krankheit. Das Vorliegen von Komorbiditäten wie Kopfschmerzen oder Migräne, chronischem Müdigkeitssyndrom und Reizdarmsyndrom kommt bei FMS sehr häufig vor [1].
Nur bei 12–28 % der in bevölkerungsbasierten Umfragen identifizierten Patienten, die die Kriterien des American College of Rheumatology (ACR) von 1990 erfüllten, wurde FMS diagnostiziert [1]. Die Diagnose Fibromyalgie wurde in den 90er-Jahren gestellt. Dabei wurden die Befunde über empfindliche Stellen berücksichtigt, die ein Arzt feststellt, wenn er die Symptome untersucht, auf die sich ein Patient bezieht (Schmerzen bei Druck an bestimmten Stellen des Körpers ohne andere Veränderungen); Im Jahr 2010 wurden jedoch zwei von Patienten bereitgestellte Fragebögen, ein allgemeiner Schmerzindex (der Widespread Pain Index (WPI)) und eine Schweregradskala der Symptome (der Symptom Severity Score (SS-Score)), als neue diagnostische Kriterien vorgeschlagen [3]. . Alles in allem haben die meisten Studien ihren Schwerpunkt von der Ätiologie auf die Symptombehandlung verlagert.
Kürzlich haben mehrere Studien gezeigt, dass oxidativer Stress an der Pathophysiologie von FMS beteiligt ist [4,5]. Bei Patienten mit FMS sind die Plasmaspiegel der Lipidperoxidation verringert, was auf die intrazelluläre Produktion reaktiver Sauerstoffspezies (ROS) zurückzuführen ist [6]; Die Konzentrationen an carbonylierten Proteinen sind ebenfalls hoch, da sie die Endprodukte der durch ROS verursachten Membranschädigung sind [7,8]. Es wurde jedoch auch eine Abnahme der gesamten antioxidativen Kapazität oder antioxidativer Enzyme wie Katalase oder Superoxiddismutase beobachtet [7–9] sowie ein Zusammenhang zwischen den Plasmaspiegeln toxischer Schwermetalle und essentieller Metalle mit Markern für oxidativen Stress [10]. ]. Bei FMS-Patienten wurde auch eine Veränderung der Plasmaverteilung von Coenzym Q10 (CoQ10) nachgewiesen, die durch Beeinträchtigung der mitochondrialen Entkopplungsproteine zu einer Funktionsstörung der Atmungskette und zu einer höheren ROS-Produktion in mononukleären Zellen führt [11].
ROS sind an der Ätiologie von Schmerzen beteiligt, einem wichtigen Symptom bei FMS [12]. Der pathophysiologische Zusammenhang zwischen mitochondrialer Dysfunktion und oxidativem Stress ist noch unbekannt, aber die Pathogenese von FMS würde damit übereinstimmen [13]. Der Verlust von Mitofusin 2 (Mfn2), einem Protein der äußeren Mitochondrienmembran, das die Mitochondrienfusion vermittelt, wurde in mehreren Studien [14–16] als Ursache für die Erschöpfung von CoQ10, veränderte Übergangsporen der Mitochondrienpermeabilität und die ROS-Produktion vorgeschlagen [17]. Darüber hinaus kontrolliert CoQ10 den Serotoninspiegel und depressive Symptome bei FMS-Patienten [18]. Die Rolle, die Mfn2 bei der Regulierung von CoQ10 für eine optimale Leistung der mitochondrialen Atmungskette spielt, ist unklar, es wurde jedoch eine überraschende und neuartige Rolle von Mfn2 bei der Aufrechterhaltung des Terpenoid-Biosynthesewegs gezeigt, der für die mitochondriale CoQ10-Produktion erforderlich ist [17]. Darüber hinaus haben andere Studien gezeigt, dass der Peroxisom-Proliferator-aktivierte Rezeptor-Gamma-Koaktivator-1alpha (PGC-1)-Signalweg die Mfn2-Gen- und Proteinexpression regulieren kann [19].
FMS wird als chronische Erkrankung unbekannter Ätiologie definiert und ist Teil einer Vielzahl von Syndromen, für die es weder genaue Klassifizierungen noch spezifische Tests gibt, die ihre Diagnose ermöglichen. Es hat große Auswirkungen auf die Lebensqualität der Patienten und ist in manchen Fällen eine behindernde Situation [2,20]. Obwohl dieses Syndrom als psychosomatische Störung angesehen wird, deuten neuere Studien darauf hin, dass FMS eine Störung der Schmerzkontrolle auf Gehirnebene ist und daher den zentralen Sensibilisierungssyndromen zugeordnet werden könnte [2]. Da es sich bei FMS um ein äußerst komplexes Syndrom mit variabler Symptomlandschaft und noch unbekannter Ätiologie handelt, konzentriert sich seine pharmakologische Behandlung im Allgemeinen auf die Linderung von Angstzuständen und Schmerzen, die Verbesserung der Stimmung/des emotionalen Zustands des Patienten oder die Bekämpfung von nächtlichen Schlafstörungen und/oder Schlaflosigkeit . Bei mehreren Stimmungsstörungen, wie saisonalen affektiven, bipolaren und schweren Depressionen, sind Störungen des Schlafes und des zirkadianen Rhythmus die Hauptsymptome [21]. Melatonin, ein Neurohormon, das hauptsächlich von der Zirbeldrüse zirkadian synthetisiert wird und nachts und unter der Kontrolle des suprachiasmatischen Kerns seinen Höhepunkt erreicht [22], ist sowohl ein Marker als auch ein Regulator des zirkadianen Rhythmus und des Schlafs [21]. Veränderungen in der Melatoninsynthese und der Expression der MT1- und MT2-Rezeptoren wurden bei Patienten mit Stimmungsstörungen berichtet, z. B. wird der MT1-Rezeptor mit angstähnlichen und zwanghaften Verhaltensweisen in Verbindung gebracht und der MT2-Melatoninrezeptor wird mit depressiven Verhaltensweisen in Verbindung gebracht. ähnliches Verhalten und könnte eine Rolle bei der Pathologie einer schweren Depression spielen [21,23]. Die Medikamente, die bei FMS verwendet werden, sind Antidepressiva, Entzündungshemmer, Muskelrelaxantien und Beruhigungsmittel-Hypnotika. Studien, in denen mehrere Medikamente kombiniert wurden (Milnacipram + Pregabalin oder Paracetamol + Tramadol), verbesserten die Krankheitssymptome [24,25]. Melatonin allein oder in Kombination mit Antidepressiva kann an der Veränderung des endogenen schmerzmodulierenden Systems bei Fibromyalgie beteiligt sein [26]. Eine dieser Strategien besteht darin, auf Melatoninrezeptoren abzuzielen, da Melatonin eine Schlüsselrolle bei der Synchronisierung zirkadianer Rhythmen spielt, die bekanntermaßen in depressiven Zuständen gestört sind, und daher auch im therapeutischen Ansatz bei FMS berücksichtigt werden kann [27,28].
2. Rolle von Melatonin bei Fibromyalgie
Melatonin ist ein niedermolekulares Indolamin (N-Acetyl-5-methoxytryptamin), das aus der Aminosäure L-Tryptophan synthetisiert wird und in Tieren, Pflanzen und sogar einzelligen Organismen vorkommt. Melatonin wird in der Hauptzelle der Zirbeldrüse, dem Pinealozyten, produziert und bei Säugetieren über Umgebungslicht gesteuert. Trotz seiner einfachen Struktur ist Melatonin ein starkes endogenes Antioxidans [29]. Darüber hinaus ist es an der Kontrolle der Fortpflanzung [30], der Immunmodulation [31] und biologischen Rhythmen [32] beteiligt, verbessert die Stimmung [33] und besitzt entzündungshemmende Wirkungen [34,35].

2.1. Rezeptorvermittelte Wirkungen von Melatonin und seine Beteiligung an Fibromyalgie
Viele der Wirkungen von Melatonin werden durch die G-Protein-gekoppelten Rezeptoren MT1 und MT2 vermittelt. Es ist auch bekannt, dass Melatonin an das Enzym Chinonreduktase II bindet, das zuvor als MT3-Rezeptor definiert wurde. Funktionell haben MT1 und MT2 unterschiedliche physiologische Rollen. Beispielsweise vermittelt MT1 die Melatonin-regulierte kardiale Vasokonstriktion [36,37], während die MT2-Aktivierung die Herzgefäße erweitert und Entzündungs- sowie Immunreaktionen moduliert [38]. Eine neuere Studie zeigte, dass MT1 möglicherweise auch die Genexpression im Zusammenhang mit der biologischen Uhr moduliert, da die Expression der meisten Uhrgene in der Hypophyse von MT1-Knockout-Mäusen verringert ist, nicht jedoch von MT2-Knockout-Mäusen [39]. Melatonin fungiert als natürlicher Ligand für die Retinoid-verwandte Orphan-Nuclear-Hormon-Rezeptor-Familie [40,41]. Die immunmodulatorischen Wirkungen und möglicherweise auch ein Teil der zirkadianen Wirkungen werden teilweise durch die Melatoninaktivierung von Kernrezeptoren vermittelt, die die 5-Lipoxygenase-mRNA-Expression in menschlichen B-Zelllinien unterdrücken [42]. Darüber hinaus kann Melatonin durch die Bindung an intrazelluläre Proteine wie Calmodulin aktiviert werden, das an der Signalübertragung von Second Messenger beteiligt ist; Dies wirkt der Bindung von Calmodulin an Ca2+ direkt entgegen [43]. Schließlich hat Melatonin wichtige antioxidative Wirkungen, die ausführlich bei verschiedenen pathologischen Zuständen im Zusammenhang mit freien Radikalen und verwandten Reaktanten untersucht wurden, wie z. B. Ischämie/Reperfusion, Entzündung, ionisierende Strahlung und mitochondriale Toxine [44,45]. Es wurde vermutet, dass Melatonin auch das Abfangen freier Radikale durch einen nichtenzymatischen Prozess der Elektronenspende verstärkt [46,47].
2.2. Wechselwirkung von Melatonin mit Rezeptoren, die an den Schmerzen bei FMS beteiligt sind
Da sowohl die Melatoninsekretion als auch die Schmerzwahrnehmung einem zirkadianen Rhythmus folgen, haben viele Forscher bestätigt, dass Melatonin eine wesentliche Rolle bei der Schmerzregulierung unter physiologischen Bedingungen spielt [48,49]. Beispielsweise benötigen Melatonin-MT2-Rezeptor-Agonisten die Aktivierung des Mu-Opioid-Rezeptors (MOR), um ihre antiallodynischen Wirkungen auszuüben, d des Hirnstamms [50,51].
-Endorphine, Gamma-Aminobuttersäure (GABA)-Rezeptoren, der Stickoxid (NO)-Arginin-Weg und Opioid-1-Rezeptoren können alle an Melatonin-vermittelten analgetischen Wirkungen beteiligt sein. Melatonin kann die Funktion von GABA-Rezeptoren modulieren [52] und die GABA-Konzentration um 50 % erhöhen [53]. Melatonin erhöht die Freisetzung von Endorphinen aus der Hypophyse, deren Antagonist auch die durch Melatonin induzierte antinozizeptive Wirkung hemmen kann [54,55]. Darüber hinaus kann eine durch Melatonin induzierte Langzeitanalgesie durch Naloxon antagonisiert werden [56]. Die Expression von MOR-mRNA folgt einem zirkadianen Muster, wobei MORs während der späten Lichtphase stärker und während der Dunkelphase weniger exprimiert werden. Bei den MT2-/−-Knockout-Mäusen könnte das Fehlen eines endogenen MT2-Tonus neuronale Kompensationsmechanismen durch eine erhöhte Penk-mRNA-Expression im rostralen ventromedialen Medulla (RVM) aktivieren, was zu einer Hochregulierung des endogenen Opioid-Enzephalins auf der zentralen Ebene führt, die daran beteiligt ist die Modulation des Schmerzes. Diese Ergebnisse könnten die Hypothese bestätigen, dass der MT2-Rezeptor eine spezifische Rolle bei der Nozizeption spielt, insbesondere während der inaktiven Phase (am Tag), wenn MT2 im Gehirn häufiger vorkommt. Daher könnte die erhöhte Empfindlichkeit von MT2–/– während der Nacht mit der geringen Verfügbarkeit von MORs in diesen Bereichen des absteigenden antinozizeptiven Signalwegs zusammenhängen [57]. Es wurde festgestellt, dass Melatonin entzündliche Schmerzen lindert, wahrscheinlich indem es die Produktion von NO durch die induzierbare NO-Synthase und die Signalübertragung von NO-zyklischem GMP blockiert [58,59]. Melatonin kann auch seine analgetische Wirkung vermitteln, indem es mit benzodiazepinergen, muskarinischen, nikotinischen, serotonergen und einem sowie zwei adrenergen Rezeptoren im Zentralnervensystem und im Hinterhorn des Rückenmarks interagiert. Seine antinozizeptive Wirkung kann auch durch Beeinflussung des Sigma-Systems, des dopaminergen Rezeptors und des glutamatergen Rezeptors (NMDA-Typ) hervorgerufen werden [60,61]. Die Wirksamkeit von Melatonin als Analgetikum und Anxiolytikum wurde in verschiedenen Schmerztiermodellen nachgewiesen, was zu seinem therapeutischen Einsatz bei einer Vielzahl von Erkrankungen führte, was auf seinen klinischen Nutzen bei der Behandlung mittelschwerer chronischer Schmerzen [62] und Entzündungen [63] schließen lässt. saisonale affektive Störung und Schlafstörungen [64]. Darüber hinaus hemmt Melatonin den physiologischen Prozess der Blutplättchenaggregation sowie die Freisetzung von ATP und Serotonin [65], was zu einer nächtlichen Veränderung der Empfindlichkeit menschlicher Blutplättchen gegenüber Melatonin führt [66]. Die maximale Wirkung von Melatonin auf die Thrombozytenaktivität geht dem Höhepunkt der Melatoninkonzentration voraus [65]. Bei Fibromyalgie wurde über eine höhere Expression von Fibrinogen und Veränderungen in der Blutplättchenverteilung berichtet [67].
2.3. Einfluss von Melatonin auf die Verbesserung der Veränderung des zirkadianen Rhythmus bei FMS
Melatonin ist an der Synchronisierung des zirkadianen Rhythmus und damit an der Regulierung von Müdigkeit und Schlaf-Wach-Rhythmen beteiligt [68]. Es steigert auch die endogenen Schmerzhemmungsmechanismen und die Stimmung. Daher sind die physiologischen Prozesse, die durch die Verfügbarkeit von Melatonin aufrechterhalten werden, entscheidend für die klinischen Symptome von FMS, einschließlich kognitiver Beeinträchtigung, Erschöpfung, anhaltender Schmerzen und Schlafstörungen. Niedrige Serotonin- und Tryptophanspiegel, die Vorläufer von Melatonin, wurden mit einer Vielzahl von Symptomen bei FMS-Patienten in Verbindung gebracht, was zu der Schlussfolgerung führte, dass Melatonin möglicherweise eine Rolle bei der Ätiologie von FMS spielt [1,69].

Obwohl mehrere Studien die Krankheit aus unterschiedlichen Blickwinkeln analysiert haben [70–74], basierend auf der zirkadianen Fähigkeit von Melatonin und seiner Auswirkung auf den Schlaf-Wach-Zyklus, haben Zannette et al. entwarfen eine doppelblinde, randomisierte, kontrollierte Studie zur Beurteilung von Indolamin bei FMS-Patienten [26].
Die Polysomnographie ist der „Goldstandard“ für die Schlafbeurteilung, aber Aktivität wird seit mehr als 25 Jahren zur Beurteilung des Schlaf-Wach-Verhaltens und zur Erfassung von Bewegungsdaten eingesetzt [75–78]. Die American Sleep Disorders Association hat die Verwendung von Aktivität mit einer Genauigkeit von 86 % als gültige Methode zur Bewertung spezifischer Bereiche der Schlafforschung und Schlafmedizin etabliert [79]. Daher haben und nutzen viele Forscher diese Methode im Bereich FMS [80–82].
Einige Studien haben gezeigt, dass Schlaf-Wach-Störungen, darunter frühes Erwachen, Schlaflosigkeit, nicht erholsamer Schlaf und schlechte Schlafqualität, bei einem hohen Prozentsatz der FMS-Patienten [83] durch Defekte in der Produktion der Vorläufer Tryptophan und Serotonin verursacht werden könnten von Melatonin [84], was eine geringere Melatoninsynthese während der Nacht erklären könnte. In einem longitudinalen, placebokontrollierten Design [77] lag die wirksamste Melatonin-Dosis (in Bezug auf die Gesamtzahl der verbesserten Parameter) nach Auswertung der chronobiologischen Parameter des Schlafs für 10 Tage im Bereich von 6 bis 15 mg Eine Verbesserung wurde bei sechs von sieben analysierten Schlafparametern (angenommener Schlaf, Immobilität, tatsächliche Schlafzeit, Schlafeffizienz, Schlaflatenz und gesamte nächtliche Aktivität) erzielt, wenn eine Dosis von 15 mg Melatonin pro Tag verabreicht wurde [77]. Dennoch deuten zwei Pilotstudien darauf hin, dass die Einnahme von 3 mg Melatonin pro Tag über 30 Tage und 6 mg/Tag über 10 Tage die Schlafstörungen verbesserte [85,86]. Folglich können die zwischen den Studien festgestellten Unterschiede mit den klinischen Profilen der Patienten und den Unterschieden im Versuchsdesign oder der Behandlungsdauer (30–60 Tage gegenüber 10 Tagen) zusammenhängen. Tabelle 1 fasst diese Studien zusammen.
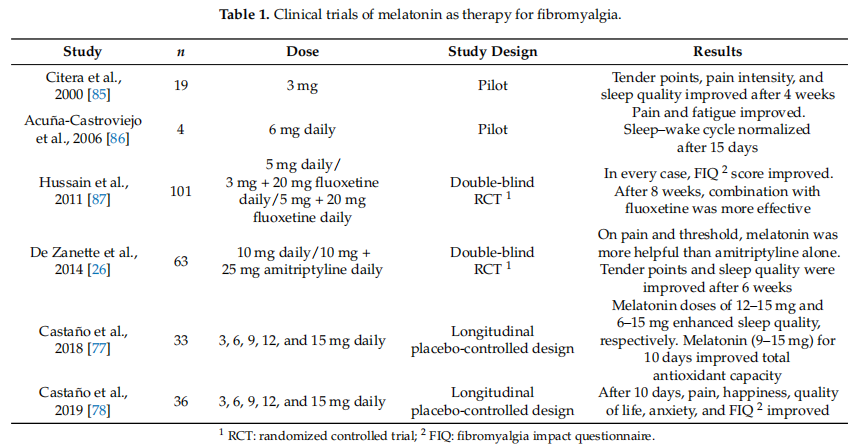
Die mit Aktivität erzielten Ergebnisse wurden durch diejenigen bestätigt, die durch die subjektive Schlafanalyse mithilfe des Pittsburgh Sleep Quality Index (PSQI) ermittelt wurden. Dieser Fragebogen wird häufig zur Messung der Schlafqualität und von Schlafstörungen verwendet [88–90]. Die spanische Version dieses Fragebogens ist ein wirksames Instrument zur Messung der subjektiven Wahrnehmung der Schlafqualität bei spanischen Patienten mit FMS [90]. Castaño et al. zeigten, dass die Wahrnehmung der Patienten über ihre Schlafqualität positiv war, nachdem sie 10 oder 15 Tage lang 6 mg Melatonin eingenommen hatten [77,78], und sie stimmten mit anderen Studien überein [87]. Mit zunehmender Melatonin-Dosis wurden bessere Ergebnisse in Form einer längeren Nachtruhe beobachtet.
Wichtig ist, dass die Unterschiede in den Ergebnissen, die nach der Bewertung der Schlafqualität anhand der Aktivität und des PSQI erzielt wurden, darauf zurückzuführen sein könnten, dass Melatonin als chronobiotische Chemikalie fungiert und an Schmerzwegen beteiligt ist. Der Melatoninspiegel bei FMS-Patienten ist verändert, mit einer geringeren Sekretion während der dunklen Stunden und einer erhöhten Sekretion während des Tages [91]. Veränderungen in der Melatoninsekretion verändern den zirkadianen Rhythmus und die Schlafarchitektur, was depressive Symptome, Müdigkeit und Schmerzen verschlimmern kann, während die Fähigkeit, sie zu regulieren, verdeckt wird [92].
2.4. Auswirkungen von Melatonin auf Schmerzen und Schlafqualität bei FMS
Melatonin wurde aufgrund seiner analgetischen, anxiolytischen und chronotropen Eigenschaften als potenzielle Behandlung für FMS vorgeschlagen [33,52,84,85]. Zuvor war Melatonin bei der Behandlung von Schlafstörungen bei schweren depressiven Störungen wirksam, wenn es in langsam freisetzender Form zusammen mit der Standard-Antidepressivum-Behandlung mit Fluoxetin eingesetzt wurde [93]. Andererseits hat sich Ramelteon, das eine hohe Selektivität für MT1/MT2-Rezeptoren und eine geringe Affinität für andere Rezeptoren, wie unter anderem Opioide, aufweist, bei Schlaflosigkeitssymptomen bei generalisierten Angststörungen als nützlich erwiesen [94]. Auch bei saisonalen Depressionen (SAD), wie z. B. der Winterdepression, die eine zirkadiane Komponente hat, wird die Gabe von Melatonin am Nachmittag neben dem hellen Morgenlicht empfohlen, nicht nur zur Behandlung von Schlafstörungen aufgrund von Störungen des zirkadianen Rhythmus, sondern auch wegen eine antidepressive Wirkung [95]. Es erscheint sinnvoll, neue Studien zur Bewertung der therapeutischen Indikation von Melatonin bei nicht-saisonaler Depression sowie anderen Schlaf- und psychiatrischen Störungen vorzuschlagen, in denen eine möglicherweise vorhandene zirkadiane Komponente analysiert werden kann [95] für die Implementierung einer Melatoninbehandlung als Koadjuvans zu FMS. Die Behandlung von FMS mit Melatonin kann die Symptome verbessern, indem sie die Synchronisation des zirkadianen Rhythmus reguliert und die Schmerzwege und/oder die Mengen an Signalmolekülen, die den Schmerz steuern, direkt beeinflusst [24,49,77,78]. Wenn Melatonin die Schmerzen bei FMS-Patienten lindern kann, führt dies wahrscheinlich zu einer besseren Schlafqualität für sie. Daher sind weitere randomisierte kontrollierte Studien erforderlich, um diesen Aspekt zu klären.
Die numerische Schmerzskala, die in der klinischen Praxis häufig verwendet wird, ergab, dass die von den Patienten wahrgenommene Schmerzintensität nach der Einnahme von Melatonin in einem Dosisbereich von 3 mg/Tag bis 15 mg/Tag über einen Zeitraum von 10 Tagen deutlich abnahm Erzielung einer dosisabhängigen Wirkung [78]. Somit könnte die Schmerzabnahme mit einem Anstieg des zirkulierenden Melatonins zusammenhängen, indirekt gemessen als 6-Sulfatoxymelatonin (aMT6-s) im Urin, dem Hauptmetaboliten von Melatonin im Urin, der das nächtliche Plasmamelatonin genau widerspiegelt [96]. ]. Die analgetische Wirkung von Melatonin wurde bei FMS-Patienten bestätigt, jedoch mit längeren Behandlungsdauern: 3 mg/Tag für 30 Tage [85]; 5 mg/Tag für 8 Wochen [86]; und 10 mg/Tag für 6 Wochen [26].

Eine erhöhte Nozizeption kann mit einer veränderten Melatoninproduktion bei FMS-Patienten verbunden sein, die sich klinisch als Hyperalgesie und/oder Allodynie manifestieren kann [60,84,91]. Studien zur Kombinationstherapie mit Melatonin und Fluoxetin [87] oder Amitriptylin [26] haben weitere Beweise für die Wirksamkeit von Melatonin bei der Behandlung von FMS geliefert und den Bedarf an zusätzlicher Forschung zu anderen Begleitmedikamenten verstärkt. Die Daten zur Kombinationstherapie reichen jedoch nicht aus, um die optimalen Alternativen zu bestimmen, und es sind weitere Untersuchungen erforderlich, um diese Möglichkeit bei FMS zu ermitteln [12].
2.5. Zusammenhang zwischen Melatonin und Cortisol bei Fibromyalgie-Symptomen
Die Wahrnehmung einer verbesserten Stimmung und körperlichen Verfassung bei Patienten mit FMS, bestimmt durch den auf der visuellen Analogskala (VAS) erhaltenen Score, war nach Melatonin (15 mg) im Vergleich zu den Grundbedingungen erhöht [78]. Melatonin und Cortisol sind an der Regulierung der Stimmung und der Modulation von Schmerzen und Angstzuständen beteiligt [33,91,97]. Die Auswirkungen auf die Stimmung könnten zumindest teilweise auf die Einnahme von Melatonin zurückzuführen sein. Im Allgemeinen weisen Patienten mit FMS ein hohes Maß an Angstzuständen und depressiven Symptomen auf, die zu einer verstärkten Schmerzwahrnehmung und Somatisierung der Symptome beitragen und ihre Lebensqualität stark beeinträchtigen [98]. Nach der Melatoninbehandlung von 3 mg/Tag auf 15 mg/Tag war die „State-Anxiety“, also die Angst, die ein Proband vorübergehend hat, im Vergleich zu der Angst, die der Proband zu Studienbeginn zeigte, reduziert [77]. Allerdings blieb die „Trait-Anxiety“, also die Angst, die als latentes Merkmal des Subjekts gilt, unverändert. Die Einnahme von Melatonin trug bei diesen Patienten zum Ausgleich von Ungleichgewichten in der Hypothalamus-Hypophysen-Nebennieren-Achse (HPA) bei [99], was auch das Stress- und Angstniveau beeinflusst [100,101].
Bei Patienten mit FMS wurden nicht nur Veränderungen im Muster der Melatoninsekretion, sondern auch im Serotonin- und Cortisolmuster festgestellt [28]. Auf physiologischer Ebene ist bei gesunden Menschen die Melatoninkonzentration tagsüber niedrig und der Cortisolspiegel hoch, und umgekehrt. Bei FMS-Patienten ist dieser Zusammenhang umgekehrt, sodass sie tagsüber im Allgemeinen ungewöhnlich niedrige Cortisolspiegel aufweisen. Somit könnte die Melatoninbehandlung bei diesen Patienten dazu beigetragen haben, Ungleichgewichte in der HPA-Achse auszugleichen. Kürzlich reduzierte Melatonin (9–15 mg für zehn Tage) dosisabhängig die Cortisolkonzentration im Urin [78]. Obwohl hinsichtlich der Cortisolspiegel bei Patienten mit FMS aufgrund der hohen Variabilität der Cortisol-Probenentnahmemethoden und der unterschiedlichen Entnahmezeiten immer noch Uneinigkeit besteht, kommt es bei Patienten mit FMS zu einer Dysregulation der HPA-Achse [102–106]. Wenn der Cortisolspiegel im Morgenurin der ersten Urinprobe gemessen wird, werden die Werte ermittelt, die die Person in der Nacht zuvor hatte. Nach der Auswertung des Cortisolspiegels im Urin und im Serum wurden bei Patienten mit FMS niedrigere Werte am Morgen im Vergleich zur Kontrollgruppe ermittelt [107,108]. Andererseits haben Mahdi et al. (2011) fanden nachts erhöhte Cortisolkonzentrationen im Serum [28]. Castaño et al. beobachteten Verbesserungen des Angstniveaus, der Stimmung, der Schmerzen und der Lebensqualität nach der Verabreichung von Melatonin [78]. Da Melatonin eine hemmende Wirkung auf die Sekretion von Cortisol ausübt [109], scheint es vernünftig, dass die Wiederherstellung beider veränderter Spiegel die Chronodisruption verbessern kann. Bei der Verabreichung von Melatonin in der Nacht deuten die Daten darauf hin, dass der Cortisolspiegel morgens niedrig ist, was als vielversprechendes Ergebnis angesehen werden kann, da die Verabreichung von exogenem Melatonin dazu beitrug, den ungewöhnlich hohen Cortisolspiegel in der Nacht bei diesen Patienten zu senken .
Um die Wirksamkeit einer angemessenen Behandlung dieser Krankheit zu bestimmen, müssen alternativ nicht nur die erzielten Vorteile in Bezug auf Angstzustände, emotionale Verfassung, Schmerzen und/oder Schlaf bewertet werden, sondern auch die Auswirkungen, die sie auf die Lebensqualität eines Menschen haben geduldig. In diesem Sinne ist der Fibromyalgie-Auswirkungsfragebogen (FIQ) am weitesten verbreitet. Castaño et al. ergab, dass die Verabreichung von 9, 12 und 15 mg Melatonin die FIQ-Werte verbesserte [78]. Bemerkenswert ist, dass ein kurzer Zeitraum (nur 10 Tage für jede Dosis) erforderlich war, um die positiven Wirkungen von Melatonin zu beobachten. De Zanette et al. [26] zeigten, dass 10 mg Melatonin pro Tag über 6 Wochen auch die FIQ-Werte verbesserten. Andere Autoren stellten einen signifikanten Rückgang der Gesamt-FIQ-Werte bei niedrigeren Melatonin-Dosen, z. B. 5 mg/Tag, fest, dafür waren jedoch längere Verabreichungszeiträume von 8 Wochen erforderlich [86].
Der SF-36-Fragebogen (SF-36) liefert Informationen zur gesundheitsbezogenen Lebensqualität und klassifiziert diese in verschiedene Dimensionen (körperliche Funktion, soziale Funktion, Rolle – körperlich, Rolle – emotional, Vitalität, Körperschmerz). , psychische Gesundheit und allgemeine Gesundheit). Es hat sich gezeigt, dass die Verabreichung von Melatonin in einer Dosierung von 9 mg/Tag über 10 Tage vier der acht vom SF-36 bewerteten Dimensionen verbessert. Nach 15 mg/Tag über 10 Tage verbesserten sich alle bewerteten Dimensionen deutlich. Mit anderen Worten: Alle Patienten gaben an, dass sich ihr emotionaler und gesundheitlicher Zustand, ihre sozialen Beziehungen und ihre Vitalität verbessert hätten [78]. Die Ergebnisse mehrerer Fragebögen sind in Tabelle 2 zusammengefasst.

Als starke Entzündungshemmer könnten Glukokortikoide eine therapeutische Wirkung bei Fibromyalgie haben [110]. Die wichtigsten klinischen Merkmale (Müdigkeit und Schmerzen) sind eher mit gestörten Glukokortikoidrezeptor-Signalwegen als mit einer Abnahme der Glukokortikoidkonzentrationen verbunden, da die Verringerung der Glukokortikoidempfindlichkeit mit einer erhöhten Häufigkeit von Müdigkeit einhergeht [110]. Müdigkeit, Schmerzen, Kopfschmerzen, Gehirnnebel, Stimmungs- und Schlafstörungen sind unter anderem Symptome, die bei Post-COVID-19-Patienten häufig auftreten. Diese Symptome könnten als Manifestationen einer zentralen Sensibilisierung angesehen werden [111]. Müdigkeit ist eines der Hauptsymptome bei Störungen, die mit zentraler Sensibilisierung in Zusammenhang stehen [112], was zu der Hypothese führt, dass zentrale Sensibilisierung eine zugrunde liegende häufige Ursache bei chronischen Schmerzpatienten und Patienten mit Post-COVID-Erkrankungen sein könnte [113] . Aufgrund der Ähnlichkeiten zwischen Enzephalomyelitis/chronischem Müdigkeitssyndrom, FMS und Post-COVID-Syndrom wird ein gemeinsamer pathogener Mechanismus vermutet [114].
Bei Fibromyalgie wird vermutet, dass das Gleichgewicht zwischen entzündungsfördernden und entzündungshemmenden Zytokinen zugunsten entzündungsfördernder Zytokine gestört ist. Zytokine werden sowohl von Immunzellen (Monozyten, T-Zellen und Makrophagen) als auch von Nichtimmunzellen (Schwann-Zellen, Fibroblasten, Mikroglia und Astrozyten) freigesetzt [115,116]. Mehrere Genvarianten sollen mit der Zytokinfreisetzung und dem Entzündungszustand bei FMS assoziiert sein [117–119].
2.6. Melatonin und seine bedeutende antioxidative Rolle bei FMS
Es wurde vermutet, dass eine Verringerung der oxidativen Kapazität an der Pathophysiologie von FMS beteiligt ist [120,121]. Das Gleichgewicht zwischen Oxidationsmitteln und Antioxidantien kann bei dieser Krankheit wichtig sein. Die gesamte antioxidative Kapazität im Urin, bestimmt im Serum von FMS-Patienten, erhöhte sich mit einer dosisabhängigen Wirkung bei Melatonin-Dosen von 9, 12 und 15 mg/Tag über 10 Tage [77]. Unter Berücksichtigung der bekannten antioxidativen Eigenschaften von Melatonin können diese Effekte auf erhöhte zirkulierende Melatoninkonzentrationen bei diesen Patienten zurückgeführt werden. Die größten antioxidativen Wirkungen fielen mit dem größten Anstieg der aMT6-s-Spiegel zusammen [77].
Darüber hinaus stieß die Identifizierung der Melatonin-Bindungsstelle MT3 als Chinonreduktase QR2 (NQO2) [122], ein mutmaßlicher „Rezeptor“, der im Gehirn von Säugetieren vorkommt [123], auf zunehmendes Interesse. Auf diese Weise wurde dieser Befund aus der Beobachtung einer Bindungsstelle [122] und mittels isothermer Titrationskalorimetrie [123] sowohl in zentralen als auch peripheren Hamstergeweben sowie durch die Cokristallisation des menschlichen Enzyms NQO2 mit Melatonin [124,125] ermittelt. stellt ein ursprüngliches Bindungsprofil und eine sehr schnelle Kinetik des Ligandenaustauschs im Vergleich zu den beiden Melatonin-G-gekoppelten Rezeptoren MT1 und MT2 dar [122]. Die oxidoreduktiven Eigenschaften von QR2 markieren die Methode für eine beginnende enzymatische Untersuchung der antioxidativen Funktion von Melatonin. Dieses Enzym ist nach MT1, MT2 und der Transferase Arylalkylamin-N-Acetyltransferase das vierte molekulare Ziel zur Erforschung der vielfältigen Facetten der Melatoninwirkung steuert die Melatonin-Biosynthese [122]. Die mögliche Fähigkeit von MT3-Bindern, QR2 zu hemmen, könnte an mehreren wichtigen pathologischen Zuständen beteiligt sein, insbesondere an der QR2-abhängigen Produktion radikalischer Sauerstoffspezies, die weiterer Erforschung bedarf. Es wurde vermutet, dass pharmakologische Melatoninkonzentrationen von etwa 100 µM und mehr die QR2-Aktivität hemmen können, die als der zuvor genannte mitochondriale Komplex I, auch NADH genannt, gilt: Ubiquinonoxidoreduktase [126]. Daher könnte die mögliche Rolle von MT3/QR2 bei der mitochondrialen Dysfunktion aufgrund von oxidativem Stress eine Rolle bei der Ätiologie von FMS spielen.
2.7. Oxidativer Stress und Neuroinflammation bei FMS
Fibromyalgie kann als zentrales Sensibilisierungssyndrom angesehen werden, da ihr vorherrschender pathogener Mechanismus die Veränderung der Schmerzregulation auf Gehirnebene ist [127]. Neuronale Zellen sind anfällig für Angriffe reaktiver Sauerstoffspezies und Lipidperoxidation. Mehrere Studien haben erhöhte Werte an Markern für oxidativen Stress bei FMS gezeigt [128,129]. Mitochondriale Dysfunktion, beeinträchtigte Bioenergetik und verringerte antioxidative Enzymspiegel gelten als zugrunde liegende Faktoren für oxidativen Stress und Entzündungen bei FMS. Zentrale Neuroinflammation, die durch erhöhte Konzentrationen an Zytokinen und neurotrophen Faktoren in der Liquor cerebrospinalis ausgelöst wird, und zentrale Sensibilisierung stehen bei FMS in engem Zusammenhang [129]. Substanz P, aus dem Gehirn stammender neurotropher Faktor, Glutamat, Nervenwachstumsfaktor und mehrere Entzündungsmediatoren aktivieren Gliazellen, die proinflammatorische Zytokine produzieren, die zu einer Neuroinflammation führen. Dieses Phänomen erhöht die zentrale Verarbeitung nozizeptiver Eingaben und trägt zu chronischen Schmerzen, Allodynie und Hyperalgesie bei FMS bei. Als Beweis für eine zentrale Neuroinflammation ist die intrathekale Konzentration von IL-8 bei Fibromyalgie-Patienten im Vergleich zu gesunden Kontrollpersonen erhöht [130] und könnte mit der Aktivierung von Gliazellen zusammenhängen. Die erhöhte IL-8-Konzentration bei fehlendem IL-1-Anstieg weist darauf hin, dass die Symptome bei FMS durch das sympathische Nervensystem und nicht durch Prostaglandin-bezogene Signalwege vermittelt werden [130,131]. Exogenes Melatonin reduzierte die Konzentration der Entzündungsmarker IL-1, 6 und 8 sowie TNF und wurde als nützliches Instrument zur Prävention und adjuvanten Behandlung von Entzündungserkrankungen vorgeschlagen [132].
【Für weitere Informationen:george.deng@wecistanche.com / WhatsApp:8613632399501】






