Teil Ⅱ Identifizierung und Validierung einer immunbezogenen Genpaarsignatur für drei urologische Krebsarten
May 06, 2023
Ergebnisse
1. Etablierung und Evaluierung des IRGPI
Insgesamt wurden 2,700 Patienten mit drei urologischen Krebsarten, darunter 835 Blasenkrebs-, 888 Prostatakrebs- und 977 Nierenkrebspatienten, in diese Studie einbezogen. Wie in der ergänzenden Abbildung 1 dargestellt, wurden 1.622 Patienten in TCGA-Kohorten als Meta-Trainingsdatensatz verwendet. Weitere 1.{81}}78 Patienten aus sieben GEO-Datensätzen und zwei ICGC-Datensätzen bildeten den Metavalidierungsdatensatz. Unter 2.483 IRGs aus der ImmPort-Datenbank wurden 606 IRGs auf allen Plattformen gemessen und erfüllten die Kriterien (MAD > 0.5) in allen unabhängigen Trainingssätzen. Basierend auf 606 IRGs wurden 183.315 IRGPs gebaut. Nach dem Entfernen derjenigen, die nicht in allen Datensätzen geteilt wurden oder in keinem Datensatz eine konstante Reihenfolge hatten, blieben 18.041 IRGPs übrig und wurden für die weitere Analyse ausgewählt. Zunächst wurden 10.943 IRGPs mithilfe des univariaten Cox-Regressionsmodells im Meta-Trainingsdatensatz herausgefiltert. Um IRGP-Kandidaten weiter zu prüfen, wurde LASSO 30 Mal durchgeführt, um aus 30 Analysen diejenigen auszuwählen, die mehr als 15 Mal vorkamen. Als Ergebnis wurden 25 IRGPs und 41 einzigartige IRGs ausgewählt. Anschließend wurde das multivariate Cox-Regressionsmodell verwendet, um das IRGPs-basierte Vorhersagemodell zu erhalten und IRGPI-Scores für alle Stichproben zu generieren. Die Patienten in der Meta-Trainingskohorte wurden mithilfe des mittleren IRGPI (-1.216973) in Gruppen mit niedrigem und hohem Immunrisiko eingeteilt. Es gab deutlich unterschiedliche RFS-Prognosen zwischen Niedrig- und Hochrisikogruppen in der Meta-Trainingskohorte (Abbildung 1A, Hazard Ratio [HR] 6,078, 95-Prozent-Konfidenzintervall [CI] 4,754-7,769). ; P < 2×10-16). Der IRGPI könnte auch Patienten in Untergruppen mit signifikant unterschiedlichem RFS in der Trainingskohorte für Blasenkrebs einteilen (Abbildung 1B, HR 2,308, 95 Prozent KI 1,660- 3,210; P=3×{{55} } ), Prostatakrebs (Abbildung 1C, HR 3,054, 95 Prozent KI 1,778-5,245; P=2×10-5 ) und Nierenkrebs (Abbildung 1D, HR 5,582, 95 Prozent). CI 3.899-7.992; P < 2×10-16). Die zeitabhängigen ROC-Kurven wurden verwendet, um die Fähigkeit des IRGPI zur Vorhersage der Prognose zu bewerten. Die Werte der Fläche unter der Kurve (AUC) zur Vorhersage des 1--, 3--, 5-- und 10-jährigen RFS der Patienten betrugen 0,816, 0,818, 0,828 bzw. 0,763. in der Meta-Trainingskohorte (ergänzende Abbildung 2A). Bei der Stratifizierung der Patienten nach verschiedenen Tumorstadien, Geschlechtern und Altersgruppen blieben die Gruppen mit niedrigem und hohem IRGPI für RFS signifikant unterschiedlich, und ein höherer IRGPI-Wert war mit einer deutlich schlechteren Prognose verbunden (Abbildung 2). Die Patienten mit hohem IRGPI und fortgeschrittenem Tumorstadium hatten das höchste RFS unter allen Patienten in der Meta-Trainingskohorte (ergänzende Abbildung 2B). Multivariate Analysen legten nahe, dass der IRGPI nach Anpassung an Alter und Stadium ein unabhängiger Prognosefaktor war (HR 4,22, 95 Prozent KI 3,23- 5,52; P < 2×10-16).

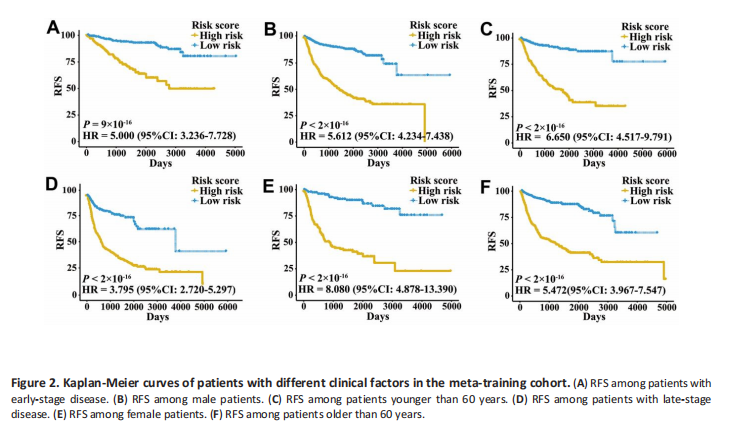
2. Validierung des IRGPI
Externe Validierungskohorten wurden verwendet, um die Fähigkeit des IRGPI zu bestätigen, das RFS von Patienten mit drei urologischen Krebsarten in verschiedenen Populationen vorherzusagen. Zur Berechnung des IRGPI wurden dieselben IRGPs verwendet, und die Patienten wurden außerdem in Gruppen mit niedrigem und hohem Risiko eingeteilt. Das RFS von Patienten in Gruppen mit niedrigem und hohem IRGPI unterschied sich in der Metavalidierungskohorte signifikant (Abbildung 3A, HR 3,326, 95 Prozent KI 2,623-4,217; P < 2×10-16), Validierung Datensatz von Blasenkrebs (Abbildung 3B, HR 3,987, 95 Prozent KI 2.641-6.019; P=1×{{20}}), Validierungsdatensatz von Prostatakrebs (Abbildung 3C, HR 3,277, 95 Prozent KI 2,275-4,719; P=2×10-11) und Validierungsdatensatz von Nierenkrebs (Abbildung 3D, HR 2,523, 95-Prozent-KI 1.529-4.165; P=2×10-4 ). Zeit-ROC-Kurven zeigten stabile Vorhersagefähigkeiten mit {{40}}-, 3--, 5-- und 10-Jahres-AUCs von 0.794. 0,764, 0,739 bzw. 0,605 (Ergänzende Abbildung 2C). In ähnlicher Weise hatten die Patienten mit hohem IRGPI und fortgeschrittenem Tumorstadium das höchste RFS unter den Patienten in der Metavalidierungskohorte (ergänzende Abbildung 2D). In Übereinstimmung mit den Trainingskohorten konnte das IRGPI Patienten in weitgehend unabhängigen Validierungskohorten hinsichtlich des RFS in deutlich unterschiedliche Gruppen einteilen (ergänzende Abbildung 3). Bei der Betrachtung von Patienten mit der Erkrankung im frühen oder letzten Lebensalter, männlichen Patienten und Patienten über 60 Jahren blieb der IRGPI hoch prognostisch und ein höherer IRGPI-Score war mit einer deutlich schlechteren Prognose verbunden (Abbildung 4). Nach Anpassung an Alter und Stadium in Cox-Regressionsanalysen blieb der IRGPI ein unabhängiger Prognosefaktor in der Metavalidierungskohorte (HR 2,15, 95 Prozent KI 1,45-3,19; P=0,000149; ).


3. Funktionsanalyse und infiltrierende Immuninhalte im Zusammenhang mit dem IRGPI
Die 41 einzigartigen IRGs, die für den IRGPI in der Meta-Trainingskohorte relevant sind, waren hauptsächlich an der Immun- und Entzündungsreaktion, der Zytokinaktivität und der Chemotaxis beteiligt (Abbildung 5). Verschiedene Immuninfiltrate wurden in der Meta-Trainingskohorte angereichert, und Makrophagen M2, T-Zellen CD8, T-Zellen CD4-Gedächtnisruhe, Makrophagen M0 und Makrophagen M1 zeigten eine höhere Häufigkeit (Abbildung 6A). Unter diesen unterschieden sich die Prozentsätze der Makrophagen M0, Makrophagen M1 und Makrophagen M2 deutlich zwischen den IRGPI-Risikogruppen (Abbildung 6B). Darüber hinaus wurden diese Ergebnisse in den Metavalidierungskohorten validiert, in denen dieselben fünf Immuninfiltrate mit einer höheren Immunzellhäufigkeit angereichert wurden (Abbildung 6C). Auch die Prozentsätze der Makrophagen M1 und Makrophagen M2 unterschieden sich deutlich zwischen den IRGPI-Risikogruppen (Abbildung 6D).


4. Nomogramm basierend auf dem IRGPI und klinischen Faktoren
Die univariate Cox-Regressionsanalyse zeigte, dass Alter, Stadium und IRGPI-Score signifikante Prädiktoren für die Prognose waren. Um einen quantitativen Ansatz für die RFS-Vorhersage zu etablieren, führten wir ein Nomogramm basierend auf Prognosefaktoren (IRGPI, Alter und Stadium) in den Meta-Trainings- und Meta-Validierungssätzen durch (Abbildung 7A, 7B). Die Zuverlässigkeit der Nomogramme wurde anhand des Kalibrierungsdiagramms bewertet. Infolgedessen lagen die Liniensegmente in den Kalibrierungsdiagrammen nahe an der 45-Grad-Linie, was auf eine hervorragende Übereinstimmung zwischen der Vorhersage und der Beobachtung in der Meta-Trainingskohorte (ergänzende Abbildung 4A–4D) und der Meta-Validierungskohorte (ergänzende Abbildung 4E) hinweist –4H).


Klicken Sie hier, um zu gelangendie Cistanche-Ergänzungen
Diskussion
In dieser Studie haben wir eine Signatur entwickelt, die auf 25 IRGPs basiert, um gleichzeitig die Prognose von Harnkrebs, einschließlich Blasen-, Prostata- und Nierenkrebs, vorherzusagen. Die Signatur zeigte eine robuste Fähigkeit zur Vorhersage des RFS von Harnkrebs in Trainingskohorten und Kohorten mit mehreren Validierungen. Unsere Signatur konnte in stratifizierten Analysen auch verschiedene RFS in definierten Patientengruppen (z. B. im Frühstadium) unterscheiden. Das auf dem IRGPI-Score und klinischen Prognosefaktoren erstellte Nomogramm war in der Lage, die RFS-Raten von Blasen-, Prostata- und Nierenkrebspatienten quantitativ vorherzusagen.
Patienten mit Blasen- [36], Prostata- [37] und Nierenkrebs [38] haben ein erhebliches Rückfallrisiko, auch nach chirurgischer Resektion. Der Einsatz verschiedener adjuvanter Therapien, insbesondere bei Patienten im Frühstadium, bleibt umstritten [39]. Zuverlässige prognostische Biomarker werden dringend benötigt, um Patienten mit einem höheren Rückfallrisiko zu identifizieren und Patienten auszuwählen, die auf Therapien ansprechen. Viele auf der Genexpression basierende Signaturen wurden entwickelt, um die Prognose von Blasen- [40–42], Prostata- [43–45] und Nierenkrebs [46–48] vorherzusagen. Der gemeinsame Nachteil dieser Studien waren jedoch technische Verzerrungen, die durch die Normalisierung von Expressionsprofilen verursacht wurden, die von verschiedenen Plattformen mithilfe von RNA-Seq oder Microarrays abgeleitet wurden. Basierend auf der relativen Rangfolge der Genexpression konzentrierte sich die IRGP-Signatur in der vorliegenden Studie auf paarweise Vergleiche innerhalb des Genexpressionsprofils von Proben. Die Notwendigkeit einer Datennormalisierung wurde weitestgehend eliminiert und technische Verzerrungen zwischen verschiedenen Plattformen bei der Kombination mehrerer Genexpressionsprofile wurden vermieden. Einige Forscher haben IRGP-Signaturen identifiziert, die mit der Prognose von Harnkrebspatienten zusammenhängen. zum Beispiel Fu et al. fanden eine neuartige IRGP-Signatur, die einen signifikanten prognostischen Wert für die Vorhersage des Gesamtüberlebens bei Blasenkrebs hatte [49]. Forscher in Südchina haben auch IRGPs entwickelt, um die Prognose von Patienten mit papillärem Nierenzellkarzinom vorherzusagen [50]. Aufgrund der relativ geringen Stichprobengröße mangelte es diesen Studien jedoch an ausreichender Validierung und sie konnten nur die Prognose eines einzelnen Tumors vorhersagen. In dieser Studie haben wir umfangreiche Datensätze von mehreren Plattformen integriert, um die Signatur des IRGP zu identifizieren. Die Signatur konnte gleichzeitig das RFS von drei urologischen Haupttumoren vorhersagen und war nach der Überprüfung robust. Daher kann unsere Signatur sinnvoll in die klinische Anwendung gebracht werden.

Standardisierte Cistanche
Die Tumorimmun-Mikroumgebung korreliert mit der Prognose von Blasen- [22, 51], Prostata- [23, 52] und Nierenkrebs [24, 53]. Im Zeitalter der Immuntherapie könnten prognostische Biomarker, die für die Immunmikroumgebung des Tumors relevant sind, einen neuen Weg zur Identifizierung neuer prognostischer Biomarker eröffnen. In dieser Studie waren die meisten IRGs, die an unserer Immunsignatur beteiligt sind, Zytokine, antimikrobielle Mittel und Zytokinrezeptoren, die eng mit der Immunantwort und Entzündungsprozessen zusammenhängen. Die Anreicherungsanalyse zeigte auch, dass die für die Immunsignatur relevanten IRGs hauptsächlich an der Immun- und Entzündungsreaktion sowie der Zytokinaktivität beteiligt waren. In den Haupttumoren des Harnsystems wurde eine erhöhte entzündliche Mikroumgebung festgestellt. Dieser Befund stimmt mit früheren Studien überein, die zeigten, dass die Bildung und das Fortschreiten von Tumoren mit einer erhöhten entzündlichen Mikroumgebung zusammenhängen [54, 55]. An der Entzündungsreaktion von Tumoren sind verschiedene Immunzellen wie Neutrophile und Makrophagen beteiligt. Makrophagen sind bei vielen Krebsarten mit einer schlechten Prognose verbunden [56, 57]. In der vorliegenden Studie stellten wir fest, dass der Infiltrationsgrad des Makrophagen M1 in der Immun-Hochrisikogruppe signifikant anstieg. Die fehlregulierte Immunkontextstruktur kann zu Überlebensunterschieden führen, die zwischen Risikogruppen gemäß der IRGPI-Definition beobachtet werden. Bemerkenswert ist, dass der Grad der Infiltration von M1-Makrophagen in der Hochrisiko- und der Niedrigrisikogruppe in der Forschung uneinheitlich ist [49, 50, 58–61]. Von diesen Studien stimmen zwei mit unserem Ergebnis überein [50, 58], drei von ihnen berichten, dass es keinen signifikanten Unterschied gibt [59–61] und nur eine Studie steht im Widerspruch zu unserer [49]. Die Inkonsistenzen im Infiltrationsgrad von M1-Makrophagen können mit Unterschieden in der Studienpopulation zusammenhängen, d. h. die Proben, die Risikobewertungen generieren, sind unterschiedlich.
Zu beachten ist, dass es in dieser Studie Einschränkungen gab. Erstens basierte die prognostische Signatur der 25 IRGPs auf einer retrospektiven Studie, obwohl neun Datensätze für eine strenge Validierung verwendet wurden. Unsere Ergebnisse sollten in zukünftigen Kohorten mit unterschiedlichen Probenattributen weiter validiert werden. Zweitens muss unsere prognostische Signatur auch durch quantitative Echtzeit-Polymerase-Kettenreaktion validiert werden, bevor sie klinisch angewendet werden kann. Drittens haben wir IRGPs mit konstanten Werten entfernt, um den Einfluss von Batch-Effekten zwischen verschiedenen Plattformen zu reduzieren, Batch-Effekte können jedoch nicht eliminiert werden.

Cistanche-Pulver
Zusammenfassend lässt sich sagen, dass unsere 25 IRGPs-Signatur ein vielversprechender und robuster prognostischer Biomarker zur Vorhersage des RFS von Blasen-, Prostata- und Nierenkrebs, einschließlich Krebserkrankungen im Frühstadium, ist. Darüber hinaus war diese Signatur mit der Infiltration von Immunzelluntergruppen und der Immunantwort verbunden, was auf Zusammenhänge zwischen der Immunmikroumgebung und diesen Krebsarten hinweist, und könnte daher bei der Formulierung einer personalisierten Immuntherapiestrategie helfen. Obwohl der klinische Nutzen unserer Signatur in prospektiven Studien validiert werden muss, hat unsere Studie durch die Integration umfangreicher Datensätze dennoch eine Reihe vielversprechender prognostischer Marker bereitgestellt.
Die Wirkung von Cistanche-Extrakt auf die Verbesserung des Harnsystems
Cistanche-Extrakt wird aus der Pflanze Cistanche Deserticola gewonnen, die traditionell in der chinesischen Medizin wegen ihrer gesundheitsfördernden Wirkung eingesetzt wird. Seine Wirksamkeit bei der Verbesserung des Harnsystems ist eine seiner bekannten Eigenschaften.
Studien haben gezeigt, dass Cistanche-Extrakt eine Reihe bioaktiver Verbindungen enthält, die antioxidative und entzündungshemmende Wirkungen haben. Diese Verbindungen können zum Schutz vor oxidativem Stress, Entzündungen und Zellschäden im Harnsystem beitragen. Dies führt zu einer verbesserten Funktion und einem geringeren Risiko urologischer Erkrankungen.
Ein Bereich, in dem Cistanche-Extrakt vielversprechende Ergebnisse gezeigt hat, ist die Verbesserung der Symptome im Zusammenhang mit der benignen Prostatahyperplasie (BPH). Bei BPH handelt es sich um eine Erkrankung, bei der sich die Prostata vergrößert und die Harnröhre zusammendrückt, was zu Harndrang, häufigerem Harndrang, schwachem Harnfluss und unvollständiger Blasenentleerung führt.
Untersuchungen legen nahe, dass Cistanche-Extrakt diese Symptome lindern kann, indem er die Größe der Prostatadrüse verringert. Dies geschieht durch Hemmung der Aktivität eines Enzyms namens 5-Alpha-Reduktase, das Testosteron in Dihydrotestosteron (DHT) umwandelt, ein Hormon, das das Prostatawachstum stimuliert. Durch die Reduzierung des DHT-Spiegels verhindert Cistanche-Extrakt eine weitere Prostatavergrößerung und verbessert die Harnbeschwerden.
Cistanche-Extrakt hat auch entzündungshemmende Wirkungen, die anderen Harnwegserkrankungen wie Harnwegsinfektionen (HWI) und interstitieller Zystitis (IC) zugute kommen können. Beide Erkrankungen verursachen eine Entzündung der Blasenwand, die zu häufigem Wasserlassen, Harndrang, Schmerzen und Unwohlsein führt. Durch die Reduzierung von Entzündungen kann Cistanche-Extrakt diese Symptome lindern.
Zusammenfassend lässt sich sagen, dass die Fähigkeit des Cistanche-Extrakts, das Harnsystem zu verbessern, auf seinen entzündungshemmenden und antioxidativen Eigenschaften beruht. Obwohl sich die Forschung noch in einem frühen Stadium befindet, deuten die bisherigen Erkenntnisse darauf hin, dass Cistanche-Extrakt eine wirksame Behandlungsoption für die Behandlung von Harnwegserkrankungen wie BPH, Harnwegsinfektionen und IC sein könnte. Dennoch ist es wichtig zu beachten, dass Einzelpersonen potenzielle Nahrungsergänzungsmittel immer mit einem qualifizierten Gesundheitsdienstleister besprechen sollten, um sicherzustellen, dass diese sicher und für ihre individuellen Bedürfnisse geeignet sind.

Vorteile von Cistanche
Verweise
36. Wang X, Ding Y, Wang J, Wu Y. Identifizierung der Schlüsselfaktoren im Zusammenhang mit Blasenkrebs durch ein lncRNA-miRNAmRNA-Dreischichtnetzwerk. Vordere Ginsterkatze. 2020; 10:1398.
37. Heidenreich A, Bastian PJ, Bellmunt J, Bolla M, Joniau S, van der Kwast T, Mason M, Matveev V, Wiegel T, Zattoni F, Mottet N und European Association of Urology. EAU-Leitlinien zu Prostatakrebs. Teil II: Behandlung von fortgeschrittenem, rezidivierendem und kastrationsresistentem Prostatakrebs. Eur Urol. 2014; 65:467–79.
38. Kelsey R. Nierenkrebs: ccrcc1-4-Klassifizierung zur Vorhersage eines Rückfalls. Nat Rev Urol. 2018; 15:205.
39. Roberts ME, Aynardi JT, Chu CS. Uterus-Leiomyosarkom: Ein Überblick über die Literatur und ein Update zu Behandlungsoptionen. Gynäkologische Onkol. 2018; 151:562–72.
40. Shariat SF, Karakiewicz PI, Godoy G, Karam JA, Ashfaq R, Fradet Y, Isbarn H, Montorsi F, Jeldres C, Bastian PJ, Nielsen ME, Müller SC, Sagalowsky AI, Lotan Y. Survivin als prognostischer Marker für Urothelkarzinom der Blase: eine multizentrische externe Validierungsstudie. Clin Cancer Res. 2009; 15:7012–9.
41. Mo Q, Nikolos F, Chen F, Tramel Z, Lee YC, Hayashi K, Xiao J, Shen J, Chan KS. Prognosekraft einer Tumordifferenzierungs-Gensignatur für Blasen-Urothelkarzinome. J Natl Cancer Inst. 2018; 110:448–59.
42. Sikic D, Eckstein M, Wirtz RM, Jarczyk J, Worst TS, Porubsky S, Keck B, Kunath F, Weyerer V, Breyer J, Otto W, Rinaldetti S, Bolenz C, et al. FOXA1-Genexpression zur Definition molekularer Subtypen von muskelinvasivem Blasenkrebs nach radikaler Zystektomie. J Clin Med. 2020; 9:994.
43. Gerke JS, Orth MF, Tolkach Y, Romero-Pérez L, Wehweck FS, Stein S, Musa J, Knott MM, Hölting TL, Li J, Sannino G, Marchetto A, Ohmura S, et al. Die integrative klinische Transkriptomanalyse zeigt die TMPRSS2-ERG-Abhängigkeit prognostischer Biomarker beim Prostata-Adenokarzinom. Int J Krebs. 2020; 146:2036–46.
44. Wu CL, Schroeder BE, Ma XJ, Cutie CJ, Wu S, Salunga R, Zhang Y, Kattan MW, Schnabel CA, Erlander MG, McDougal WS. Entwicklung und Validierung eines 32-Gen-Prognoseindex für das Fortschreiten von Prostatakrebs. Proc Natl Acad Sci USA. 2013; 110:6121–6.
45. Zhao SG, Evans JR, Kothari V, Sun G, Larm A, Mondine V, Schaeffer EM, Ross AE, Klein EA, Den RB, Dicker AP, Karnes RJ, Erho N, et al. Die Landschaft prognostischer Ausreißergene bei Hochrisiko-Prostatakrebs. Clin Cancer Res. 2016; 22:1777–86.
46. Liang T, Sang S, Shao Q, Chen C, Deng Z, Wang T, Kang Q. Abnormale Expression und prognostische Bedeutung von EPB41L1 beim klarzelligen Nierenkarzinom basierend auf Data Mining. Krebszelle Int. 2020; 20:356.
47. Yang CA, Huang HY, Yen JC, Chang JG. Prognostischer Wert von RNASEH2A-, CDK1-- und CD151--bezogenen Pathway-Genprofilen für Nierenkrebs. Int J Mol Sci. 2018; 19:1586.
48. Kim KM, Hussein UK, Bae JS, Park SH, Kwon KS, Ha SH, Park HS, Lee H, Chung MJ, Moon WS, Kang MJ, Jang KY. Die Expressionsmuster von FAM83H und PANX2 sind mit einem kürzeren Überleben von Patienten mit klarzelligem Nierenzellkarzinom verbunden. Front Oncol. 2019; 9:14.
49. Fu Y, Sun S, Bi J, Kong C, Yin L. Eine neuartige immunbezogene Genpaar-Prognosesignatur zur Vorhersage des Gesamtüberlebens bei Blasenkrebs. BMC-Krebs. 2021; 21:810.
50. Zhou X, Qiu S, Jin D, Jin K, Zheng Vordere Ginsterkatze. 2020; 11:569884.
51. Wong YN, Joshi K, Khetrapal P, Ismail M, Reading JL, Sunderland MW, Georgiou A, Furness AJ, Ben Aissa A, Ghorani E, Oakes T, Uddin I, Tan WS, et al. Aus dem Urin stammende Lymphozyten als nicht-invasives Maß für die Immunmikroumgebung des Blasentumors. J Exp Med. 2018; 215:2748–59.
52. Luo C, Chen J, Chen L. Untersuchung von Genexpressionsprofilen und der Immunmikroumgebung zwischen Gruppen mit hoher und niedriger Tumormutationslast bei Prostatakrebs. Int Immunopharmacol. 2020; 86:106709.
53. Şenbabaoğlu Y, Gejman RS, Winer AG, Liu M, Van Allen EM, de Velasco G, Miao D, Ostrovnaya I, Drill E, Luna A, Weinhold N, Lee W, Manley BJ, et al. Erratum zu: Die Charakterisierung der Tumorimmun-Mikroumgebung bei klarzelligem Nierenzellkarzinom identifiziert prognostische und immuntherapeutisch relevante Messenger-RNA-Signaturen. Genombiol. 2017; 18:46.
54. Greten FR, Grivennikov SI. Entzündung und Krebs: Auslöser, Mechanismen und Folgen. Immunität. 2019; 51:27–41.
55. Crusz SM, Balkwill FR. Entzündung und Krebs: Fortschritte und neue Wirkstoffe. Nat Rev Clin Oncol. 2015; 12:584–96.
56. Cassetta L, Pollard JW. Targeting von Makrophagen: Therapieansätze bei Krebs. Nat Rev Drug Discov. 2018; 17:887–904.
57. Ngambenjawong C, Gustafson HH, Pun SH. Fortschritte bei gegen Tumor-assoziierte Makrophagen (TAM) gerichteten Therapeutika. Adv Drug Deliv Rev. 2017; 114:206–21.
58. Shi YR, Xiong K, Ye X, Yang P, Wu Z, Zu XB. Entwicklung einer prognostischen Signatur für Blasenkrebs basierend auf immunbezogenen Genen. Ann Transl Med. 2020; 8:1380.
59. Zheng X, Zhou X, . Vordere Ginsterkatze. 2021; 12:764184.
60. Zhang LH, Li LQ, Zhan YH, Zhu ZW, Zhang XP. Identifizierung einer IRGP-Signatur zur Vorhersage der Prognose und der immuntherapeutischen Wirksamkeit bei Blasenkrebs. Front Mol Biosci. 2021; 8:607090.
61. Tao Z, Zhang E, Li L, Zheng J, Zhao Y, Chen Biotechnologisch. 2021; 12:4259–77.
Biao Xie 1, Kangjie Li 1, Hong Zhang 1, Guichuan Lai 1, Dapeng Li 2, Xiaoni Zhong1.
1. Abteilung für Biostatistik, School of Public Health and Management, Chongqing Medical University, Chongqing, China
2. Institut für Hepatologie, Nationales klinisches Forschungszentrum für Infektionskrankheiten, Shenzhen Third People's Hospital, Shenzhen, China
