Bildgebung der renalen Mikrozirkulation in der Zelltherapie
Mar 17, 2022
Kontakt:ali.ma@wecistanche.com
Katerina Apelt u

Cistanche-Stamm für Nierenerkrankungen, klicken Sie hier, um die Probe zu erhalten
Abstrakt:
NierenDie mikrovaskuläre Verdünnung spielt eine zentrale Rolle bei der ProgressionNiereErkrankung. Daher werden Modalitäten zur Visualisierung der Mikrozirkulation der Niere unser Verständnis von Krankheitsmechanismen verbessern und folglich neue Ansätze für die Bewertung zellbasierter Therapien liefern. Derzeit mangelt es der klinischen Praxis jedoch an nicht-invasiven, sicheren und effizienten Bildgebungsverfahren zur Überwachung der mikrovaskulären Veränderungen der Nieren im Laufe der Zeit bei Patienten mit Nierenerkrankungen. Um die Bedeutung zu betonen, fassen wir das aktuelle Wissen über die renale Mikrozirkulation zusammen und diskutieren die Beteiligung an fortschreitender Nierenerkrankung. Darüber hinaus wird ein Überblick über verfügbare bildgebende Verfahren zur Aufdeckung der mikrovaskulären Morphologie, Funktion und des Verhaltens der Nieren mit den damit verbundenen Vorteilen und Einschränkungen gegeben. Letztendlich kann die Notwendigkeit, Nierenerkrankungen auf der Grundlage von In-vivo-Messwerten mit einer Auflösung bis zur Kapillarebene zu beurteilen und zu untersuchen, einen Paradigmenwechsel für die Diagnose und Therapie auf dem Gebiet der Nierenerkrankungen bewirkenNephrologie.
Schlüsselwörter: Niere; Mikrozirkulation; mikrovaskulärVerdünnung; Zelltherapie; Bildgebung
1. Einleitung
Das Nierengefäßsystem hat eine anatomisch komplexe Architektur, die seine einzigartige physiologische Funktion widerspiegelt [1]. Trotz der hochdynamischen Anpassung des mikrovaskulären Netzwerks an hämodynamische Veränderungen können vaskuläre Dysfunktionen die Folge oder sogar die Ursache seinNiereKrankheitsentwicklung und -progression [2,3]. Dementsprechend kann eine mikrovaskuläre Dysfunktion als frühes Kennzeichen einer fibrotischen Nierenschädigung dienen, was impliziert, dass eine nicht-invasive Bewertung und Validierung der mikrovaskulären Architektur und Funktion der Nieren eine große Verbesserung darstellen würde, um die Wirksamkeit von Therapien zur Verringerung der Nierenfibrose zu bewerten.
In der klinischen Praxis ist der Schweregrad chronischNiere(CKD) wird basierend auf der glomerulären Filtrationsrate (GFR) klassifiziert, die leicht (60–89 ml/min/1,73 m2), mäßig (30–59 ml/min/1,73 m2) oder schwer (15–29 ml/ min/1,73 m2 ) verringertNiereFunktionbasierend auf vordefinierten Kategorien [4]. Die Krankheitsprogression zu fortgeschrittener CKD und terminaler Niereninsuffizienz (ESRD) wird durch das Auftreten von Glomerulosklerose und tubulointerstitieller Fifibrose mit einer GFR von weniger als 15 ml/min/1,73 m2 definiert. Mehrere Studien haben gezeigt, dass das Phänomen des Verlusts von Nierenkapillaren, dh renale mikrovaskuläre Rarefaction, eng mit der Schwere der Nierenerkrankung korreliert und an der Biologie des späteren Fortschreitens zu CKD beteiligt ist [3,5–7]. Als zentrales Merkmal für einen solchen peritubulären Kapillarverlust und den daraus resultierenden Nierenepithelverlust wurde die Bildung einer Nierenfibrose hervorgehoben. Wenn die Mikrovaskulatur der Niere geschützt oder sogar wiederhergestellt werden kann, würde sich die strukturelle Gewebeintegrität der Niere verbessern und das Fortschreiten der Krankheit kann verhindert werden [2,8]. Darüber hinaus kann möglicherweise ein therapeutisches Fenster definiert werden, um die Schwere der Verletzung zu beurteilen, bevor das Ausmaß der Nierenschädigung irreversibel ist. Insbesondere die Nutzung von Zelltherapien wie vielversprechende Anwendungen von mesenchymalen Stromazellen (MSCs) können zur Behandlung von Nierengefäßerkrankungen bewertet und verfeinert werden. Ein detailliertes Verständnis der renalen mikrovaskulären Verdünnung wird jedoch immer noch durch das Fehlen von Bildgebungsmodalitäten behindert, die eine hochauflösende und nicht-invasive Überwachung der Gefäßarchitektur und -funktionalität ermöglichen.

In dieser Übersicht fassen wir das aktuelle Wissen über die Mikrogefäße der Niere und die pathologischen Mechanismen zusammen, die die Mikrozirkulation beeinflussen können. Wir diskutieren die Bedeutung von Perizyten und geben Einblicke in ihre zentrale Rolle bei der Verursachung des Fortschreitens von Nierenerkrankungen durch mikrovaskuläre Dysfunktion und Rarefaction sowie die Entwicklung vonNiereFibrose. Anschließend beschreiben wir neue Entwicklungen in bildgebenden Verfahren, die solche Veränderungen in der renalen Mikrozirkulation überwachen könnten.
2. Das renale Gefäßsystem
2.1. Die renale Durchblutung
Die Mikrovaskulatur des menschlichen Körpers besteht aus Arteriolen, Kapillaren und Venolen und bewirkt den Austausch von Sauerstoff, Nährstoffen und Metaboliten zwischen dem Blut und dem umgebenden Gewebe [8,9]. Offensichtlich wird die lebenswichtige Funktion der Mikrozirkulation basierend auf den Stoffwechselbedürfnissen des Organs streng reguliert. Die Hauptaufgabe der Arteriolen besteht darin, den Blutfluss zu regulieren, indem sie den Widerstand anpassen, um sicherzustellen, dass der lebenswichtige Austausch auf der Ebene der Kapillaren ausgeführt werden kann [10]. Dabei ist die kontinuierliche Anpassung an den homöostatischen Bedarf des darunter liegenden Gewebes hauptsächlich von der dynamischen Plastizität der Endothelzellen abhängig. Gleichzeitig stützt sich die endotheliale Gesundheit der Mikrozirkulation auf die enge interzelluläre Kommunikation mit Perizyten, die die Blutgefäße physikalisch stabilisieren, die Angiogenese regulieren und den Blutfluss kontrollieren [11,12].
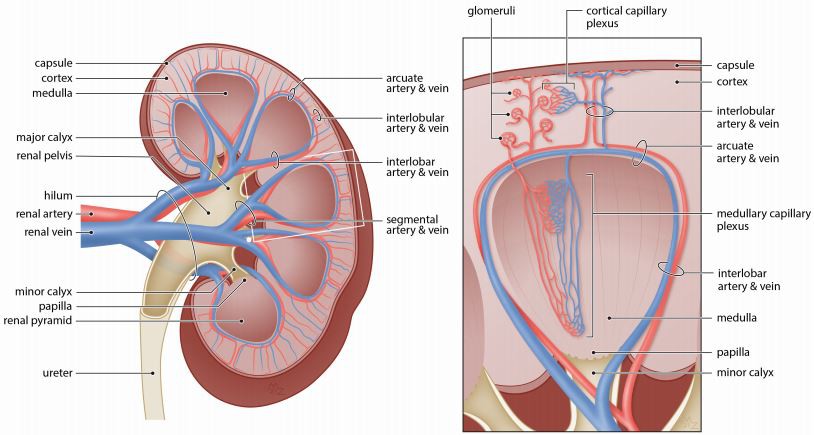
Die Niere ist ein stark vaskularisiertes Organ mit einzigartigen morphologischen und funktionellen Merkmalen, die die bemerkenswerte Heterogenität ihres Gefäßnetzwerks widerspiegeln [1,10]. Blut gelangt über die Nierenarterie durch den Hilus in die Niere (Abbildung 1), der sich im Nierenbecken weiter dichotom in Segmentarterien teilt und sich auf Höhe des kleinen Kelchs progressiv in interlobare Arterien verzweigt, die sich zwischen den Nierenpyramiden ausbreiten [1,13 ]. An der Grenze zwischen Kortex und Medulla münden interlobäre Arterien in die Bogenarterien und bilden eine anatomische Trennung zwischen den beiden Nierenkompartimenten [1]. In der Kortikalis entspringen interlobuläre Arterien, auch bekannt als kortikale Strahlenarterien oder kortikale durchdringende Arteriolen, senkrecht von bogenförmigen Arterien und divergieren in afferente Arteriolen, um die verschiedenen Äste des glomerulären Baums zu versorgen. Je nach Lage der Glomeruli sammelt sich gefiltertes Blut im kortikalen Kapillarplexus, der die proximalen und distalen Tubuli umgibt, oder im medullären Kapillarplexus auf Höhe der Henle-Schleife. Schließlich fließt Blut in das venöse System, das parallel zum arteriellen Netzwerk verläuft und die Niere über die interlobuläre, bogenförmige, interlobäre, segmentale und schließlich die Nierenvene direkt über dem Harnleiter verlässt. Im Allgemeinen bleibt dieses grundlegende Gefäßmuster bei Säugetieren erhalten [14,15].
2.2. Die Kapillarnetzwerke der Niere
Die Komplexität der renalen Mikrogefäßarchitektur spiegelt sich in einer vielfältigen Morphologie der verschiedenen Nierenblutgefäße wider (Abbildung 2). Die strukturelle und funktionelle Heterogenität des Nierenendotheliums und der es umgebenden perivaskulären Zellen gehen eng mit der Art des Kapillarnetzwerks einher [15–17]. Tatsächlich ist das Vorhandensein verschiedener Kapillarbetten ein bemerkenswertes Merkmal, das die Filtration durch das glomeruläre Kapillarnetzwerk sowie die Sekretion und Reabsorption über das peritubulare Kapillarnetzwerk und das medulläre Kapillarnetzwerk gewährleistet [1,13,14]. Die kortikale Mikrozirkulation sorgt hauptsächlich für die Rückresorption des glomerulären Filtrats, während die Salz- und Wasserausscheidung überwiegend durch das medulläre mikrovaskuläre Kompartiment reguliert wird [14]. Obwohl das Medulla ungefähr 30 Prozent der gesamten Nierengewebemasse ausmacht, macht interessanterweise nur 10 Prozent des gesamten renalen Blutflusses (RBF) diesen Teil aus [10]. Basierend auf der anatomischen Position kann die renale Mikrozirkulation unterteilt werden in (i) kortikale Mikrozirkulation; und (ii) medulläre Mikrozirkulation [13,14].
Die kortikale Mikrozirkulation wird physisch durch die bogenförmigen Arterien getrennt, die zu interlobulären Arterien führen, die sich von beiden Seiten weiter in mehrere afferente Arteriolen verzweigen, um das glomeruläre Kapillarnetz zu versorgen [14]. Die Verzweigung erfolgt in einem anderen Winkel, abhängig von der Lage der Glomeruli innerhalb des Cortex. Über die zuführende Arteriole wird das aus 6–8 Kapillarschleifen bestehende glomeruläre Kapillarnetz mit Blut versorgt, das filtriert über die abführende Arteriole austritt [10]. Glomeruläre Kapillaren (Abbildung 2a) bestehen aus einem dünnen, durchgehenden und meist flachen gefensterten Endothel, das von Podozyten bedeckt ist. Die gefensterten Bereiche können bis zu 20–50 Prozent ihrer gesamten Zelloberfläche einnehmen [16]. Die kortikalen Glomeruli machen 90 Prozent aller in der Niere vorhandenen Glomeruli aus, und daher ist es nicht verwunderlich, dass der größte Teil des RBF überwiegend durch sie fließt [13]. Die restlichen 10 Prozent aller Glomeruli liegen an der kortiko-medullären Grenze und sind größer. Neben den Größenunterschieden der Glomeruli lassen sich strukturelle Unterschiede der afferenten und efferenten Arteriolen, die die kortikalen und juxtamedullären Glomeruli versorgen, durch die Bedeutung für die Aufrechterhaltung des Kapillardrucks erklären.
Um eine ordnungsgemäße Blutfiltration zu gewährleisten, beträgt der Durchmesserunterschied zwischen kortikalen afferenten (Abbildung 2b) und kortikalen efferenten (Abbildung 2c) Arteriolen 15 µm gegenüber 10 µm [13]. Der Blutdruck wird an der Seite der afferenten Arteriolen durch Widerstandsänderungen reguliert, die das kontinuierliche Endothel erklären, das von glatten Muskelzellen (SMCs) umhüllt ist [18]. Eine nähere Untersuchung der zuführenden Arteriole offenbart das Vorhandensein von zwei Gefäßsegmenten anstelle eines einheitlichen Endothels entlang der gesamten Gefäßlänge, wie es üblicherweise anzutreffen ist. Der proximale Teil der zuführenden Arteriole besteht aus einem nicht durchlässigen Endothel mit dicht angeordneten SMCs, die für die Gefäßkontraktion erforderlich sind. Im Gegensatz zum distalen Teil, der eng am Glomerulus liegt und aufgrund der Fensterung aus einem durchlässigen Endothel besteht. Interessanterweise ist diese Fensterung bei Gefäßen mit hohem intravasalen Druck eher ungewöhnlich. Außerdem umhüllen würfelförmige Renin-produzierende Perizyten den distalen Teil der afferenten Arteriole, um die Regulierung des lokalen Blutdrucks im Glomerulus zu vermitteln [17,19].

Gefiltertes Blut tritt aus jedem der kortikalen Glomeruli über die efferente Arteriole aus, um in dem dichten kortikalen Kapillarplexus zusammenzukommen, der die Nierentubuli umgibt [10]. Neben dem glomerulären Kapillarsystem ist dieses zweite Kapillarkompartiment als peritubuläres Kapillarsystem bekannt [16]. Die peritubulären Kapillaren (Abbildung 2d) sind gefenstert und dünnwandig mit einem durchschnittlichen Durchmesser von etwa 7 µm [13,15]. Diese Kapillaren versorgen die Tubuli in der Nierenrinde mit Sauerstoff und Nährstoffen, aber nicht unbedingt die, aus der sie stammen [10,15]. Peritubuläre Kapillaren weisen ein durchgehenderes Endothel sowie einen kleineren Durchmesser im Vergleich zu den Markkapillaren der Vasa recta auf [13,16]. Bei einer Nierenerkrankung beeinflusst die glomeruläre Schädigung schließlich die stromabwärts sequentiell angeordneten peritubulären Kapillaren und beschleunigt dadurch das Fortschreiten der Nierenerkrankung [10,20].
Die juxtamedulläre afferente Arteriole (Abbildung 2e) hat einen ungefähren Durchmesser von 20 µm, während die juxtamedulläre efferente Arteriole (Abbildung 2f) einen dickeren Innendurchmesser von 20–25 µm hat [13]. Die efferente Arteriole, die aus dem juxtamedullären Glomerulus austritt, ist stark von mehreren SMCs umgeben. Dieser auffällige Unterschied im Gefäßdurchmesser sowie eine verstärkte Muskulatur werfen die Debatte über die Beteiligung dieses Glomerulustyps an der Ischämie auf. Es scheint, dass die Nierengefäßarchitektur auf eine bestimmte Weise organisiert ist, um das Medulla vor ischämischen Schäden zu bewahren. Es gibt die Hypothese, dass afferente und efferente Arteriolen der juxtamedullären Glomeruli möglicherweise nicht für die Regulierung des medullären Blutspenders (MBF) verantwortlich sind, aber dies würde möglicherweise auch im Widerspruch zu ihrer Rolle stehen, die glomeruläre Filtrationsrate zu kontrollieren [21]. Stattdessen scheint die absteigende Vasa recta (DVR) der im inneren Streifen der äußeren Medulla gelegenen Gefäßbündel für die Kontrolle der MBF verantwortlich zu sein, was die hohe Anzahl von Perizyten erklären könnte, die dieses Gefäßkompartiment umhüllen. Der DVR spielt daher eine Schlüsselrolle bei der Langzeitregulation des arteriellen Drucks [13]. Efferente Arteriolen, die mit den juxtamedullären Glomeruli verbunden sind, fließen durch die Gefäßbündel, die sich im inneren Streifen der äußeren Medulla befinden, und münden in den DVR. Aus dem DVR entsteht das medulläre Kapillarnetz, das mit der aufsteigenden Vasa recta (AVR) verbunden ist [1].
Die medulläre Mikrozirkulation beginnt, wenn die efferenten Arteriolen, die von den juxtamedullären Glomeruli stammen, tiefer in das Gewebe eindringen, um die verbleibenden 30 Prozent des als Medulla bekannten Nierengewebes zu versorgen [13,14]. Das Mark einer Nierenpyramide ist anatomisch in zwei Teile geteilt: das äußere Mark, das sich direkt unter der Rinde befindet, gefolgt vom inneren Mark, das sich bis zur Spitze des Parenchyms, der so genannten Papille, ausbreitet. Im Allgemeinen nimmt die Anzahl der Markkapillaren von der Spitze der Nierenpyramide ab zu. Bei näherer Betrachtung lässt sich die äußere Medulla weiter unterteilen in den äußeren Streifen und den stark vaskularisierten inneren Streifen, der den dichten Kapillarplexus und den Interbündelplexus enthält [15]. Die Kapillaren zwischen den Bündeln sind durch ein gefenstertes Endothel gekennzeichnet und mit der Bogenvene verbunden [14,22].
Jede juxtamedulläre efferente Arteriole teilt sich in mehrere Bündel auf, die als Gefäßbündel bekannt sind, um die Äste des DVR (Abbildung 2g) zu bilden, die im Vergleich zu den peritubulären Kapillaren des Kortex einen größeren Durchmesser haben [15,23]. Mehrere Perizyten sind am Endothel des DVR der Gefäßbündel befestigt [17]. Interessanterweise nimmt die Anzahl der Perizyten, die die Gefäße umhüllen, in DVR (Abbildung 2h) der inneren Medulla ab [15,17]. Diese morphologische Anordnung des DVR im äußeren und inneren Medullakompartiment spiegelt seine Doppelfunktion wider [10]. Genauer gesagt, tritt die Vasokonstriktion des DVR hauptsächlich im proximalen Teil auf, der sich in der äußeren Medulla befindet [15]. Im distalen Teil, also dem Innenmark, findet dagegen hauptsächlich Elektrolytaustausch statt. Dieser anatomische Unterschied impliziert direkt eine unterschiedliche Subpopulation von Perizyten in Bezug auf das morphologische Erscheinungsbild und die funktionellen Eigenschaften [15,17].
Tief im inneren Medulla spalten sich verschiedene Äste des DVR in ein komplexes Kapillarnetzwerk auf, bevor sie sich mit dem deutlich kleineren AVR verbinden [10]. Das Endothel des DVR ist durchgehend, im Gegensatz zu den Endothelzellen des AVR (Abbildung 2i), die stark gefenstert sind. Schließlich wird das gesamte Blut aus dem AVR sowie den peritubulären Kapillaren des kortikalen Kapillarplexus in das Venensystem gesammelt. Im Allgemeinen weisen Nierenvenen eine extrem dünne Gefäßwand auf und interlobuläre, bogenförmige und interlobäre Venen sind gefenstert und enthalten Zwerchfelle. Überraschenderweise zeigen interlobuläre Venen aufgrund des dünnen und stark gefensterten Epithels im Allgemeinen größere Ähnlichkeiten mit peritubulären Kapillaren als mit Venen.
Die unterschiedlichen mikrovaskulären Segmente der Niere und ihr elegantes morphologisches Erscheinungsbild auf Zellebene legen den Verdacht nahe, dass die vorhandene Komplexität in einen noch komplizierteren Krankheitsmechanismus übersetzt wird. Daher konzentriert sich der folgende Abschnitt auf die zugrunde liegenden Prozesse, die an mikrovaskulären Fehlfunktionen der Niere beteiligt sind.

3. Nierenmikrovaskuläre Fehlfunktionen
3.1. Endotheliale Dysfunktion
Das Nierenendothel ist unter physiologischen Bedingungen meist ruhig; als Reaktion auf Mikroumgebungsveränderungen, dh Scherstress, Hypoxie, oxidativen Stress oder Entzündung, kommt es jedoch zu einer Endothelzellaktivierung und angiogenen Wachstumsfaktoren werden produziert [24]. Je nach Auslöser kann die Aktivierung von Endothelzellen einen proinflammatorischen und prothrombotischen Phänotyp induzieren, um die Adhäsion und Infiltration von Immunzellen zur Bildung von Mikrothromben zu fördern. Um jedoch die Gefäßbarriere für eine geeignete weitreichende regulatorische Funktion und Durchlässigkeit für den Transport gelöster Stoffe aufrechtzuerhalten, ist es wesentlich, den metabolischen Zustand von ruhenden sowie aktivierten Endothelzellen streng zu regulieren.
Gewebeintegrität und Organfunktion sind hauptsächlich von einer geeigneten Durchblutung des mikrovaskulären Netzwerks abhängig [8]. Daher ist es nicht überraschend, dass Endothelzellen eine hohe Plastizität aufweisen, um eine dynamische Anpassung an Umweltveränderungen durch Anpassung der Kapillarzahl, morphologischen Form und Funktion sicherzustellen [1,2,8]. Ein länger andauernder erhöhter Blutdruck verursacht jedoch irreversible Veränderungen in der Mikrozirkulation, was zu verletzten Endothelzellen führt, die durch beeinträchtigte Anpassungseigenschaften gekennzeichnet sind. Diese gestörte Homöostase spiegelt sich in einer Reduktion von Stickstoffmonoxid (NO), Hypoxie-induzierbarem Faktor -1 (HIF-1 ) und vaskulärem endothelialem Wachstumsfaktor (VEGF) wider, zusammen mit einem Anstieg anderer Faktoren wie z B. Angiostatin, Endostatin und Thrombospondin [1]. Bemerkenswerterweise ist die Anfälligkeit für endotheliale Dysfunktion in der Niere vielfältig und hängt vom Endothelzelltyp ab, der sich in den verschiedenen Kompartimenten der renalen Mikrozirkulation befindet [16,24]. Um die heterogenen Phänotypen renaler Endothelzellen und ihre unterschiedliche Reaktion auf mikrovaskuläre Veränderungen aufzuklären, haben Dumas et al. [25] stellten kürzlich einen hochauflösenden Atlas des Nierenendothels unter Verwendung von Einzelzell-RNA-Sequenzierung zur Verfügung.
Eine endotheliale Dysfunktion tritt häufig zusammen mit einem akuten und fortschreitenden Rückgang der Nierenfunktion auf [24]. Diese Fehlfunktion verursacht einen erhöhten Gefäßwiderstand, der mit einer Verringerung des RBF einhergeht [26]. Eine längere Phase der Vasokonstriktion führt zu einer unzureichenden Gewebedurchblutung und Aktivierung von Stress- und Wachstumsfaktoren, was zu morphologischen Veränderungen führt [1]. Abhängig von der Schwere und insbesondere der Dauer eines bestimmten Insults kann der RBF irreversibel verändert werden, indem strukturelle Veränderungen in der Mikrozirkulation eingeführt werden. Diese morphologischen Veränderungen werden durch einen Prozess verursacht, der als mikrovaskulärer Umbau bekannt ist. Der mikrovaskuläre Umbau ist definiert als die Reaktion auf funktionelle Veränderungen der Mikrovaskulatur, die folglich eine Veränderung der mikrovaskulären Architektur auf struktureller Ebene verursachen kann, um als letzten Versuch, eine hämodynamische Homöostase zu erreichen [1,2,8]. Schließlich kann eine endotheliale Dysfunktion zu einem Phänomen führen, das als „No-Reflow“ bezeichnet wird, wodurch die Perfusion nicht wiederhergestellt werden kann, was schließlich zu einer Schädigung der tubulären Epithelzellen führt, die zu einer akuten Nierenschädigung (AKI) führt [24].
Es ist von großer Bedeutung hervorzuheben, dass eine endotheliale Dysfunktion nicht nur mit einer Nierenerkrankung assoziiert ist, sondern auch das Fortschreiten der Erkrankung aktiv vorantreibt [24]. Eine renale mikrovaskuläre Fehlfunktion spiegelt sich in einer endothelialen Dysfunktion wider, die durch eine Zellverletzung hervorgerufen wird, die die enge Interaktion der Perizyten mit der Endothelschicht stört und die Zellkommunikation behindert.
3.2. Beteiligung von Perizyten an Nierenfunktionsstörungen
Ein zentrales Merkmal der CKD ist der fortschreitende Verlust des peritubulären Kapillarnetzwerks, ein Prozess, der als Rarefaction bezeichnet wird [27]. Tubulointerstitielle Fifibrose sowie geschädigtes tubuläres Epithel gehen dieser kapillären Verdünnung in der Niere voraus [27], während diese mikrovaskuläre Verdünnung direkt mit dem Schweregrad der Fibrose korreliert [28,29]. Darüber hinaus wurde festgestellt, dass das Ausmaß der Verdünnung den Grad der interstitiellen Schädigung sowie Änderungen der glomerulären Filtrationsrate bei CKD-Patienten vorhersagt [28]. Diese Befunde deuten auf eine frühe, ratenbegrenzende Rolle der mikrovaskulären Destabilisierung/des Verlusts bei der Entwicklung von CKD und der Pathogenese der Fibrose hin [30]. Chronische Aktivierung von Endothelzellen durch kardiovaskuläre Risikofaktoren kann zum Verlust von Perizyten führen, die durch Wechselwirkungen mit Endothelzellen eine entscheidende Rolle bei der Stabilisierung und Proliferation von Kapillaren spielen [31]. In der Tat zeigen immer mehr Beweise die Bedeutung von Perizyten und ihre Beteiligung an der mikrovaskulären Gesundheit der Nieren [17].
Perizyten sind perivaskuläre Wandzellen mit länglichen Fortsätzen, die das Endothel bedecken und in die Basalmembran von Kapillaren eingebettet sind [32]. Sie sind Zellen mesenchymalen Ursprungs und entstehen aus der Forkhead-Box D1 (FoxD1) plus Stroma-Vorläuferpopulation, die auch die anderen Wandzellen des Nierengefäßsystems hervorbringen, einschließlich SMCs, residente Fibroblasten, Reninzellen und Mesangialzellen [33], während alle Endothelzellen des Nierengefäßsystems aus Stammzellleukämie (SCL) plus Vorläufern stammen [34]. Perizyten unterscheiden sich von residenten (perivaskulären) Fibroblasten, da sie in die vaskuläre Basalmembran eingebettet sind, aber die meisten Studien in der Niere unterscheiden nicht zwischen Perizyten und perivaskulären Fibroblasten [31,35], wahrscheinlich aufgrund eines Mangels an spezifischen Markern. Marker, die üblicherweise verwendet werden, um Perizyten zu identifizieren, umfassen Thrombozyten-Wachstumsfaktor-Rezeptor (PDGFR), Chondroitinsulfat-Proteoglykan NG2, Aktin der glatten Muskulatur (SMA), Differenzierungscluster 73 (CD73) und PDGFR, aber diese Marker identifizieren unterschiedliche ( überlappende) Teilmengen von Perizyten, die in verschiedenen anatomischen Regionen lokalisiert sind, was die Heterogenität dieser Zellpopulation [17] und höchstwahrscheinlich auch funktionelle Heterogenität widerspiegelt. Perizyten regulieren streng die vaskuläre Entwicklung, Stabilisierung, Reifung und Remodellierung [11] und kontrollieren den Blutfluss durch Vasokonstriktion. Perizyten werden funktionell durch vasokonstriktive Faktoren wie Angiotensin II und Adenosintriphosphat (ATP) sowie durch vasodilatatorische Faktoren wie NO und Prostaglandine reguliert [17]. Die Reifung von Blutgefäßen hängt von der Rekrutierung perivaskulärer Zellen ab, um das Gefäßsystem zu stabilisieren und den Blutdruck zu kontrollieren [12].
In der Niere umhüllen Perizyten die distalen Teile der afferenten Arteriolen der kortikalen Glomeruli und sind hauptsächlich an den peritubulären Kapillaren und an den Vasa recta vorhanden [13,19]. Darüber hinaus sind Mesangialzellen eine (spezialisierte) Untergruppe von Nierenperizyten, die wichtig sind, um die strukturelle Unterstützung für glomeruläre Kapillaren aufrechtzuerhalten und die glomeruläre Hämodynamik zu regulieren. Darüber hinaus vermitteln kontraktile juxtaglomeruläre Perizyten an den Arteriolen den lokalen glomerulären Blutdruck und beeinflussen den systemischen Blutdruck durch Reninsekretion [19]. Interessanterweise sind Renin-Vorläuferzellen, die aus dem Stroma-Kompartiment stammen, raumzeitlich mit der Entwicklung von Blutgefäßen verbunden, während gezeigt wurde, dass der arteriellen Verzweigungsbildung das Auftreten von Renin-exprimierenden Zellen am Verzweigungspunkt vorausgeht [33,36]. Darüber hinaus wurde unter Verwendung von transgenem Renin-Reporter-Zebrafisch gezeigt, dass Renin-exprimierende Zellen angiogenen Sprossen vorausgehen [37]. In der Niere der erwachsenen Maus werden Renin-Ursprungszellen auch an perivaskulären Stellen beobachtet und gemeinsam mit Perizytenmarkern (PDGFR /NG2) [38] angefärbt, was auf eine möglicherweise wichtige Rolle dieser Untergruppe bei der Gefäßerhaltung hindeutet.
3.3. Wechselwirkungen zwischen Endothelzellen und Perizytensignalen
Perizyten interagieren mit den Endothelzellen durch eine Vielzahl wechselseitiger Wechselwirkungen, die die Signalwege regulieren, die für die Stabilisierung und das angiogene Sprossen erforderlich sind. Perizytensignal an das Endothel durch sezernierte Faktoren wie VEGF, PDGF, Transforming Growth Factor- (TGF-) und Angiopoietin-1 (Ang-1) sowie durch direkten Endothel-Perizyten-Crosstalk [39 ]. In ähnlicher Weise sendet das Endothel Signale an umgebende Stromazellen unter Verwendung von Faktoren wie Angiopoietin-2 (Ang-2) und PDGF. Ang-2 interferiert negativ mit der Ang-1--vermittelten Tie-2-Signalgebung, was zu einer Störung der Perizyten-Endothelzellen-Interaktion und anschließender Gefäßdestabilisierung und anormaler mikrovaskulärer Remodellierung führt [40,41]. Die entscheidende Bedeutung der Interaktion zwischen perivaskulären Stromazellen und Endothelzellen bei der Aufrechterhaltung des Kapillarnetzwerks wird auch durch Mausstudien belegt, die zeigen, dass das Kapillarnetzwerk destabilisiert wird und eine Verdünnung auftritt, wenn die Anlage von Perizyten behindert wird [42]. Beispielsweise erhöht eine Hyperglykämie die endotheliale Ang-2-Expression, was dazu führt, dass perivaskuläre Stromazellen von den Kapillaren weg wandern [43]. Neuere Studien aus unserem Labor haben gezeigt, dass sowohl bei Ratten [44] als auch bei menschlichen Spendernieren [45] eine Ischämie-Reperfusionsschädigung zu einer raschen Erhöhung des damit verbundenen Ang-2/Ang{-1-Gleichgewichts führt mit Verlust der mikrovaskulären Integrität. Darüber hinaus wurde bei Patienten mit Diabetes innerhalb von 12 Monaten nach gleichzeitiger Nieren-Pankreas-Transplantation eine Umkehrung der Kapillargesundheit und eine Abnahme des Ang-2/Ang-1-Verhältnisses und des löslichen Thrombomodulins (Endothelzellschädigungsmarker) beobachtet [46 ]. Neben den Angiopoietin/Tie2-Signalwegen [47] wird das Endothel-Perizyten-Crosstalk durch die Signalwege der TGF-Superfamilie [48], VEGF [49] und Sphingosin-1-phosphat (S1P) [50] reguliert.
3.4. Perizyten als Vorläufer von Myofifibroblasten
Mausmodelle zur genetischen Abstammungsverfolgung haben gezeigt, dass Perizyten (und andere perivaskuläre Zellen) die Hauptquelle von -SMA-positiven Myofifibroblasten in Mausmodellen für Nierenfibrose sind [51,52]. Tatsächlich hat eine kürzlich durchgeführte elegante Studie mit Einzelzell-RNA-Sequenzierung drei Hauptquellen von Myofibroblasten in menschlichen Nieren aufgezeigt: (i) NOTCH3 plus RGS5 plus PDGFR – Perizyten; (ii) MEG3 plus PDGFR plus Fibroblasten; und (iii) COLEC11 plus CXCL12 plus Fibroblasten [53]. Während der Perizyten-zu-Myofibroblasten-Differenzierung wurden Zellzyklusveränderungen beobachtet, die mit Differenzierung und Expansion übereinstimmen, und angereicherte Signalwege umfassten kanonische WNT- und Aktivatorprotein-1 (AP-1)-Signale sowie aktivierende Transkription Faktor 2 (ATF2), PDGFR , Integrin, Rezeptorinteraktion der extrazellulären Matrix (ECM) und TGF-Signalwege [53]. Es wurde zuvor gezeigt, dass ein kleiner Teil der PDGFR-Plus-Zellpopulation aus perivaskulären Gli1-Plus-Vorläufern besteht, die eine perivaskuläre MSC-ähnliche Zellpopulation markieren, von der gezeigt wurde, dass sie durch die Erzeugung von Myofifibroblasten auch entscheidend zur verletzungsinduzierten Organfibrose beiträgt [54]. . Darüber hinaus wurde gezeigt, dass das Gliom-assoziierte Onkogen-Homolog 1 (Gli1) plus Perizytenverlust eine Kapillarrarifikation und proximale tubuläre Verletzung induziert [55]. Da Perizyten zuvor mit MSCs verknüpft wurden und eng verwandt sind [56], wirft dies die Frage auf, ob eine Untergruppe von Perizyten MSCs sein und als solche zur Nierenregeneration beitragen könnte. Tatsächlich haben viele Studien eine multipotente Vorläufer-ähnliche Rolle für Perizyten in verschiedenen Geweben gefunden [35,57,58].
Zusammengenommen trägt die mikrovaskuläre Verdünnung direkt zum Pool von Myofibroblasten bei, die für die übermäßige Bildung von ECM-Proteinen verantwortlich sind, die der Hauptbestandteil von Narbengewebe bei Fibrose sind. Darüber hinaus verursacht der Übergang von Perizyten zu Myofibroblasten eine Ablösung der Perizyten von der Gefäßwand, was zu instabilen Kapillaren führt, die an sich eine Verdünnung verursachen würden [52]. Dennoch wird der Haupteinfluss der Verdünnung auf die Pathogenese des chronischen Nierenversagens durch einen Verlust der Nierendurchblutung verursacht, der die medulläre Ischämie weiter verschlimmert und die Entwicklung einer interstitiellen Fibrose vorantreibt, die durch die erhöhte Expression von TGF- und Bindegewebewachstumsfaktor vermittelt wird (CTGF) [59]. Somit kann die mikrovaskuläre Rarefaction durchaus als geschwindigkeitsbegrenzender pro-fibrotischer Schalter in der Pathogenese des chronischen Nierenversagens fungieren. Tatsächlich könnten Therapien, die auf die Endothelzell-Perizyten-Wechselwirkung abzielen, z. B. die auf die PDGFR- oder VEGF-Rezeptorsignalisierung abzielen, den Myofibroblastenübergang verhindern und die Entwicklung von Fibrose begrenzen [60–62], was die Schlüsselrolle des Kapillarnetzwerks bei Nierenverletzungen und ähnlichem verdeutlicht ein potenzielles therapeutisches Ziel.
Auf der Grundlage des oben Gesagten ist klar, dass die komplexe Gefäßarchitektur der Niere mehrere perivaskuläre Kompartimente erzeugt, von denen jedes seine eigenen spezifischen Funktionen und Anforderungen hat. Daher ist zukünftige Forschung erforderlich, die sich auf eine eingehende Klassifizierung von Nierenperizyten konzentriert, indem Subpopulationen anhand ihrer Lage, Zellmorphologie und Funktion charakterisiert werden. Daher könnten neuartige Bildgebungsverfahren, die darauf abzielen, nicht-invasiv Zugang zu kleinen Blutgefäßen zu erhalten, diese wesentlichen Informationen liefern. Wie auf dem Gebiet der Neurobiologie veranschaulicht [12], könnte die wohldefinierte Kategorisierung verschiedener Subtypen von Perizyten neue Wege für die Entwicklung einer zielgerichteten Therapie für vaskuläre Fehlfunktionen eröffnen.
4. Vaskuläre Bildgebungsmodalitäten
Verschiedene Nierenerkrankungen spiegeln ein charakteristisches Muster ultrastruktureller Veränderungen wider. Als Ergebnis technologischer Fortschritte auf dem Gebiet der biomedizinischen Bildgebung wurden in den letzten Jahrzehnten nierenphysiologische und pathophysiologische Mechanismen enträtselt [63]. Durch die Konzentration auf anatomische und morphologische Veränderungen der Gewebearchitektur erweiterte sich unser Wissen über Nierenerkrankungen zunehmend, was die Diagnostik verbesserte und innovative Behandlungsmöglichkeiten bot. Die dynamische Veränderung von Blutgefäßen wurde jedoch hauptsächlich ignoriert, da es schwierig war, das Gefäßverhalten in Zeitreihenexperimenten zu untersuchen. Infolgedessen besteht ein ungedeckter medizinischer Bedarf an der Entwicklung nicht-invasiver Bildgebungsverfahren zur Überwachung der Hämodynamik der renalen Mikrozirkulation [16].
Es wäre auch interessant, bildgebende Ergebnisse mit (neuen) Biomarkern im Bereich der vaskulären Nephrologie zu verknüpfen. Zum Beispiel haben wir gezeigt, dass nichtkodierende RNAs eng mit Gefäßverletzungen verbunden sind [64,65]. Die Kombination dieser Messungen kann zu neuen (kausalen) Zusammenhängen und neuen Diagnosemöglichkeiten führen. Wenn darüber hinaus neuartige Bildgebungsmodalitäten mit der jüngsten Entwicklung von Einzelzell-basierten Techniken wie Einzelzell-RNA-Sequenzierung und räumlicher Transkriptomik gekoppelt werden [53,66,67], könnte dies eine beispiellose eingehende Analyse der Zusammensetzung und Dynamik ermöglichen des Nierengefäßsystems. Die folgenden Abschnitte fassen bereits verfügbare Ex-vivo- und In-vivo-Bildgebungsmodalitäten zur Untersuchung morphologischer und funktioneller Aspekte der renalen Mikrovaskulatur zusammen.
4.1. Ex-vivo
Ein Großteil unseres Wissens über die Mikrovaskulatur der Niere stammt aus umfassenden Ex-vivo-Analysen von Gewebebiopsien. Dementsprechend wird die zellbasierte Therapie oft durch Gewebeschnitte und Färbung bewertet. Obwohl es viele Studien gibt, die die therapeutische Wirkung von MSCs auf das Nierengefäßsystem untersuchen [68], haben sich nur wenige Forschungsgruppen ausgeklügelte Bildgebungsverfahren wie die Mikrocomputertomographie (Mikro-CT) zunutze gemacht, um die MSC-Therapie durch Untersuchung der 3D-Architektur zu bewerten der Nierengefäße [69–74].
4.1.1. Mikro-Computertomographie (Mikro-CT)
Die Einführung der Mikrocomputertomographie (Mikro-CT) durch Flannery et al. [75] im Jahr 1987 hat neue Wege zur Untersuchung des intakten Gefäßsystems von Nagetieren eröffnet, um Erkenntnisse über Krankheitsmechanismen mit hoher räumlicher Auflösung zu gewinnen. Diese Ex-vivo-Modalität ermöglichte die Visualisierung der mikrovaskulären Architektur der Niere und die Quantifizierung der glomerulären Anzahl, räumlichen Verteilung und des Volumens, was als Indikator für den pathophysiologischen Zustand des gesamten Organs verwendet werden kann [76]. Die Auflösung in einem 3D-Sichtfeld mit 10.243 Voxeln ermöglichte die Visualisierung von afferenten und efferenten Arteriolen sowie der glomerulären Kapillaren von Nagetiernieren. Bei Ratten wurde eine rekonstituierte Voxelgröße von 21 µm verwendet [77] und bei Schweinen wurde das renale Gefäßsystem mit einer Voxelgröße von 40 µm und einem Scan-Sichtfeld von 1,2 mm untersucht [78]. Fortschritte auf dem Gebiet der Mikro-CT boten die Möglichkeit, die Nephron-Blutgefäße der Ratte mit einer Voxelauflösung von 1 µm innerhalb eines Scan-Sichtfelds von 2 mm abzubilden [79].
Basierend auf der von Hillman et al. [80] mittels konventioneller CT wurden Gefäßarchitektur und Gefäßvolumen in verschiedenen Nierengewebskompartimenten im Einklang mit ähnlichen Studien bestimmt, die Nierengefäße anhand histologischer Gewebeschnitte bewerteten [77]. Interessanterweise wurde durch die Anwendung von bildgebenden Verfahren wie der Mikro-CT die Bedeutung erhöht, um die peritubulären Kapillaren und ihre Beteiligung an pathologischen Zuständen zusätzlich zu der herkömmlichen Denkweise über die Rolle des glomerulären Kapillarnetzwerks zu untersuchen.
Frühe strukturelle Veränderungen der Mikrovaskulatur können durch Mikro-CT sichtbar gemacht und erkannt werden, und daher ist es nicht verwunderlich, dass mehrere molekulare Mechanismen auf vaskulärer Ebene, die an Nierenerkrankungen beteiligt sind, durch Mikro-CT identifiziert wurden. In verschiedenen Nierenerkrankungsmodellen, wie z. B. bei der polyzystischen Nierenerkrankung (PKD), wurde eine Korrelation zwischen der Pathologie und einer verminderten Mikrovaskulatur beschrieben, die durch Mikro-CT mit einer Auflösung von 17 µm Voxelgröße bestimmt wurde [81]. Darüber hinaus wurde bei Hypercholesterinämie eine erhöhte kortikale mikrovaskuläre Dichte als frühes Zeichen einer fortschreitenden morphologischen Nierenschädigung beobachtet [78]. Bei Ratten mit chronischer Gallengangsligatur wurde im Mikro-CT eine kortikale Minderdurchblutung festgestellt, was die Störung der Salz- und Wasserretention bei weiterem Krankheitsverlauf erklären könnte [82]. Außerdem wurde bei stenotischen Nieren der erhöhte oxidative Stress mit dem mikrovaskulären Umbau der Nieren in Verbindung gebracht, und es wurden Behandlungsmöglichkeiten durch chronische antioxidative Intervention vorgeschlagen [83].
Ein großer Vorteil der Mikro-CT ist, dass sowohl die axiale als auch die radiale Geometrie von Gefäßsystemen definiert werden kann [84]. Neben der Visualisierung der renalen Gefäßarchitektur in 3D kann die räumliche Dichte von Mikrogefäßen geschätzt werden [78,83], Gefäßdichte und -größe mit einem Durchmesser von bis zu 80 µm in verschiedenen anatomischen Nierenkompartimenten bestimmt werden [77,78,83,85]. ], und es kann eine Gewundenheit der Gefäße beobachtet werden [83]. Darüber hinaus konnte das vaskuläre Kapillarvolumen der Glomeruli sowie der peritubulären Kapillaren innerhalb des Kortex unterschieden und quantifiziert werden [82].
Ein standardisiertes Quantifizierungsprotokoll wurde weithin verwendet, um die mikrovaskuläre Veränderung innerhalb der gut definierten kortikalen und medullären Kompartimente auf struktureller Ebene zu untersuchen, um die Gefäßdichte und den Durchmesser zu bestimmen [77,82]. Ngo et al. [84] führten eine Vergleichsstudie zwischen Mikro-CT und Lichtmikroskopie durch und kamen zu dem Schluss, dass die Quantifizierung der durch Mikro-CT erfassten Geometrie der Nierengefäße eine praktikable und genaue Technik ist. Der einzige Mehrwert der lichtmikroskopischen Bildgebung gegenüber der Mikro-CT besteht darin, dass sie durch die Darstellung der Gefäßwand eine Unterscheidung zwischen Arterien und Venen ermöglicht. Durch die Anwendung von Mikro-CT konnten jedoch Arterien von 100 und 60 µm Durchmesser von Ratten bzw. Kaninchen in 3D visualisiert werden. Allerdings können kleine Blutgefäße, die kleiner als 10 µm sind, nicht richtig durch Mikro-CT identifiziert werden, was die Notwendigkeit drängt, auf die Immunhistochemie zurückzugreifen, um selbst die kleinsten Nierenkapillaren zu erfassen [85].
4.1.2. Lichtblatt-Fluoreszenzmikroskopie (LSFM)
Mit der Einführung der Lichtblatt-Fluoreszenzmikroskopie (LSFM) kann heute eine hochauflösende Abbildung großer Volumina in angemessener Zeit erreicht werden [86,87]. Durch die Verfügbarkeit von LSFM verlagerte sich das Interesse von routinemäßig angewendeten herkömmlichen histologischen Techniken, die das Schneiden des Gewebes mit anschließender Färbung der Mikrogefäße umfassen, hin zur Abbildung des Gewebes als Ganzes. Die volumetrische Analyse ist günstig, da nicht nur ein ausgewählter Teil des Gewebes untersucht wird, sondern auch der dynamische Charakter der Gefäßarchitektur und des Verhaltens in der 3D-Ansicht erhalten bleibt.
Um die 3D-Informationen zu erhalten, wird eine biologische Probe über verschiedene OTC-Protokolle (Optical Tissue Clearing) transparent gemacht, um Lichtstreuung und Lichtabsorption für weitere FL-Fluoreszenzfärbungen zu minimieren [87]. In den letzten Jahren haben OTC-Methoden an Popularität gewonnen, da die 3D-Bildgebung die Möglichkeit bietet, intakte Organe zu untersuchen, was aufgrund moderner Fortschritte bei LSFM möglich wurde. Die Konstruktion eines intakten Organs oder sogar eines ganzen Tieres mit einer Auflösung auf zellulärer Ebene in 3D kann innerhalb von Minuten erstellt werden [88]. Mit einer vergleichbaren Auflösung wie die konfokale FL-Fluoreszenzmikroskopie hat LSFM jedoch ein um zwei Größenordnungen besseres Signal-Rausch-Verhältnis, wodurch das Ausbleichen von FL-Fluorophoren und die Phototoxizität drastisch reduziert werden, wodurch eine groß angelegte Bildverarbeitung ermöglicht wird, die für OTC erforderlich ist [89]. Weitere Vorteile sind, dass die Anzahl der aufgezeichneten Bilder und die Aufzeichnungsgeschwindigkeit größer sind, während die gesamte Aufnahmedauer viel kürzer ist.
Seit der Einführung von LSFM wurden mehrere OTC-Protokolle für verschiedene Gewebeproben und Organe verschiedener Arten verbessert und verfeinert. In den letzten Jahren wurde die ungiftige lösungsmittelbasierte Klärung durch Ethylcinnamat (ECi) weit verbreitet bei klaren Mäusenieren angewendet [88,90,91]. Dieses Protokoll ist weniger zeitaufwändig als beispielsweise die bahnbrechenden Protokolle CLARITY (klare lipidgetauschte Acrylamid-hybridisierte starre Bildgebung), CUBIC (klare, ungehinderte Gehirn-/Körper-Bildgebungscocktails und Computeranalyse) und/oder DISCO (dreidimensionale Bildgebung von Lösungsmittel-gereinigte Organe), bietet jedoch eine relativ vernünftige Reinigung der Niere mit einer geringen verbleibenden Menge an Autofluoreszenz. Bemerkenswerte Arbeit wurde von Ertürk und Kollegen geleistet [92], die erfolgreich eine komplette menschliche Niere durch einen neuen Gewebepermeabilisierungsansatz namens SHANEL (Small-Micelle-Mediated Human Organ Efficient Clearing and Labeling) reinigten. Es wurde bestimmt, dass die Kortexzone Abmessungen von etwa 2742 ± 665 mm (Mittelwert ± SD) aufwies, die glomeruläre Kapillaren mit einem Durchmesser von 221 ± 37 mm enthielt, und die afferente Arteriole hatte einen Durchmesser von 71 ± 28 mm. Darüber hinaus wurde im Bereich der Neurowissenschaften ein hochentwickeltes, auf Deep Learning basierendes Framework zur Quantifizierung des neuronalen Gefäßsystems nach OTC namens VesSAP (Vessel Segmentation & Analysis Pipeline) entwickelt [93].
Trotz der Tatsache, dass auf dem Gebiet der OTC in den letzten Jahren viele große Fortschritte erzielt wurden, bleiben einige Nachteile bestehen, da die Expression von endogenen FL-Fluorophoren meist nicht zufriedenstellend erhalten bleibt, was die Verwendung von transgenen Tieren einschränkt. Ein Hauptanliegen ist jedoch, dass die morphologische Größe des Gewebes und folglich des Gefäßsystems durch die für OTC erforderlichen scharfen Lösungsmittel verändert wird. Darüber hinaus bleibt die enorme Datenmenge, die von LSFM produziert wird, eine Herausforderung, nicht nur für die ordnungsgemäße Datenspeicherung und -verarbeitung, sondern auch für die quantitative Analyse [87].
Kurz gesagt besteht ein wichtiger Vorteil der Anwendung von Techniken wie Mikro-CT oder SFM darin, dass die räumliche Gefäßverteilung erfasst und die strukturelle Verdünnung des Gefäßnetzwerks mit einer geeigneten Auflösung identifiziert werden kann, um fast alle Nierenkapillarstrukturen abzubilden. Beide Techniken erfordern jedoch eine Fixierung und können daher nur ex vivo durchgeführt werden. Um morphologische und funktionelle Veränderungen der Nierenmikrovaskulatur zu überwachen, sind In-vivo-Bildgebungsstrategien erwünscht.
4.2. In vivo
Die Anwendung von In-vivo-Bildgebungsmodalitäten würde die Möglichkeit bieten, zellbasierte Therapien in Echtzeit zu evaluieren und mögliche therapeutische Wirkungen auf vaskulärer Ebene zu validieren. Folglich drängen Fortschritte auf dem Gebiet der biomedizinischen In-vivo-Bildgebung auf die Untersuchung von MSC-basierten Wirkungen auf das Nierengefäßsystem. Nur eine Handvoll Studien hat die In-vivo-Bildgebung angewendet, um die MSC-Wirkung zu untersuchen, wobei Multiphotonenmikroskopie (MPM) [94], CT [95,96] und Magnetresonanztomographie (MRT) [95–97] verwendet wurden.
4.2.1. Multiphotonenmikroskopie (MPM)
Die Multiphotonenmikroskopie (MPM) beruht auf der gleichzeitigen Absorption von zwei oder mehr Photonen nur innerhalb der Fokusebene, die 1995 verfügbar wurde [98]. Dynamische Prozesse können in vivo auf zellulärer Ebene visualisiert werden, und neben der Untersuchung des renalen vaskulären Blutflusses [63] bietet MPM die Möglichkeit, verschiedene mikrovaskuläre Segmente der Niere in Echtzeit zu überwachen. Die hohe Auflösung ermöglicht die Visualisierung der zu- und abführenden Arteriolen und der glomerulären Kapillaren. Der Zugang zur medullären Mikrozirkulation ist zwar technisch möglich, bleibt aber aufgrund der Eindringtiefe eine Herausforderung [98]. Es ist jedoch möglich, einen ganzen Glomerulus mit einem ungefähren Durchmesser von 100 µm zu visualisieren und Zugang zu dynamischen Prozessen auf zellulärer Ebene zu erhalten.
Wichtig ist, dass die mikrovaskuläre Leckage in vivo durch Evans-Blau-Extravasation in fibrotischen Nieren durch MPM visualisiert und quantifiziert werden kann [99]. Die Anzahl der perfundierten Kapillaren wurde quantifiziert und der Durchmesser weit unter 10 µm bestimmt. Kürzlich wandte unsere Forschungsgruppe MPM an, um in vivo nachzuweisen, dass aus humanen pluripotenten Stammzellen (hPSC) stammende Nierenorganoide eine funktionelle Verbindung mit dem vorbestehenden Nierengefäßsystem bei Mäusen nach subkapsulärer Nierentransplantation bildeten [100,101].
Die Vorteile von MPM sind das Fehlen einer FL-Fluoreszenz außerhalb des Fokus und eine eingeschränkte Photobleichung innerhalb der Fokusregion [98]. Einer der Nachteile ist jedoch die begrenzte Bildgebungstiefe, die die Anwendung eines abdominalen Bildgebungsfensters für den Zugang zu den Nierengefäßen in vivo erfordert [102,103]. Dieses Abdominalfenster ermöglicht eine In-vivo-Bildgebung für mehrere Wochen bis zu einem Monat; Das Einsetzen eines solchen Abbildungsfensters erfordert jedoch einen invasiven chirurgischen Eingriff und ist mit der Möglichkeit einer Entzündung verbunden. Darüber hinaus gehen manchmal Bildgebungsfenster verloren und es kann zu Gewebenekrose kommen [102]. Offensichtlich ist diese Bildgebungsmodalität nicht auf die klinische Praxis übertragbar.
Seit der Einführung der handgehaltenen Vitalmikroskopie (HVM) in die klinische Praxis ist eine interessante Alternative zur nicht-invasiven Überwachung des kapillaren Blutflusses am Krankenbett realisierbar [104]. Obwohl diese Bildgebungsmodalität auf einer völlig anderen Technologie basiert, dh Seitenstrom- und Einfalls-Dunkelfeld-Videomikroskope, bietet sie eine Echtzeit-Beurteilung oberflächlich lokalisierter Kapillaren. Neuartige klinisch implementierte Algorithmen, die als MicroTools-Softwarepakete bekannt sind, ermöglichen eine automatisierte mikrovaskuläre Bildgebungsanalyse der gesamten und perfundierten Gefäßdichte für den Zugriff auf Angiogenese, Gefäßerweiterung/-verengung und Flüssigkeitshaushalt sowie die Sauerstoffabgabekapazität basierend auf dem kapillaren Hämatokrit und der Erythrozytengeschwindigkeit [105 ]. Zur Untersuchung der renalen Mikrovaskulatur sind diese Modalitäten jedoch aufgrund ihrer begrenzten Eindringtiefe nicht geeignet.
4.2.2. Computertomographie (CT)
Nicht-invasive Bildgebungsverfahren, die in der Lage sind, morphologische und funktionelle Veränderungen der renalen Mikrovaskulatur zu überwachen und zu quantifizieren, sind sehr gefragt, um die Rolle der Mikrovaskulatur beim Fortschreiten der Erkrankung zu CKD zu bestimmen. Obwohl seit vielen Jahren ein kausaler Zusammenhang zwischen der Kapillarrarifikation und dem Fortschreiten der Nierenfibrose bekannt ist, haben Ehling et al. [3] waren die ersten, die nicht-invasive qualitative und quantitative Analysen anatomischer und funktioneller Gefäßveränderungen während des Fortschreitens von CKD durchführten. Eine fortschreitende Abnahme des Nierenblutvolumens wurde durch in vivo kontrastverstärktes Mikro-CT in drei Mausmodellen mit fortschreitender Nierenfibrose, dh Ischämie-Reperfusionsverletzung (IRI), einseitiger Ureterobstruktion und Alport-Mäusen beobachtet. Neben funktionellen Veränderungen der Mikrogefäße korrelierte der peritubuläre Gefäßverlust in allen drei CNE-Mausmodellen mit der Bildung von fibrotischem Gewebe. Um jedoch Informationen über Verzweigungspunkte, Gefäßdurchmesser und Tortuosität zu erhalten, war eine Ex-vivo-Mikro-CT erforderlich, was auf den Bedarf an neuen biomedizinischen Bildgebungstechnologien hinweist, die den Zugang zu Mikrogefäßen in vivo mit einer nahezu zellulären Auflösung ermöglichen.
Ein großer Vorteil der CT besteht darin, dass die Visualisierung der Nierengefäße innerhalb von Minuten mit einer angemessenen Auflösung erfolgt und 3D-Informationen über die Gefäßorganisation liefert. Durch jodhaltige Kontrastmittel wird der Kontrast verstärkt und eine noch detailliertere Darstellung der Mikrogefäße erreicht. Kürzlich wurde die qualitative und quantitative Beurteilung durch Mikro-CT von Mäusenieren unter physiologischen und pathologischen Bedingungen verfeinert, indem sie mit Phosphorwolframsäure (PTA) perfundiert wurde, um den Kontrast innerhalb der Blutgefäße zu verbessern [106]. Auch wenn die Einschränkung, dass Arterien und Venen nicht eindeutig voneinander unterschieden werden konnten, erfasste die Auflösung mit einer Voxelgröße von 40 µm in vivo und einer Voxelgröße von 12,5 µm ex vivo die Organisation bis auf die Ebene bogenförmiger Blutgefäße.
Ein weiterer großer Nachteil der Verwendung von CT zur Überwachung von Nierenerkrankungen ist jedoch die Notwendigkeit, jodhaltige Röntgenkontrastmittel zu verwenden. Es ist bekannt, dass diese Kontrastmittel Nephrotoxizität verursachen, was eine Kontraindikation für die klinische Anwendung bei Patienten mit vorbestehender Nierenfunktionsstörung darstellt [107–109]. Die akute Schädigung der Niere durch das verabreichte Kontrastmittel verändert die renale Hämodynamik und führt zu einer medullären Hypoxie, die insbesondere bei der Untersuchung der renalen mikrovaskulären Rarefaction unerwünscht ist. In ähnlicher Weise werden Gadolinium-basierte Kontrastmittel, die in der MRT weit verbreitet sind, über die Niere ausgeschieden und scheinen eine Nierenfunktionsstörung zu verursachen [110].
4.2.3. Magnetresonanztomographie (MRT)
Die MRT wurde in den 1980er Jahren in die klinische Praxis eingeführt und entwickelte sich sofort zu einem der am häufigsten verwendeten Bildgebungsverfahren [111]. Die MRT ist eine nicht-invasive und nicht-ionisierende Bildgebungsmodalität, die ein starkes Magnetfeld anwendet und durch die Änderung der T1- und T2-Kontrastmittel die Relaxationseigenschaften von Blut nachweisen kann. Darüber hinaus visualisiert die Magnetresonanzangiographie (MRA) die Gefäßarchitektur von Kleintieren durch Verwendung eines Gadolinium-basierten Kontrastmittels. Ein großer Nachteil der MRA ist jedoch die schwierige Anwendung des erforderlichen Kontrastmittels. Glücklicherweise kann die Nierendurchblutung mit und ohne die Notwendigkeit von Kontrastmitteln bestimmt werden, was sowohl Vorteile als auch Einschränkungen bietet [112].
Ohne die Verwendung eines Kontrastmittels nutzt das Spin-Labeling endogenes Wasser als diffusiblen Tracer, der es nur ermöglicht, die Durchblutung innerhalb der Nierenrinde zu quantifizieren, da die medulläre Transitzeit zu lang ist, um erfasst zu werden. Darüber hinaus werden zur Bestimmung des renalen Blutflusses Phasenverschiebungen von Spins entlang einer Richtung gemessen, was die Notwendigkeit einer senkrechten Bildebene zu den interessierenden Arterien impliziert, um eine genaue Messung zu erreichen [112]. Daher ist es nicht verwunderlich, dass diese Technik eine große Herausforderung darstellt, wenn es um die Darstellung der Nierenarterien geht, ganz zu schweigen von den kleinen kortikalen Kapillaren.
Die Gefäßfunktionalität kann durch Quantifizierung des RBF durch MR-Perfusion und Überwachung des Oxygenierungszustands durch blutsauerstoffspiegelabhängige Kontrastmittel (BOLD)-Bildgebung bestimmt werden [112,113]. Die Haupteinschränkung der funktionellen MRT besteht jedoch darin, zuverlässige und reproduzierbare Ergebnisse in Organen zu erzielen, die von Atembewegungen betroffen sind, zu denen die Niere gehört, obwohl sie im Vergleich zu Leber oder Darm weniger anfällig für Bewegungsartefakte ist [112]. Trotz der Tatsache, dass Machbarkeitsstudien mit funktioneller 1,5-Tesla-MRT bei der voxelweisen Quantifizierung vielversprechend waren [114], konnten Perfusionsanomalien nur in pathologischen Bereichen nachgewiesen werden, was die Frage aufwirft, ob geringfügige Gefäßveränderungen ausreichend erkannt werden. Mit der Einführung eines MRT-Scanners mit einer Magnetfeldstärke von 3,0 Tesla wurde das Signal-Rausch-Verhältnis enorm verbessert [115,116], jedoch bleibt die erreichte Auflösung ein Problem.
Die Auflösung der MRT ist hauptsächlich abhängig von der Magnetfeldstärke und kann durch Anpassung der Pulssequenzen für das jeweilige Magnetfeld optimiert werden [111]. Die räumliche Auflösung wird hauptsächlich durch das Signal-Rausch-Verhältnis begrenzt, das eine schnelle Aufnahmezeit erfordert und im Allgemeinen eine Auflösung von 3 × 4 mm Pixelgröße erreicht [117]. Selbst wenn ein hohes Magnetfeld von 7 Tesla angelegt wird, liegt die beste Auflösung, die man mit BOLD erreichen kann, bei etwa 500 µm. Neben der unbefriedigenden Auflösung und der Einschränkung auf die Visualisierung dynamischster Prozesse besteht ein weiterer großer Nachteil darin, dass die MRT mit hohen Kosten verbunden ist und spezielle Einrichtungen und Wartung erfordert.
4.2.4. Ultraschall
Fortschritte in der Ultraschalltechnik leiteten einen Paradigmenwechsel für die nicht-invasive Überwachung struktureller und funktioneller mikrovaskulärer Veränderungen der Nieren ein und eröffneten neue Wege zur Erforschung kleiner Gefäße mit einem tragbaren System zu relativ geringen Kosten. In einem Rattenmodell mit akuter Ischämie, verursacht durch schwere Hypoperfusion für 1 Stunde, wurde der renale Blutfluss in Echtzeit unter Verwendung von Farb- und Pulswellen-(PW)-Doppler-Ultraschall bewertet [118]. Die Farb-Doppler-Bildgebung zeigte auch die Schwierigkeit, bogenförmige Arterien aufgrund ihrer relativ geringen Größe und der senkrechten Sondenpositionierung zu visualisieren, um den Arterienfluss zu erfassen, der für die Berechnung der Blutgeschwindigkeit und die Anwendung der Doppler-Winkelkorrektur erforderlich ist. Die Blutgeschwindigkeit konnte jedoch nur an den intrarenalen Arterien, dh Segmentarterien, interlobären und bogenförmigen Arterien, berechnet werden. Dementsprechend konnten aufgrund der Auflösungsbeschränkung des herkömmlichen Ultraschalls keine Informationen über die Mikrozirkulation gewonnen werden.
Mit der Einführung der ultraschnellen Doppler-Ultraschalltechnologie konnte eine höhere Auflösung durch unfokussierte Wellenübertragung erreicht werden, bei der mehrere synchrone Wellen mit einer hohen Bildrate gleichzeitig in einem gesamten Sichtfeld gesendet werden, anstatt Zeile für Zeile durch die Anwendung von zu scannen fokussierte Strahlübertragung [119]. Diese ebene Wellenübertragung ist das grundlegende Konzept hinter der ultraschnellen Doppler-Ultraschallbildgebung und ermöglicht es, kortikale Gefäße einer transplantierten menschlichen Niere mit einem Durchmesser von weniger als 1 mm zu erkennen [120]. Darüber hinaus bietet ultraschneller Doppler-Ultraschall eine äußerst günstige In-vivo-Technik zur Überwachung der renalen mikrovaskulären Verdünnung in präklinischen Studien (Abbildung 3A). Trotz der Fortschritte des ultraschnellen Doppler-Ultraschalls ist der Zugang zu einer Kapillarebene immer noch auf die Verwendung von kontrastverstärkten Mitteln angewiesen [121]. Dennoch bestehen keine nennenswerten Sicherheitsbedenken beim Einsatz eines kontrastverstärkten Mittels für den Doppler-Ultraschall, insbesondere im Vergleich zu CT- und MRT-Kontrastmitteln, die häufig eine Nephrotoxizität aufweisen [122]. In vivo kann jedoch eine unglaubliche Auflösung des murinen Nierengefäßsystems erreicht werden (Abbildung 3B).
Die Ultraschall-Lokalisationsmikroskopie (ULM) löste den Zielkonflikt zwischen räumlicher Auflösung und Eindringtiefe, indem sie einerseits ultraschnelle Doppler-Ultraschallbildgebung und andererseits Ultraschallkontrastmittel in Form von gasgefüllten Mikrobläschen einsetzte [121,123,124]. Unter anderem haben Errico et al. [123] schlugen ULM vor, kraniale Mikrogefäße mit einem Durchmesser von 10 µm über die gesamte Tiefe des etwa 10 mm dicken Mäusehirns abzubilden. In einer kürzlich veröffentlichten Veröffentlichung beschreiben Demené et al. [125] konnten die Dynamik des zerebrovaskulären Blutflusses auf mikroskopischer Ebene tief im menschlichen Gehirn erfassen, indem sie intravenös injizierte Mikrobläschen einzeln verfolgten, um die hochauflösende Bildgebung zu verbessern und eine Gefäßauflösung von bis zu 25 µm zu ermöglichen. Um diese erstaunliche Leistung zu verstehen, ist es wichtig zu erwähnen, dass keine andere nicht-invasive Bildgebungsmethode die Mikrovaskulatur in vivo unterhalb einer Millimeterskala darstellen konnte. Um diese bemerkenswerte räumliche Auflösung in vivo zu erreichen, mussten zwei große Herausforderungen bewältigt werden: die Schädelaberration und Bewegungsartefakte. Obwohl die Anwendung der ULM für Bauchorgane wie die Niere nicht durch die Aberration von Knochenstrukturen behindert wird, stellen die Bewegungsartefakte eine große Schwierigkeit dar. Neuere In-vivo-Studien lieferten jedoch erfolgreich erste Versuche, das renale Gefäßsystem mittels ULM abzubilden [5,126,127].

Verschiedene Gefäßkompartimente innerhalb der Rattenniere konnten unterschieden werden, und durch das Aufbringen von Mikrobläschen wurde die Auflösung erhöht, um die dünnen Gefäßbündel der Vasa recta zu visualisieren, die einen Abstand von 400 µm voneinander haben [5]. Zusätzlich wurde die axiale Blutgeschwindigkeit, dh unter 2 mm/s, die mit dem Fluss von Nierenmikrogefäßen verbunden ist, abgeschätzt, indem injizierte Mikrobläschen mit einem Durchmesser von 1 &mgr;m verfolgt wurden, die einen Gefäßdurchmesser von weniger als 20 &mgr;m erreichen können. Songet al. [127] bildeten die nierenkortikalen Mikrogefäße von Kaninchen ab und konnten Gefäße mit einem Durchmesser von 76 µm in vivo deutlich trennen. Obwohl die Atembewegung korrigiert werden könnte, bleiben Bewegungsartefakte außerhalb der Ebene eine Herausforderung und unmöglich zu korrigieren, da Bildinformationen nicht vollständig erfasst werden konnten [5].
Kürzlich wurde die Progression von AKI zu CKD durch kontrastverstärkten ultraschnellen Doppler-Ultraschall in einem Mausmodell mit einseitiger IRI untersucht [6]. Mittels Injektion von Mikrobläschen wurden 32 µm kleine Nierenblutgefäße identifiziert und Gefäßveränderungen in der Niere quantifiziert, dh Nierenblutvolumen, Gefäßdichte und Windung. Die durch Ultraschall während der In-vivo-Bildgebung erfasste Gefäßdichte des Kortex und der kortikomedullären Verbindung stimmte mit der Quantifizierung überein, die nach der CD31-Immunfärbung erhalten wurde, die als Goldstandard in der Gefäßbiologie anerkannt ist. Dies steht im Einklang mit einer anderen Studie, die von Cao et al. [128], die verdeutlichten, dass der Schweregrad der AKI mittels kontrastverstärktem Ultraschall mittels Mikroblaseninjektion bestimmt werden kann. Nierenperfusionsmessungen in vivo korrelieren eng mit der auf histologischer Ebene festgestellten Nierenschädigung.
In Übereinstimmung mit diesen Ultraschallstudien haben Hueper et al. [7] schlugen zuvor vor, dass die renale Durchblutung die durch MRT bestimmte Progression von AKI zu CKD vorhersagen kann.
Die mikroblasenverstärkte Ultraschallbildgebung der Nierengefäße wurde bereits erfolgreich beim Menschen zur Bestimmung der renalen mikrovaskulären Perfusion durchgeführt und zeigte große Perspektiven für die Diagnose [129–133]. Interessanterweise wurde diese bildgebende Modalität bei der Nierentransplantation angewendet, um den Perfusionsstatus von Nieren-Allotransplantaten zu bestimmen, was eine geeignete nicht-invasive Anzeige zur Vorhersage einer akuten Abstoßung liefern könnte [134]. Abgesehen von der Bedienerabhängigkeit, die eine Einschränkung bei der Verwendung von Ultraschall darstellen kann, war die Stärke der Übereinstimmung zwischen den Beobachtern zwischen zwei Lesern sehr hoch, was die große Machbarkeit bei der Anwendung im klinischen Umfeld widerspiegelt [132]. Aufgrund der Portabilität und der zeitsparenden und einfachen individuellen Anwendung bietet der Ultraschall mit kontrastverstärkten Mikrobläschen hervorragende Perspektiven für die Beurteilung der renalen Mikrovaskulatur in der klinischen Praxis, insbesondere bei Patienten auf der Intensivstation [135]. Diese Technologie ist daher vielversprechend für die Umsetzung in die klinische Praxis, nachdem die Korrektur von abdominalen Bewegungsartefakten für ein robustes Mikroblasen-Tracking mit hoher Präzision erfolgreich gemeistert wurde.
5. Schlussfolgerungen und Perspektiven
Die auffällige Heterogenität der renalen Gefäßarchitektur spiegelt ihre komplexe funktionelle Diversität und Kompartimentierung wider, mit einer logischen Konsequenz, dass die Untersuchung mikrovaskulärer Veränderungen und Verdünnungen ausgefeilte bildgebende Verfahren erfordert. Die Entwicklung, Anwendung und Verbesserung von In-vivo-Bildgebungsverfahren zur Untersuchung von Nierengefäßerkrankungen wird ein besseres Verständnis der Wirkung von Zelltherapien wie MSC auf vaskulärer Ebene ermöglichen und spezifische Biomarker aufklären, die während des Krankheitsverlaufs überwacht werden können.

Verweise
1. Chade, AR Nierengefäßstruktur und Verdünnung. Kompr. Physiol. 2013, 3, 817–831. [Querverweis] [PubMed]
2. Chade, AR Small Vessels, Big Role: Renale Mikrozirkulation und Fortschreiten der Nierenschädigung. Bluthochdruck 2017, 69, 551–563. [Querverweis] [PubMed]
3. Ehling, J.; Bábícková, J.; Gremse, F.; Klinkhammer, BM; Baetke, S.; Knochel, R.; Kießling, F.; Floege, J.; Lammers, T.; Boor, P. Quantitative Mikro-Computertomographie-Bildgebung der vaskulären Dysfunktion bei fortschreitenden Nierenerkrankungen. Marmelade. Soc. Nephrol. 2016, 27, 520–532. [Querverweis] [PubMed]
4. Chen, TK; Knicely, DH; Grams, ME Diagnose und Behandlung chronischer Nierenerkrankungen: Eine Übersicht. Physiol. Verhalten 2019, 322, 1294–1304. [Querverweis] [PubMed]
5. Foiret, J.; Zhang, H.; Ilovitsh, T.; Mahakian, L.; Tam, S.; Ferrara, KW Ultraschall-Lokalisationsmikroskopie zur Abbildung und Beurteilung der Mikrovaskulatur in einer Rattenniere. Wissenschaft. Rep. 2017, 7, 13662. [Querverweis] [PubMed]
6. Chen, Q.; Yu, J.; Ansturm, BM; Stocker, SD; Hellbraun, RJ; Kim, K. Kidney Int. 2020, 98, 355–365. [Querverweis] [PubMed]
7. Hüper, K.; Gutberlet, M.; Rong, S.; Hartung, D.; Mengel, M.; Lu, X.; Haller, H.; Wacker, F.; Meier, M.; Gueler, F. Acute Kidney Injury: Arterial Spin Labeling to Monitor Renal Perfusion Impairment in Mouses – Comparation with histopathological results and renal function. Radiologie 2014, 270, 117–24. [Querverweis]
8. Abgabe, BI; Schiffrin, EL; Mourad, JJ; Agostini, D.; Vicaut, E.; Safar, ME; Struijker-Boudier, HA Beeinträchtigte Gewebedurchblutung, eine Pathologie, die bei Bluthochdruck, Fettleibigkeit und Diabetes mellitus üblich ist. Auflage 2008, 118, 968–976. [Querverweis]
9. Carmeliet, P.; Jain, RK Molekulare Mechanismen und klinische Anwendungen der Angiogenese. Natur 2011, 473, 298–307. [Querverweis]
10. Molema, G.; Aird, WC Vaskuläre Heterogenität in der Niere. Semin. Nephrol. 2012, 32, 145–155. [Querverweis]
11. Armulik, A.; Abramson, A.; Betsholtz, C. Endothel/Perizyten-Wechselwirkungen. Zirk. Auflösung 2005, 97, 512–523. 03.16652.d7. [Querverweis]
12. Attwell, D.; Mischra, A.; Halle, CN; O'Farrell, FM; Dalkara, T. Was ist ein Perizyt? J. Cereb. Blutfluss-Metab. 2016, 36, 451–5. [Querverweis]
13. Evans, RG; Eppel, GA; Anderson, WP; Denton, KM Mechanismen, die der differentiellen Kontrolle des Blutflusses im Nierenmark und -kortex zugrunde liegen. J. Hypertens. 2004, 22, 1439–1451. [Querverweis]
14. Pallone, TL; Sildorff, EP; Turner, MR Intrarenaler Blutfluss: Mikrovaskuläre Anatomie und die Regulation der medullären Perfusion. Klin. Erw. Pharmakol. Physiol. 1998, 25, 383–392. doi:10.1111/j.1440-1681.1998.tb02220.x. [Querverweis]
15. Pallone, TL; Edwards, A.; Mattson, DL Nierenmarkkreislauf. Kompr. Physiol. 2012, 2, 97–140. [Querverweis] [PubMed]
16. Guerci, P.; Ergin, B.; Ince, C. Die Makro- und Mikrozirkulation der Niere. Beste Praxis. Auflösung Klin. Anästhesiol. 2017, 31, 315–329. [Querverweis]
17. Shaw, I.; Reiter, S.; Mullins, J.; Hughes, J.; Péault, B. Pericytes in the renal vasculature: Roles in health and disease. Nat. Rev. Nephrol. 2018, 14, 521–534. [Querverweis]
18. Rosivall, L.; Peti-Peterdi, JJ Heterogenität der afferenten Arteriole – Korrelationen zwischen Morphologie und Funktion. Nephrol. Wählen. Transplantation. 2006, 21, 2703–2707. [Querverweis]
19. Stefanska, A.; Kenyon, C.; Christian, HC; Buckley, C.; Shaw, I.; Mullins, JJ; Péault, B. Menschliche Nierenperizyten produzieren Renin. Niere Int. 2016, 90, 1251–1261. [Querverweis]
20. Schlondorff, DO Überblick über Faktoren, die zur Pathophysiologie einer fortschreitenden Nierenerkrankung beitragen. Niere Int. 2008, 74, 860–866. [Querverweis]
21. Pallone, TL; Zhang, Z.; Rhinehart, K. Physiologie der Mikrozirkulation des Nierenmarks. Bin. J. Physiol. Ren. Physiol. 2003, 284, F253–66. [Querverweis] [PubMed]
22. Pallone, TL Komplexe Leitbündel, dicke aufsteigende Gliedmaßen und Aquaporine: Auswringen des äußeren Marks. Bin. J. Physiol. Ren. Physiol. 2014, 306, 505–506. [Querverweis] [PubMed]
23. Zimmerhäckl, BL; Robertson, CR; Jamison, RL Die medulläre Mikrozirkulation. Niere Int. 1987, 31, 641–647. [Querverweis] [PubMed]
24. Dumas, SJ; Meta, E.; Borri, M.; Luo, Y.; Li, X.; Rabelink, TJ; Carmeliet, P. Phänotypische Vielfalt und Stoffwechsel. Nat. Rev. Nephrol. 2021, 1–24. [Querverweis]
25. Dumas, SJ; García-Caballero, M.; Carmeliet, P. Metabolische Signaturen unterschiedlicher endothelialer Phänotypen. Trends Endokrinol. Metab. 2020, 31, 580–595. [Querverweis]
26. Jourde-Chiche, N.; Fakhouri, F.; Dou, L.; Bellini, J.; Burley, S.; Format, M.; Jarrot, PA; Kaplanski, G.; Le Quintrec, M.; Pernin, V.; et al. Endothelstruktur und -funktion bei Nierengesundheit und -erkrankung. Nat. Rev. Nephrol. 2019, 15, 87–108. [Querverweis]
27. Lang, DA; Norman, JT; Fine, LG Wiederherstellung der Mikrovaskulatur der Niere zur Behandlung chronischer Nierenerkrankungen. Nat. Rev. Nephrol. 2012, 8, 244–250. [Querverweis]
28. Choi, YJ; Chakraborty, S.; Nguyen, V.; Nguyen, C.; Kim, BK; Shim, SI; Suki, WN; Truong, LD Peritubulärer Kapillarverlust ist mit chronischer tubulointerstitieller Verletzung in der menschlichen Niere verbunden: Veränderte Expression des vaskulären endothelialen Wachstumsfaktors. Summen. Pathol. 2000, 31, 1491–1497. [Querverweis]
29. Ishii, Y.; Sawada, T.; Kubota, K.; Fuchinoue, S.; Teraoka, S.; Shimizu, A. Verletzung und fortschreitender Verlust von peritubulären Kapillaren bei der Entwicklung einer chronischen Allograft-Nephropathie. Niere Int. 2005, 67, 321–332. [Querverweis]
30. Serón, D.; Alexopoulos, E.; Raftery, MJ; Hartley, B.; Cameron, JS Anzahl interstitieller Kapillarquerschnitte, bewertet durch monoklonale Antikörper: Beziehung zu interstitieller Schädigung. Nephrol. Wählen. Transplantation. 1990, 5, 889–893. [Querverweis]
