Teil 1: Schutzwirkung von Flavonoiden gegen Mitochondriopathien und damit verbundene Pathologien: Fokus auf den prädiktiven Ansatz und personalisierte Prävention
Mar 31, 2022
Für mehr Information. Kontakttina.xiang@wecistanche.com
Abstrakt: Multifaktorielle mitochondriale Schädigung weist einen "Teufelskreis" auf, der zu einem Fortschreiten der mitochondrialen Dysfunktion und Nebenwirkungen an mehreren Organen führt. Mitochondriale Beeinträchtigungen (Mitochondriopathien) sind mit schweren Pathologien verbunden, einschließlich, aber nicht beschränkt auf Krebs, Herz-Kreislauf-Erkrankungen und Neurodegeneration. Art und Ausmaß kaskadierender Pathologien sind jedoch höchst individuell. Folglich sind Patientenstratifizierung, Risikobewertung und Minderungsmaßnahmen für einen kosteneffizienten individuellen Schutz von entscheidender Bedeutung. Daher ist der Paradigmenwechsel von der reaktiven zur prädiktiven, präventiven und personalisierten Medizin (15:00 Uhr) in der Advanced Healthcare unumgänglich.Flavonoide deutlich zeigenAntioxidansund die Aufräumaktivität ist von großem therapeutischem Nutzen gegen mitochondriale Schäden und kaskadierende Pathologien. Im Zusammenhang mit 15:00 Uhr konzentriert sich diese Übersicht auf vorklinische und klinische Forschungsdaten, die die Wirksamkeit von Flavonoiden als wirksamen Schutz gegen Mitochondriopathien und damit verbundene Pathologien bewerten.
Schlüsselwörter: Naturstoffe; sekundäre Pflanzenstoffe; Flavonoide; antioxidative Aktivität;Genoprotektion;Stress; mitochondriale Beeinträchtigung; Mitochondriopathie; mitochondriale Funktion; Funktionsstörung; Verletzung; Tumorentstehung; Krebs; Herzkreislauferkrankung; Neurodegeneration; prädiktive präventive personalisierte Medizin (PPPM/3PM); Patientenstratifizierung

1. Einleitung
Die Begriffe mitochondriale Funktion und Dysfunktion sind in der Bioenergetik und Zellbiologie weit verbreitet. Anomalien in mitochondrialen Prozessen, einschließlich Adenosintriphosphat(ATP)-Erzeugung, Apoptose, zytoplasmatischer und mitochondrialer Matrix-Kalziumregulierung, reaktiver Sauerstoffspezies (ROS)-Erzeugung und -Entgiftung, Metabolitensynthese und intrazellulärem Transport, können als mitochondriale Dysfunktion bezeichnet werden [1. Eine mitochondriale Dysfunktion betrifft verschiedene Organe und Gewebe, einschließlich Gehirn, Muskeln, Netzhaut, Cochlea, Leber und Niere, die am anfälligsten für Defekte der oxidativen Phosphorylierung (OXPHOS) sind. Patienten mit mitochondrialen Erkrankungen (Mitochondriopathien) weisen verschiedene Symptome auf, darunter Taubheit, Sehbehinderung, Herz-, Leber- und Nierenprobleme, Schlaganfall, Migräne, Diabetes, Epilepsie, Ataxie, verzögerte motorische und geistige Entwicklung sowie Gedeihstörung häufig bei mehreren nicht-mitochondrialen Erkrankungen beobachtet [2]. Daher ist die effektive Behandlung von Mitochondriopathien eine große Herausforderung in der Medizin.
Derzeit werden mitochondriale Erkrankungen anhand von Funktionsstudien, klinischen, biochemischen und histopathologischen Untersuchungen sowie molekulargenetischen Untersuchungen diagnostiziert [3]. Diagnostische Techniken, die zellfreie Nukleinsäuren oder Bioflüssigkeiten wie Blut, Urin, Speichel, Liquor, Schweiß oder Tränen verwenden, könnten jedoch invasive Gewebebiopsien ersetzen [4-7]. Der Paradigmenwechsel von reaktiver zu prädiktiver, präventiver und personalisierter Medizin (3 PM) basiert auf Gesundheitsansätzen, die gezielte Präventionsmaßnahmen nutzen, die chronische Krankheiten und ethische sowie ökonomische Aspekte medizinischer Leistungen berücksichtigen [8,9].3 PM beinhaltet eine individualisierte Patientenprofilerstellung, die für die Patientenstratifizierung, Charakterisierung der individuellen Prädisposition und personalisierte Behandlungen wichtig ist [10]. Darüber hinaus umfassen mehrstufige diagnostische Ansätze die molekularbiologische Charakterisierung, neuartige eHealth-basierte Diagnosewerkzeuge, Fragebögen und medizinische Bildgebung [9].
In den letzten Jahren haben die gesundheitsfördernden Wirkungen von Flavonoiden, natürlich vorkommenden polyphenolischen Verbindungen, die medizinische Forschung angezogen, einschließlich ihrer Anwendung bei Pathologien im Zusammenhang mit mitochondrialen Beeinträchtigungen [11] wie Krebs, kardiovaskulären und neurodegenerativen Erkrankungen[12]. Die Wirksamkeit von Flavonoiden wird durch umfangreiche präklinische Beweise gestützt, die die Grundlage für weitere Forschungen zur potenziellen zukünftigen Verwendung dieser Verbindungen in der spezifischen gezielten und personalisierten Therapie von Mitochondriopathien gemäß dem 3-Uhr-Ansatz darstellen [13-19].
Diese Übersicht diskutiert die Wirksamkeit von Flavonoiden bei Mitochondriopathien wie zKrebs, Herz-Kreislauf-Erkrankungen(CVDs) und neurodegenerative Erkrankungen, wobei die Notwendigkeit einer fortgeschrittenen Implementierung von 15:00 Uhr hervorgehoben wird.

2. Mitochondriale Schäden und damit verbundene Beeinträchtigungen
In eukaryotischen Organismen spielen Mitochondrien eine wesentliche Rolle bei Zellfunktionen wie Energiestoffwechsel, Biosynthese, Ionenregulierung, Oxidation und/oder Reduktion und Signalwegen im Zusammenhang mit Zellkommunikation, Alterung, Immunantworten, Apoptose, Überleben und Tod [12]. . Die Hauptfunktionen der Mitochondrien sind die ATP-Synthese durch OXPHOS, die Metabolitenoxidation durch den Krebszyklus und die Fettsäureoxidation [20]. Das mitochondriale Genom kodiert Schlüsselproteine der Elektronentransportkette (ETC), die eine wesentliche Rolle bei der Energieerzeugung in aeroben Organismen spielen [21]. Menschliche mitochondriale DNA (mtDNA) ist ein doppelsträngiges kreisförmiges Molekül, das aus 16.569 Basenpaaren besteht [22]. Unter normalen Bedingungen enthalten Mitochondrien mehrere Kopien (100 bis 10 000 pro Zelle) ihrer DNA [23].
Das ETC ist auch eine Quelle von ROS und reaktiven Stickstoffspezies (RNS), Nebenprodukten von OXPHOS, die DNA-, RNA- und Proteinschäden verursachen [24]. Die Unfähigkeit der Basenexzisionsreparatur (BER), die beschädigte mtDNA zu reparieren, führt zu einer ETC-Unterbrechung im Zusammenhang mit der ROS-Produktion (siehe Abbildung 1). Darüber hinaus kann die Aktivität von ETC auch als Prädiktor und Ziel für die Empfindlichkeit gegenüber Arzneimitteln (Venetoclax) bei Patienten mit multiplem Myelom dienen [25]. Darüber hinaus,oxidativen Stressand insufficient DNA damage repair could increase DNA damage resulting in mitochondrial dysfunction in patients with depression. Therefore, a marker 8-oxoguanine of oxidative DNA damage obtained from fluid biopsies (blood, urine) could be beneficial for the prevention and prediction of neurodegenerative disorders such as mito chondriopathies [26]. Subsequently, extensive oxidative mtDNA damage manifests in several mitochondrial dysfunctions and diseases [27]. Mitochondrial dysfunctions can also be caused by mtDNA mutations, deletions, and impaired DNA replication (shown in Figure 1)[28]. For example, the mtDNA m.3243A>Die G-Mutation kann zu klinischen Phänotypen führen, die mit zwei klinischen Syndromen in Zusammenhang stehen: maternal vererbte Diabetes und Taubheit (MDD) und mitochondriale Enzephalomyopathie, Laktatazidose und schlaganfallähnliche Episoden (MELAS)-Syndrom [29]. Darüber hinaus umfassen einige klinische Merkmale von mitochondrialen Syndromen, die mit mtDNA-Mutationen assoziiert sind, eine mütterliche Familiengeschichte aufgrund des mütterlichen Musters der mitochondrialen Vererbung. Die Einfachheit der Analyse der mitochondrialen Genomsequenzierung aufgrund der Verfügbarkeit von Konsensus-Humansequenzen könnte helfen, mtDNA-Störungen im Hinblick auf die Vererbung zu erkennen. Andere mtDNA-Mutationen, die mit einer mitochondrialen Dysfunktion assoziiert sind, werden während des Lebens durch den Alterungsprozess erworben. Diese erworbenen mtDNA-Mutationen stehen oft im Zusammenhang mit altersbedingten Krankheiten wie Diabetes. Daher wird der Fortschritt im Verständnis der grundlegenden mitochondrialen Genetik als ein wichtiges Werkzeug für die Analyse der Beziehung zwischen vererbten mitochondrialen Mutationen und Krankheitsphänotypen durch die Identifizierung erworbener mtDNA-Mutationen angesehen [30,31]. Darüber hinaus kann mitochondriale Dysfunktion durch pathogene Ursachen verursacht werden Varianten in nuklearen Genen, die mit der mtDNA-Erhaltung assoziiert sind, einschließlich solcher, die für mtDNA-Replikationsenzyme kodieren, Proteine, die bei der Aufrechterhaltung des mitochondrialen Nukleotidpools funktionieren, und Proteine, die an der mitochondrialen Fusion beteiligt sind (gezeigt in Abbildung 1)[32]. Außerdem ist der Alterungsprozess mit einer Abnahme der mitochondrialen Biogenese (Fusion und Spaltung) und auch mit einem kritischen Prozess der Eliminierung dysfunktionaler Mitochondrien verbunden, der als Mitophagie bezeichnet wird [20]. Darüber hinaus nehmen die Inzidenz und Häufigkeit von mtDNA-Mutationen mit dem Alter deutlich zu und tragen zur zellulären Seneszenz bei [33].

Wie oben diskutiert, sind mitochondriale Beeinträchtigungen hinsichtlich ihrer unterschiedlichen klinischen Merkmale und genetischen Ätiologie mit verschiedenen sehr heterogenen Erkrankungen assoziiert. Daher kann die Analyse und/oder Aufklärung molekularer Mechanismen im Zusammenhang mit mitochondrialen Beeinträchtigungen die Herausforderungen für die Diagnose und das weitere klinische Management darstellen [34]. Schließlich ist die mitochondriale Dysfunktion ein Kennzeichen vieler Krankheiten, die als Mitochondriopathien bekannt sind, einschließlich bösartiger Erkrankungen, CVDs und Neurodegeneration. Daher ist es unerlässlich, neue Therapien zu finden, die auf mitochondriale Krankheitsmechanismen abzielen.
2.1. Mitochondiopatien sind an der Krebsentstehung beteiligt
Mitochondrien haben wesentliche Funktionen in apoptotischen Signalwegen und den Mechanismen des Warburg-Phänotyps, Prozesse, die eng mit diesen verwandt sindKrebs. Mitochondrien spielen eine wesentliche Rolle im intrinsischen Weg des apoptotischen Zelltods, der mit der Permeabilisierung der äußeren Mitochondrienmembran, der Freisetzung von Cytochrom c, der Apoptosomenbildung, der Caspase-Aktivierung und dem Zelltod verbunden ist [35]. Die Vermeidung von Apoptose ist ein Kennzeichen der menschlichen Krebsentstehung. Krebszellen nutzen mehrere Überlebensstrategien, einschließlich der Aktivierung von anti-apoptotischen und überlebensfördernden Signalen durch die Hemmung der mitochondrialen Apoptose. Daher stellen intrinsische (mitochondriale) Apoptosewege ein vielversprechendes Ziel für Antikrebsstrategien dar [36].
1956 beschrieb Otto Warburg den Prozess, durch den Krebszellen eine schnelle Proliferation aufrechterhalten; Dieser als Warburg-Effekt bekannte Prozess ist durch eine erhöhte Glukoseaufnahme und Laktatsekretion (aerobe Glykolyse) auch unter normoxischen Bedingungen gekennzeichnet, was darauf hindeutet, dass Defekte in der mitochondrialen Atmung die Tumorgenese fördern können [37,38]. Bei Säugetieren verstärkt die Modulation von Proteinkinasen (PK), wie PKL, PKR, PKM1 und PKM2, den Warburg-Effekt in Krebszellen [39]. Darüber hinaus führt die mtDNA-Verarmung zu Veränderungen der mitochondrialen Funktion bei Brust-, Nieren-, Prostata- und anderen Krebsarten sowie altersbedingten Erkrankungen, was die Rolle der Mitochondrien bei der Tumorentstehung unterstreicht [40-43]. Darüber hinaus sind verschiedene Mutationen in Krebszyklusenzymen, einschließlich Succinatdehydrogenase (SDH), Fumarathydratase (FH) und Isocitratdehydrogenase 1 (IDH1) und 2 (IDH2), in Krebszellen beschrieben [44]. SDH-Mutationen sind mit der Aktivierung des Hypoxiewegs verbunden, was die mitochondriale Fusion und Spaltung, Mitophagie und OXPHOS verändern kann. Darüber hinaus führen FH- und IDH-Mutationen durch die Unterdrückung der Zelldifferenzierung zur Tumorinitiierung, und IDH1- und DH2-Mutationen verursachen eine Energieverschiebung in Krebszellen [45,46]. Anomalien in den erwähnten Enzymen des Krebszyklus fördern die Karzinogenese durch die Produktion von Einstoffmetaboliten, einschließlich 2--Hydroxyglutarat und Citrat, erhöhte Fettsäureoxidation und Induktion des epithelial-mesenchymalen Übergangs (EMT) [47].
Darüber hinaus wurden Mutationen in mtDNA, insbesondere in Genen für die Komplexe I, IⅢ, IV und V, die eng mit OXPHOS und der Redoxregulation assoziiert sind, in Endometrium-, Zervix-, Brust- und epithelialen Eierstockkrebszellen beobachtet [44,46,48 ]. Insbesondere sind Mutationen im Komplex I mit einem höheren -Ketoglutarat/Succinat-Verhältnis assoziiert, das die Tumorentstehung durch Hypoxie-induzierbarer Faktor 1 (HIF1)-Destabilisierung fördert [49]. Obwohl Mutationen in der mtDNA zu einer mitochondrialen Dysfunktion und dem Potenzial zur Krebsentstehung führen, beeinflussen diese Mutationen auch die nukleäre Genexpression durch retrograde Signalübertragung [44].

2.2. Mitochondriale Dysfunktion bei Herz-Kreislauf-Erkrankungen
Herz-Kreislauf-Erkrankungen sind die Hauptursache für weltweite Mortalität und Morbidität [50]. Mitochondrien spielen eine zentrale Rolle in der Homöostase des Herzens. Die mitochondriale Morphologie reagiert auf Veränderungen in Kardiomyozyten [51]. Mitochondriale Erkrankungen, die bevorzugt das Herz betreffen, sind mit mitochondrialen Dysfunktionen assoziiert, wie z. B. Störungen in OXPHOS oder dem ETC[52]. Strukturelle und funktionelle Veränderungen in mitochondrialen Organellen verursachen ischämische Kardiomyopathie, Herzinsuffizienz und Schlaganfall [53].
Darüber hinaus führen Störungen der mitochondrialen Dynamik, einschließlich mitochondrialer Fusion, Spaltung, Biogenese und Mitophagie, zur Entwicklung und Progression von CVDs wie diabetischer Kardiomyopathie, Atherosklerose, Schäden durch Ischämie-Reperfusion, Herzhypertrophie und dekompensierter Herzinsuffizienz [54]. Mehrere Kerngene, die die Aufrechterhaltung und Replikation der mtDNA regulieren, einschließlich des mitochondrialen Transkriptionsfaktors A (TFAM), der mtDNA-Polymerase (POLG) und PEO1 (Twinkle), sind bei CVDs verändert 【55】. Außerdem fördern mtDNA-Mutationen, die die mtDNA-Genexpression dysregulieren, die Pathogenese von Schlaganfall und Myokardinfarkt [56]. Darüber hinaus verursacht Hypoxie Veränderungen in zellulären Mechanismen, die zu oxidativem Stress und anschließender mitochondrialer Dysfunktion führen [57].
In patients with atherosclerosis and associated CVDs dysfunctional mitochondria affect cellular respiration and energy production and also act as dangerous ROS generators leading to the induction of apoptosis [58]. The accumulation of ROS and RNS in the heart by dysfunctional mitochondria is associated with several CVDs, including cardiomyopathies and heart failure [59,60]. Interestingly, ROS production caused by TFAM dysfunction is related to mtDNA damage and consequent cardiomyocyte cell cycle arrest resulting in lethal cardiomyopathy [61]. Moreover, the prognosis of cardiomyopathy is poor in children with mitochondrial diseases, especially those with mtDNA defects, including the m.3243A>G mutation in mitochondrially encoded tRNA-Leu(UUA/G)1(MT-TL1), the m.13513G>A mutation in mitochondrially encoded NADH: Ubiquinone oxidoreductase core subunit 5(MT-ND5), the m.8528T>Cmutation in the overlapping region of mitochondrially encoded ATP synthase membrane subunits 6(MT-ATP6) and 8(MT-ATP8), the m.3302A>G mutation in MT-ND1, the m.1644G>Eine Mutation in mitochondrial kodierter tRNA Valin (MT-TV) und pathogene Mutationen in BolA-Familienmitglied 3 (BOLA3) und Tafazzin TAZ. Kinder mit den erwähnten mitochondrialen Mutationen haben ein höheres Risiko für Kardiomyopathie und die damit verbundene Sterblichkeit. Daher könnte die genetische Analyse mit detaillierter Phänotypisierung von mitochondrialen Beeinträchtigungen für die Prognose einer Kardiomyopathie hilfreich sein [62]. Darüber hinaus können mehrere Kerngenmutationen die mitochondriale Atmungskette und ihre Komponenten direkt beeinflussen. Die Veränderungen in den Genen von Komplex I (NDuFS1, NDuFS2, NDUFS3), Komplex IV (SURF1, SCO1, SCO2, COX10, COX15), Komplex V (ATP12, TMEM70), mitochondrialer Translation (TACO1, EFG1) und Cardiolipin-Biosynthese (TAZ ) sind mit Kardiomyopathie assoziiert [59]. Darüber hinaus repräsentieren intermyofibrilläre Mitochondrien ein gut organisiertes Netzwerk aus langen und dichten Organellen und kontraktilen Myofilamenten. Bei Herzinsuffizienz verringert eine Störung der physikalischen und chemischen Wechselwirkungen zwischen den intermyofibrillären Mitochondrien und dem sarkoplasmatischen Retikulum die Kontraktilität der Kardiomyozyten und induziert den Zelltod [63]. Darüber hinaus kann Herzinsuffizienz durch mitochondriale Kalziumüberlastung, höhere ROS-Freisetzung und verringerte ATP-Produktion gekennzeichnet sein [64]. Während einer Herzinsuffizienz erhöht eine Kalziumüberladung üblicherweise die mitochondriale Spaltung und Dysfunktion. In der Folge führen diese Prozesse zu einer Abnahme der Herztätigkeit, die durch eine verminderte Fähigkeit gekennzeichnet ist, die linke Herzkammer bedarfsgerecht zu füllen und Blut auszustoßen. Diese metabolische Anforderung des Herzens könnte mit Veränderungen der Herzfrequenz, des inotropen Zustands des Myokards und der Spannung der Myokardwand in Verbindung gebracht werden, die letztendlich eine Herzschädigung begünstigen. Die Kalziumakkumulation ist auch mit einer Verringerung der mitochondrialen Energetik (ATP-Produktion) verbunden, die zu negativen Veränderungen von ETC und OXPHOS führt, die mit der Erzeugung von zellschädigenden ROS und Apoptose-Induktion verbunden sind [65]. Darüber hinaus ist Cardiolipin ein wichtiges mitochondriales Phospholipid in der inneren mitochondrialen Membran, das für die Aktivität des ETC erforderlich ist. Der Verlust von Cardiolipin verursacht eine ROS-Produktion, die mit der Störung der Cardiolipin-Peroxidation und der Cytochrom-c-Freisetzung verbunden ist, was zur Apoptose der Kardiomyozyten führt. Bei Herzinsuffizienz führt dieser Teufelskreis zu einer mitochondrialen Dysfunktion und nachfolgendem Kardiomyozytentod [66].
2.3. Mitochondriopathien in der Neurodegeneration
Eine normale mitochondriale Dynamik ist wichtig, um die Polarität in stark polarisierten Neuronen aufrechtzuerhalten [67,68]. Der neuronale Zelltod bei Hirnerkrankungen (Neurodegeneration) und Verletzungen (Neurotoxizität und Ischämie) ist mit verschiedenen Veränderungen der mitochondrialen Homöostase und/oder Funktion verbunden, darunter Verkehr, Qualitätskontrolle, Umsatz, Bioenergetik, Elektronentransport und Signalübertragung [69]. Neuronen sind mehr auf OXPHOS angewiesen, um ihren Energiebedarf zu decken als andere Zelltypen [70]. Neurodegenerative Erkrankungen sind auch durch die allmähliche Akkumulation von mtDNA-Mutationen gekennzeichnet, die möglicherweise die ETC- und ATP-Produktionseffizienz verringern und die ROS-Produktion erhöhen können [71]. Ein höherer ROS-Spiegel könnte weitere mtDNA-Mutationen in einem „Teufelskreis“ verursachen, der zum Zelltod führt [72]. Darüber hinaus wurden bei verschiedenen neurodegenerativen Erkrankungen, einschließlich der Alzheimer-Krankheit (AD), der Parkinson-Krankheit (PD) und der Pick-Krankheit, Anomalien des Mikrotubuli-assoziierten Proteins Tau (Tau) beobachtet [73]. Mitochondriale Dysfunktion ist eng mit der Tau-Pathologie bei AD verbunden; Es wird vermutet, dass die Überexpression von hyperphosphoryliertem und aggregiertem Tau den axonalen Transport schädigt und die abnormale Verteilung von Mitochondrien verursacht [74].
Mitochondriale Dysfunktion und oxidativer Stress tragen zu AD und PD bei, den beiden häufigsten altersbedingten neurodegenerativen Erkrankungen [71]. AD, eine Form der Altersdemenz, ist durch die Anhäufung geschädigter Mitochondrien während des Alterns gekennzeichnet. Die extrazelluläre Ablagerung von Amyloid-Peptid(A)-Plaques und die intrazelluläre Bildung von neurofibrillären Tangles (NFIs) treten in der Großhirnrinde von AD-Patienten auf [75]. Bei AD verursachen Oligomere von A mit hyperphosphoryliertem pTau den Verlust der synaptischen Funktion und kognitive Beeinträchtigung [76,77]. Mehrere Mutationen sind eng mit der mitochondrialen Funktion verbunden, einschließlich derer in den Genen, die das Amyloid-Vorläuferprotein (APP), Presenilin 1 (PSEN1) und 2 (PSEN2) und Apolipoprotein E (APOE4) kodieren, die zur Entwicklung von AD führen. Verschiedene Missense- oder Deletionsmutationen des mitochondrialen APP verursachen die vererbte Form von AD[73]. Neben APP-Mutationen werden Mutationen in PSENI und PSEN2 bei früh einsetzender familiärer AD beobachtet [78]. Darüber hinaus hängt der Beitrag von APOE4 zur AD-Pathogenese mit APOE4--vermittelten Veränderungen der A-Aggregation und -Clearance zusammen. APOE4-Mutationen stellen einen der wichtigsten genetischen Risikofaktoren für spät einsetzende sporadische AD dar [79].
Darüber hinaus gehören zu den pathologischen Merkmalen von PD der Verlust dopaminerger Neuronen in der Substantia nigra und das Vorhandensein von fehlgefaltetem -Synuclein (c-syn) in intrazytoplasmatischen Einschlüssen, die als Lewy-Körperchen bekannt sind [80]. PD entsteht aus verschiedenen mitochondrialen Dysfunktionen, einschließlich bioenergetischer und transkriptioneller Defekte, und Veränderungen in Dynamik (Fusion oder Spaltung), Größe, Morphologie, Verkehr, Transport und Bewegung. Zweifellos sind Mutationen in mtDNA, Kern-DNA und mitochondrialen Proteinen bei Parkinson gut beschrieben[81]. Daher Mutationen oder Störungen in E3-Ubiquitin-Ligase (Parkin), c-syn, einem Parkin-assoziierten Protein, das an oxidativem Stress beteiligt ist (DJ1), Ubiquitin-Carboxy-terminale Hydrolase L1 (UCHL1), Auxilin (DNAJC6), putative Serin-Threonin-Kinase (PINKT), Synaptojanin1 (SYN1), Serin-Peptidase 2 (HTRA2) und Endophilin A1 (SH3GL2) stören mehrere mitochondriale Funktionen und können die Entwicklung von Parkinson verursachen [12].

3. Klassifizierung und Funktionen der Flavonoide
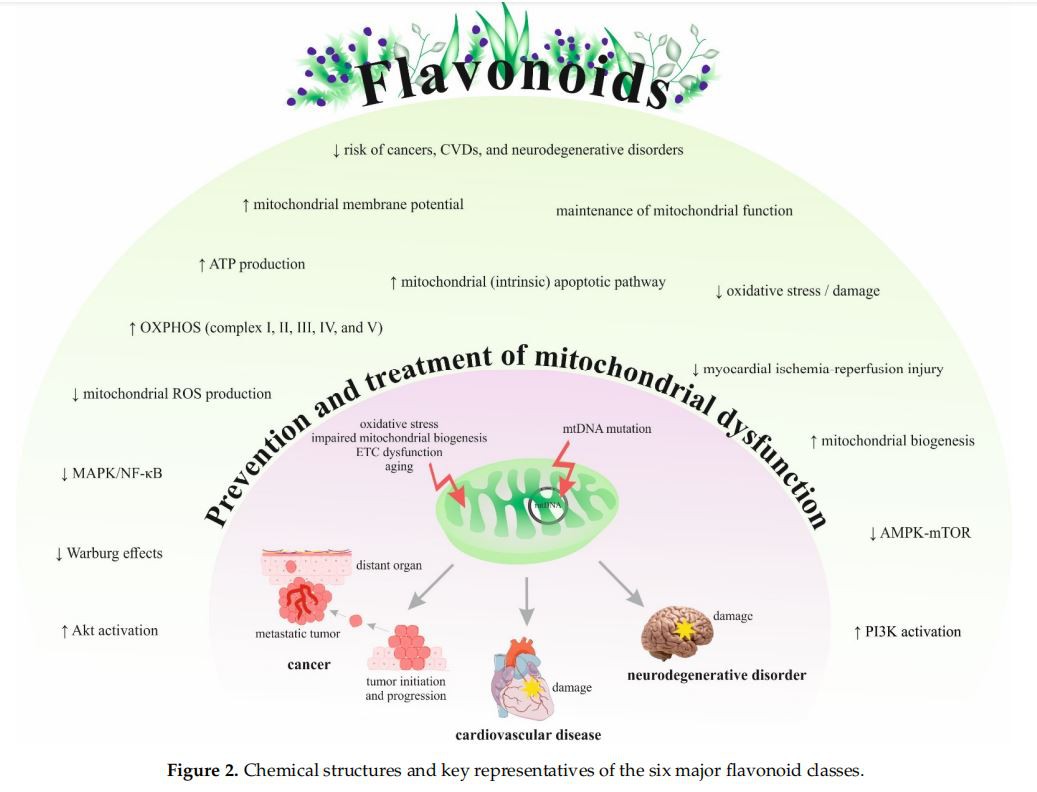
Flavonoide stellen eine wichtige Klasse von Naturstoffen dar. Alle Flavonoide werden in Pflanzen als bioaktive Sekundärmetaboliten synthetisiert und enthalten ein grundlegendes Flavanskelett, das aus einer 15-Kohlenstoff-Phenylpropanoidkette (C6-C3-C6-System) mit einer charakteristischen polyphenolischen Struktur besteht aus zwei Phenylringen und einem heterocyclischen Pyranring [82,83]. Flavonoide können in sechs Hauptgruppen eingeteilt werden: Isoflavonoide, Flavanone, Flavanole, Flavanole, Flavone und Anthocyanidine [84]. Zusätzliche Nebenklassen von Flavonoiden umfassen Chalkone, Dihydrochalkone und Aurone, die in Nebenflavonoide kategorisiert werden [85, 86]. Darüber hinaus sind Flavonoide in pflanzlichen Lebensmitteln reichlich vorhanden und werden daher durch Obst, Gemüse, Nüsse, Samen, Körner, Rinde, Wurzeln, Stängel, Blumen, Tee und Wein konsumiert [84]. Die allgemeinen chemischen Strukturen [83] und die wichtigsten Vertreter der sechs Hauptklassen der Flavonoide [87,88] sind in Abbildung 2 dargestellt.
Flavonoide haben viele vorteilhafte Eigenschaften, wie z. B. antioxidative, Radikalfänger-, hepatoprotektive, kardioprotektive, entzündungshemmende, immunmodulatorische, antiangiogene, antivirale, krebsbekämpfende Aktivitäten und antidepressive Wirkungen [82, 89-91]. Verschiedene Flavonoide (Vitexin und Baicalin) und andere phytochemische Verbindungen wie Curcumin (Diarylheptanoid), Lycopin (Carotin) und Ginsenosid (Triterpene) haben neuroprotektive Wirkungen gegen ischämisch induzierte Verletzungen [92]. Darüber hinaus können Flavonoide mehrere wichtige mitochondriale Enzymwege modulieren [93]. Redoxpotentiale, die mit der chemischen Struktur von Flavonoiden verbunden sind, ermöglichen es diesen Verbindungen, ROS, einschließlich Hydroxyl-, Superoxid-, Alkoxyl-, Alkylperoxyl- und Stickoxidradikalen, thermodynamisch abzufangen [94]. Andererseits destabilisieren die oxidierten reaktiven Nebenprodukte des Redox- und Abfangmechanismus von Flavonoiden diese Verbindungen chemisch [95]. Bemerkenswerterweise variieren die Redox-Eigenschaften von Flavonoiden mit den zellulären Bedingungen, der Dosierung, der Behandlungszeit, dem experimentellen Modell, dem tumorerzeugenden Zustand und anderen Faktoren. Unter bestimmten zellulären Bedingungen wie dem Auftreten von Umweltfaktoren oder Stressoren können die Antioxidantien auch als Prooxidantien wirken. Die prooxidative Aktivität von Flavonoiden, z. B. Luteolin und Fisetin, kann durch die Fähigkeit charakterisiert werden, eine durch die Übergangsmetalle katalysierte Autoxidation zu durchlaufen, um Superoxidanionen zu produzieren [96,97]. Für die Bestimmung des prooxidativen Status ist es wichtig, verschiedene Reduktionsmittel-Oxidationsmittel-Marker wie Glutathion (GSH) zu GSSG, NADPH zu NAPD- und NADH zu NAD-[98] zu bewerten. Die prooxidativen Eigenschaften von Flavonoiden können durch Reaktionen mit verschiedenen Biomolekülen wie Lipiden, Proteinen und DNA oxidative Schäden verursachen [99,100].
Flavonoide weisen aufgrund ihrer schlechten Wasserlöslichkeit im Allgemeinen eine geringe orale Bioverfügbarkeit auf. Auch die Zusammensetzung ihrer Quellen kann ihre Bioverfügbarkeit beeinflussen. Daher ist das Darmmikrobiom entscheidend für die Absorption und den Metabolismus von Flavonoiden [101]. Anthocyanidine und Pro-Anthocyanidine haben die niedrigste Bioverfügbarkeit, während Quercetin-Glucoside, Catechin, Flavanone, Isoflavone und Gallussäure die höchste haben [102]. Dies ist die Frage, die aus biotechnologischer Sicht betrachtet werden muss, um ihre Bioverfügbarkeit zu erhöhen und die klinische Umsetzung zu erleichtern.
Flavonoide leisten einen wertvollen Beitrag zum Gerüst von 3 PM. Die Rolle von 3 PM besteht darin, prädiktive Analyseansätze durch kostengünstige gezielte Prävention und Personalisierung medizinischer Leistungen einzuführen. Prädispositionen und Frühdiagnostik, Ausrichtung auf Hochrisikopersonen, individualisiertes Patientenprofiling und Patientenstratifizierung könnten die therapeutischen Strategien für verschiedene Erkrankungen signifikant verbessern [12]. Flavonoide stellen trotz der oben genannten Einschränkungen umweltfreundliche und kostengünstige Substanzen mit minimalen Nebenwirkungen bei Langzeitanwendung dar. Gesundheitsfördernde Wirkungen von Flavonoiden sind vielversprechend für 15-Uhr-Konzepte, einschließlich prädiktiver Ansätze, gezielter Prävention und Personalisierung medizinischer Leistungen, die präventive und therapeutische Strategien positiv beeinflussen können, z ihre Ausbreitung bei Personen mit hohem Risiko [86].





