Perspektive auf den Antagonismus nichtsteroidaler Mineralokortikoidrezeptoren bei diabetischer Nierenerkrankung
Aug 21, 2023
Hintergrund
Diabetesist weltweit die Hauptursache für ESKD. Es wird geschätzt, dass 30 % der Personen mit Typ-1-Diabetes mellitus und 40 % der Personen mit Diabetes mellitus Typ 1 leidenTyp 2 Diabetesmellitus (T2DM) entwickeln eine Nierenerkrankung (1). Todesfälle im Zusammenhang mitdiabetische Nierenerkrankung(DKD) sind im Vergleich zu jeder anderen Art von CKD höher (2). Diese übermäßige Sterblichkeit ist hauptsächlich darauf zurückzuführenHerz-Kreislauf-Erkrankungen (CV).und die meisten Patienten mitDKDwird ohne Progression sterbenESKD(1). Daher ist der ungedeckte Bedarf an Therapien, die das Risiko einer DKD verringern, enorm.

KLICKEN SIE HIER, UM CISTANCHE FÜR CNI ZU ERHALTEN
Wirkmechanismen des Mineralocorticoid-Antagonismus in der diabetischen Niere
Die Mechanismen, durch die Diabetes entstehtNierenerkrankungsind unzählige. Hämodynamische Veränderungen, Stoffwechselstörungen, proinflammatorische und profibrotische Prozesse gipfeln in strukturellen Veränderungen innerhalb der Niere. Zu den Kennzeichen der DKD zählen glomeruläre Hypertrophie, glomeruläre Basalmembranverdickung und mesangiale Ausdehnung, Glomerulosklerose, tubulointerstitielle Fibrose und Entzündung sowie Arteriosklerose (1). In den letzten Jahren wurde unser Arsenal zur Behandlung von DKD durch die Hinzufügung von Natrium-Glucose-Cotransporter-2 (SGLT-2)-Inhibitoren und zuletzt durch den nichtsteroidalen Mineralocorticoid-Rezeptor-Antagonisten (MRA), Finerenon, erweitert. MRs sind physiologische Bindungsstellen für Aldosteron, Cortisol und in geringerem Maße Progesteron. Sie werden in verschiedenen Zellen der Niere exprimiert, darunter Epithelzellen des Sammelrohrs, Podozyten, Mesangialzellen, tubulointerstitielle Fibroblasten und Makrophagen (Abbildung 1). Im Sammelrohr fördert die MR-Aktivierung die Wiederaufnahme von Natrium, die Sekretion von Kalium und die Flüssigkeitsretention. In nichtepithelialen Zellen steuert die MR die Expression vieler proinflammatorischer und profibrotischer Gene, die mit dem Fortschreiten der DKD assoziiert sind. Die MR kann bei DKD unangemessen überaktiviert sein, was zu einer erhöhten NADPH-Oxidase-Aktivität und einer Hochregulierung proinflammatorischer Zytokine (z. B. TNF-a, IL-1b) und profibrotischer Proteine (z. B. Bindegewebswachstumsfaktor, transformierender Wachstumsfaktor b1, Plasminogenaktivator-Inhibitor 1, Matrix-Metalloproteinase 2). Der resultierende Schaden gipfelt in Glomerulosklerose und einer fortschreitenden tubulointerstitiellen Schädigung (3).
Durch die Bindung von Finerenon an den MR ändert sich seine Konfiguration, so dass Liganden (z. B. Aldosteron) nicht binden können, was die nachgeschaltete Transkription von proinflammatorischen und profibrotischen Faktoren verhindert (Abbildung 1) (3). Finerenon hat im Vergleich zu steroidalen Mineralocorticoid-Antagonisten, die die therapeutischen Wirkungen beeinflussen, unterschiedliche pharmakokinetische und physiologische WirkungenDKDund Serumkalium. Im Gegensatz zu den steroidalen MRAs (Spironolacton und Eplerenon) weist das nichtsteroidale MRA Fifinerenon eine höhere Selektivität für die MR auf und wirkt als inverser Agonist, während steroidale MRAs als partielle Agonisten wirken. Somit blockiert Fifinerenon die Aktivierung des Rezeptors in Abwesenheit eines Liganden, wodurch die Rekrutierung transkriptioneller Cofaktoren vollständiger unterbrochen wird (4). Bei vergleichbaren natriuretischen Dosen bewirkt Fifinerenon eine stärkere Hemmung proinflammatorischer und profibrotischer Gene in der Niere als Spironolacton oder Eplerenon. Es besteht auch ein geringeres Hyperkaliämierisiko. Zu den Effekten, die eine geringere Hyperkaliämie bei Fifinerenon begünstigen, gehören die kürzere Halbwertszeit, das Fehlen aktiver Metaboliten, eine ausgewogene Verteilung der MR-Selektivität zwischen Niere und Herz und eine geringere Hochregulierung des epithelialen Natriumkanals (5). Darüber hinaus bindet Fifinerenon im Gegensatz zu steroidalen MRAs auch an den mutierten MR S180L, einen Rezeptor, der paradoxerweise durch Progesteron aktiviert wird, das normalerweise ein MR-Antagonist ist, was entweder zu Schwangerschaftshypertonie oder einer Verschlechterung des Bluthochdrucks während der Schwangerschaft führt. Diese einzigartige Eigenschaft legt eine mögliche Verwendung in diesem Zustand nahe (5).
Klinischer Beweis
Bisher gab es zwei bemerkenswerte Studien zu nichtsteroidalen MRAs. In der FIDELIO-DKD-Studie (Finerenone in Reducing Kidney Failure and Disease Progression in Diabetic Kidney Disease) wurde die Rolle von Fifinerenon bei der Verlangsamung der CKD-Progression und der Reduzierung der kardiovaskulären Mortalität bei Patienten mit T2DM und CKD (n55674) vor dem Hintergrund der Behandlung mit einem Angiotensin-Converting-Enzym untersucht (ACE-Hemmer) oder ein Angiotensin-Rezeptor-Blocker (ARB). Die Teilnehmer hatten eine mittlere (SD) eGFR von 44,3 (12,6) ml/min pro 1,73 m2 und ein mittleres (Interquartilbereich) Urin-Albumin-Kreatin-Verhältnis von 852 (446–1634) mg/g. Es gab eine 18-prozentige Verringerung des primären Nierenerkrankungsergebnisses (ein Betrag von 40 %).Abnahme der eGFR, Nierenversagen, oder Tod vonNierenursachen). Darüber hinaus gab es eine 14-prozentige Reduzierung des sekundären CV-Ergebnisses (Tod durch).CV-Ursachen, nicht tödlicher Myokardinfarkt, nicht tödlicher Schlaganfall oder Krankenhausaufenthalt wegen Herzinsuffizienz) (6).
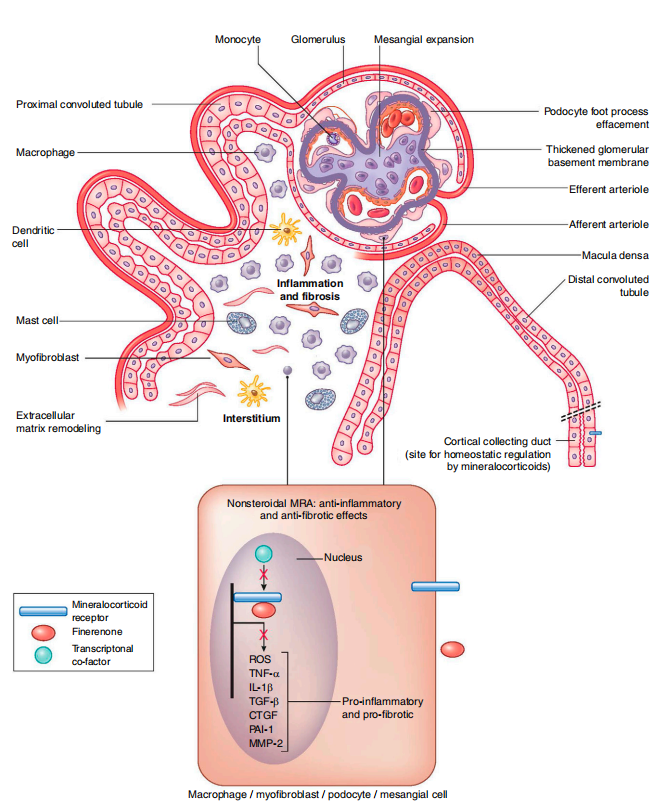
Abbildung 1.|Schematische Darstellung eines erkrankten Nephrons mit damit verbundenen strukturellen VeränderungenDiabetes. Die Bindung von Finerenon an den Mineralocorticoidrezeptor stört die Transkription proinflammatorischer und profibrotischer Faktoren. ROS, reaktive Sauerstoffspezies; CTGF, Bindegewebswachstumsfaktor; PAI-1, Plasminogenaktivator-Inhibitor 1; MMP-2, Matrix-Metalloproteinase 2.

Die Wirksamkeit und Sicherheit von Finerenon bei Patienten mitTyp 2 DiabetesMellitus und die klinische Diagnose vonDiabetische Nierenerkrankung(FIGARO-DKD)-Studie (n57352) bewertete das gleiche CV-Ergebnis wie in FIDELIO-DKD als primäres Ergebnis und das Nierenerkrankungsergebnis als primäres sekundäres Ergebnis bei Patienten mit T2DM und weniger schwerer CKD mit einer mittleren (SD) eGFR von 67,8 ( 21,7) ml/min pro 1,73 m2 und mittleres (IQR) Urin-Albumin-Kreatin-Verhältnis 308 (108–740) mg/g. Im Vergleich zur Placebo-Gruppe kam es in der Fifinerenon-Gruppe zu einer Reduzierung des primären kardiovaskulären Ergebnisses um 13 %. Obwohl es eine Reduzierung gabsekundäre NierenerkrankungDas Ergebnis in der Finerenon-Gruppe erreichte keine statistische Signifikanz (7).

Um die Sicherheit und Wirksamkeit von Finerenon bei Personen mit T2DM in einem breiten Spektrum von CKD zu untersuchen, wurde eine vorab festgelegte Analyse kombinierter FIDELIO-FIGARO-Studien namens FIDELITY durchgeführt. Für diese gepoolte Analysepopulation (n513.026) mit einer mittleren Nachbeobachtungszeit von 3 Jahren gab es einen Rückgang des kardiovaskulären Ergebnisses um 14 % und einen Rückgang des kombinierten Ergebnisses einer Nierenerkrankung um 23 % (Zeit bis zum Nierenversagen, dauerhaft 57 %). Rückgang der eGFR oder nierenbedingter Tod) (8). Als Ergebnis dieser klinischen Studien erhielt Finerenon die Zulassung der US-amerikanischen Food and Drug Administration zur Reduzierung des Fortschreitens von CKD, kardiovaskulärer Ereignisse und Krankenhauseinweisungen aufgrund von Herzinsuffizienz bei Patienten mit CKD aufgrund von T2DM.
Die Standardbehandlung bei DKD ist ein ACE-Hemmer oder ein ARB und ein SGLT2-Hemmer. Auf der Grundlage der verfügbaren Beweise kann Fifinerenon als ausgezeichnete Wahl für Patienten mit DKD angesehen werden, die keinen SGLT2-Hemmer einnehmen können, oder für Patienten mit anhaltend erhöhter Albuminurie trotz Behandlung mit der Standardtherapie. Die Dosis und Titration von Finerenon hängen sowohl von der eGFR als auch vom Serumkalium ab. Die volle Dosis von Fifineron beträgt 20-mg täglich. Personen mit einer eGFR von 25–60 ml/min pro 1,73 m2 oder einem Serumkaliumwert von 4,8–5 mEq/L wird gemäß der Kennzeichnung der US-amerikanischen Food and Drug Administration die niedrigere Dosis von 10 mg täglich empfohlen (Tabelle 1).
Risiko einer Hyperkaliämie
Ein Hauptrisiko für MRAs ist Hyperkaliämie, und in der Finerenon-Gruppe in FIDELIO-FIGARO wurde ein erhöhtes Risiko für Hyperkaliämie beobachtet. Insgesamt scheint das Risiko einer Hyperkaliämie bei einer nichtsteroidalen MRA geringer zu sein als bei einer steroidalen MRA. In einem CKD-Rattenmodell war das Risiko einer Hyperkaliämie mit dem nichtsteroidalen MRA PF-03882845 im Vergleich zu Eplerenon deutlich geringer (5). Die Mineralocorticoid Receptor Antagonist Tolerability Study (ARTS) war eine Phase-2-Studie zur Bewertung der Sicherheit von feinerem Enon (BAY 94–8862) im Vergleich zu Spironolacton bei Patienten mit Herzinsuffizienz mit reduzierter Ejektionsfraktion und leichter oder mittelschwerer chronischer Nierenerkrankung. Finerenon war im Vergleich zu Spironolacton mit einem geringeren mittleren Anstieg des Serumkaliumspiegels verbunden (9). Obwohl die maximale Tagesdosis von Finerenon bei ARTS 10 mg im Vergleich zu 20 mg bei FIDELIO-FIGARO betrug, stützen das präklinische CKD-Modell (5) und Daten von ARTS ein geringeres Risiko einer Hyperkaliämie unter Fifinerenon im Vergleich zu steroidalen MRAs. Darüber hinaus kann das Risiko einer Hyperkaliämie durch MRA durch SGLT-2-Hemmung gemindert werden. Durch die Erhöhung des Urinflusses im kortikalen Verbindungskanal könnten SGLT-2-Inhibitoren die Kaliumausscheidung fördern (10). Interessanterweise werden große Kaliumkanäle, die Kalium absondern, über die Mechanosensierung von Urin-Fellows durch interkalierte Zellen aktiviert, ohne dass ein direkter Austausch gegen Natrium erforderlich ist, obwohl ein langfristiger Anstieg der Urin-Follower den epithelialen Natriumkanal aktivieren und die Natrium-Wiederaufnahme in benachbarte Hauptzellen fördern kann und tragen so dazu bei, das elektrochemische Gleichgewicht im Filtrat aufrechtzuerhalten (11). Tatsächlich ergab eine aktuelle Post-hoc-Analyse von CREDENCE, dass Canagliflozin im Vergleich zu Placebo das Risiko einer Hyperkaliämie bei Studienteilnehmern mit DKD um etwa 20 % reduzierte (12). Eine weitere Post-hoc-Analyse von FIDELIO-DKD zeigte, dass das Risiko einer Hyperkaliämie bei Anwendern von SGLT-2-Inhibitoren um mehr als die Hälfte reduziert war (13). Bei Patienten mit chronischer Nierenerkrankung, die mit Fifinerenon behandelt werden, ist jedoch eine sorgfältige Überwachung des Serumkaliumspiegels mit gegebenenfalls einer Dosisanpassung oder Behandlungsunterbrechung erforderlich (Tabelle 1).
Auswirkungen auf den Blutdruck
Es ist wichtig zu beachten, dass die entzündungshemmenden und antifibrotischen Wirkungen der nichtsteroidalen MRA weitgehend unabhängig von der Blutdrucksenkung sind. In der FIDELIO-FIGARO-Studie waren die Auswirkungen von Fifinerenon auf den Blutdruck nominal (6,7). Bei ARTS senkte Spironolacton den systolischen Blutdruck, während der Blutdruck zwischen Placebo und Fifinerenon nicht schwankte (9). Eine geringere Senkung des Blutdrucks durch Fifinerenon wurde auf die kürzere Halbwertszeit und die geringere Wirkung auf die Natriurese zurückgeführt (7). Daher haben die steroidalen Mineralocorticoid-Antagonisten eine stärkere blutdrucksenkende Wirkung, weshalb diese Wirkstoffe bevorzugt zur Behandlung von Bluthochdruck eingesetzt werden
Zukünftige Richtungen
Da SGLT-2-Inhibitoren und Fifinerenon die behördliche Zulassung für die Behandlung von DKD erhalten haben, stehen uns nun neue Therapien zur Verbesserung der Nierengesundheit zur Verfügung. ACE-Hemmer und ARBs, SGLT-2-Hemmer und Fifinerenon wirken durch komplementäre Mechanismen zum Schutz der Nieren und des Herzens. Zukünftige Forschungen werden klären, wie diese Therapien in Kombination eingesetzt und auf einzelne Patienten zugeschnitten werden können. Wir gehen davon aus, dass sich die Nierenpflege in Zukunft von der Behandlung fortgeschrittener Nierenerkrankungen und Nierenversagen hin zur Förderung der Nierengesundheit und der Prävention von Krankheiten verlagern wird. Jetzt verfügen wir über ein wachsendes Arsenal sicherer und wirksamer Therapien, und es ist unbedingt erforderlich, sich auf deren Verbreitung und Umsetzung für Millionen von Menschen mit DKD auf der ganzen Welt zu konzentrieren, die davon profitieren können
Offenlegung
K. Tuttle berichtet über eine aktuelle Anstellung bei Providence Health Care und der University of Washington; Berichte über Beraterverträge mit AstraZeneca, Bayer, Boehringer Ingelheim, Eli Lilly, Gilead, Goldfinch Bio und Novo Nordisk; berichtet, dass sie Forschungsgelder von Bayer und Goldfinch Bio erhalten; Berichte über den Erhalt von Honoraren von Bayer, Gilead und Goldfinch Bio; und berichtet als wissenschaftlicher Berater oder Mitglied von CJASN, Kidney Health Initiative, Lancet Diabetes Endocrinology, National Institute of Diabetes and Digestive and Kidney Diseases und Nature Reviews Nephrology. Der verbleibende Autor hat nichts preiszugeben.
Verweise
1. Alicic RZ, Rooney MT, Tuttle KR: Diabetische Nierenerkrankung: Herausforderungen, Fortschritte und Möglichkeiten. Clin J Am Soc Nephrol 12: 2032–2045, 2017 https://doi.org/10.2215/CJN.11491116
2. Thomas B: Die globale Belastung durch diabetische Nierenerkrankungen: Zeittrends und geschlechtsspezifische Unterschiede. Curr Diab Rep 19: 18, 2019 https://doi.org/10.1007/s11892-019-1133-6 3. Bauersachs J, Jaisser F, Toto R: Mineralocorticoid-Rezeptor-Aktivierung und Mineralocorticoid-Rezeptor-Antagonisten-Behandlung bei Herz- und Nierenerkrankungen. Hypertension 65: 257–263, 2015 https://doi.org/10.1161/HYPERTENSIONAHA.114.04488 4. Grune J, Beyhoff N, Smeir E, Chudek R, Blumrich A, Ban Z, Brix S, Betz IR, Schupp M, Foryst-Ludwig A, Klopflfleisch R, Stawowy P, Houtman R, Kolkhof P, Kintscher U: Selektiver Mineralocorticoid-Rezeptor Cofaktormodulation als molekulare Grundlage für die antifibrotische Aktivität von Fifinerenon. Hypertonie 71: 599– 608, 2018 https://doi.org/10.1161/HYPERTENSIONAHA.117. 10360 5. Agarwal R, Kolkhof P, Bakris G, Bauersachs J, Haller H, Wada T, Zannad F: Steroidale und nichtsteroidale Mineralocorticoid-Rezeptor-Antagonisten in der kardiorenalen Medizin. Eur Heart J 42: 152–161, 2021 https://doi.org/10.1093/eurheartj/ehaa736 6. Bakris GL, Agarwal R, Anker SD, Pitt B, Ruilope LM, Rossing P, Kolkhof P, Nowack C, Schloemer P, Joseph A, Filippatos G; FIDELIO-DKD-Forscher: Wirkung von Fifinerenon auf die Folgen chronischer Nierenerkrankungen bei Typ-2-Diabetes. N Engl J Med 383: 2219–2229, 2020 https://doi.org/10.1056/NEJMoa2025845
Unterstützender Service:
E-Mail:wallence.suen@wecistanche.com
WhatsApp/Tel:+86 15292862950
Geschäft:
https://www.xjcistanche.com/cistanche-shop






