Nierenschützende Rolle von Liponsäure bei Nierenerkrankungen
Aug 31, 2023
Abstrakt:Die Niere ist ein wichtiges Organ, das Stoffwechselabfälle ausscheidet und Nährstoffe wieder aufnimmt. Es ist auch an der Regulierung des Blutdrucks, der Aufrechterhaltung des Elektrolytgleichgewichts und der pH-Homöostase des Blutes sowie an der Erythropoese und der Reifung von Vitamin D beteiligt. Aufgrund dieser hohen Arbeitsbelastung ist die Niere ein energieverbrauchendes Organ und ständig endogenen und exogenen Belastungen ausgesetzt, was zur Entwicklung beider Faktoren führtakute Nierenschädigung(AKI) oderchronisches Nierenleiden(CKD). Dennoch gibt es keine therapeutischen Möglichkeiten zur wirksamen Behandlung von AKI oder CKD. Daher sind neuartige Therapieansätze zur Bekämpfung von Nierenschäden dringend erforderlich. In diesem Übersichtsartikel wird die Rolle von -Liponsäure (ALA) bei der Vorbeugung und Behandlung von Nierenerkrankungen erörtert. Wir konzentrieren uns auf verschiedene Tiermodelle von Nierenschäden, durch die die zugrunde liegenden renoprotektiven Mechanismen von ALA entschlüsselt wurden. Zu den abgedeckten Tiermodellen gehören diabetische Nephropathie, Sepsis-induzierte Nierenschädigung, renale ischämische Schädigung, einseitige Harnleiterobstruktion und Nierenschäden, die durch Folsäure und Metalle wie Cisplatin, Cadmium und Eisen hervorgerufen werden. Wir beleuchten die gemeinsamen Mechanismen der Nierenschutzwirkung von ALA, zu denen die Verringerung oxidativer Schäden, die Erhöhung der antioxidativen Kapazitäten, die Bekämpfung von Entzündungen, die Linderung von Nierenfibrose und die Abschwächung des Nephronzelltods gehören. Durch diese Mechanismen erfüllt ALA seine biologische Funktion, Nierenschäden zu lindern und die Nierenfunktion zu verbessern. Dennoch weisen wir auch darauf hin, dass umfassendere präklinische und klinische Studien erforderlich sein werden, um ALA zu einem besseren Therapeutikum zur Behandlung von Nierenerkrankungen zu machen.
Schlüsselwörter: Liponsäure;akute Nierenschädigung; chronisches Nierenleiden; diabetische Nierenerkrankung; diabetische Nephropathie; Nephroprotektion

KLICKEN SIE HIER, UM CISTANCHE FÜR CNI-BEHANDLUNGEN ZU ERHALTEN
1. Einleitung
Die Niere ist ein lebenswichtiges Organ, das an der Aufrechterhaltung des Elektrolytgleichgewichts, der pH-Stabilität des Blutes, der Entfernung von Stoffwechselabfällen und der Rückresorption von Nährstoffen und Mineralien beteiligt ist [1,2]. Die Niere ist auch an der Erythropoese, der Reifung von Vitamin D und der Regulierung des Blutdrucks beteiligt [3]. Unter pathophysiologischen Bedingungen wie Fasten, langfristigem Hungern und Insulinresistenz kann die Niere auch Glukose über die Gluconeogenese unter Verwendung von Vorläufermolekülen wie Glycerin, Alanin, Pyruvat und Laktat regenerieren [4]. Dadurch ist die Niere stets einer hohen Belastung ausgesetzt und somit zahlreichen Risikofaktoren ausgesetzt, die zu Nierenerkrankungen oder -verletzungen führen können. Es gibt zwei Arten von Nierenerkrankungen: chronische Nierenerkrankung (CKD) [5] und akute Nierenschädigung (AKI) [6]. CKD tritt auf, wenn die Nierenfunktion über einen Zeitraum von mehr als drei Monaten aufgrund einer Schädigung der glomerulären Filtration und tubulärer Verletzungen allmählich abnimmt [7]. Es wurde prognostiziert, dass CNI bis 2040 die fünfthäufigste Todesursache weltweit sein wird [8]. Andererseits tritt AKI auf, wenn die Nierenfunktion weniger als drei Monate lang rapide abnimmt und dies durch Azidose, Flüssigkeitsüberladung und Anomalien bei Elektrolyten und hämatologischen Veränderungen angezeigt wird [7]. Es ist auch bekannt, dass Personen mit CKD ein erhöhtes Risiko für AKI haben können [8]. Derzeit gibt es keine pharmazeutischen Produkte zur Heilung von AKI oder CKD. Während die Nierendialyse häufig eingesetzt wird, um weitere Schäden an den Nieren zu verhindern und ihre Funktion aufrechtzuerhalten, kann ein Nierenersatz der letzte Ausweg für das Überleben des Patienten sein. Daher können AKI und CKD, wenn sie nicht kontrolliert werden, zu Nierenversagen führen, was die Morbidität und Mortalität deutlich erhöht [7,9]. Daher besteht ein ungedeckter Bedarf bei der Bekämpfung von Nierenerkrankungen.
Zur Bekämpfung von Nierenerkrankungen wurden zahlreiche Therapieansätze erforscht [10–13]. Dazu gehören exogene und endogene Verbindungen, Ernährungsumstellungen, Modulation von Stoffwechselwegen, Stammzellansätze und Zellsignalprozesse [10,11,14–21]. In diesem Übersichtsartikel konzentrieren wir uns auf die Rolle von Liponsäure bei der Vorbeugung und Linderung von Nierenschäden. Insbesondere werden wir uns auf Studien an Tiermodellen konzentrieren, um die schützende Wirkung von Liponsäure bei Nierenschäden zu untersuchen. Zu diesen Tiermodellen für Nierenschäden gehören diabetische Nierenerkrankung oder diabetische Nephropathie, renale Ischämie-Reperfusionsschädigung, durch Sepsis verursachte Nierenschädigung, durch einseitige Harnleiterobstruktion (UUO) verursachte Nierenschädigung, Cisplatin-verursachte Nierenschädigung, Cadmium-induzierte Nierenschädigung, FolsäureSäurebedingte Nierenschädigung, UndEisenbedingte akute Nierenschädigung(Abbildung 1).
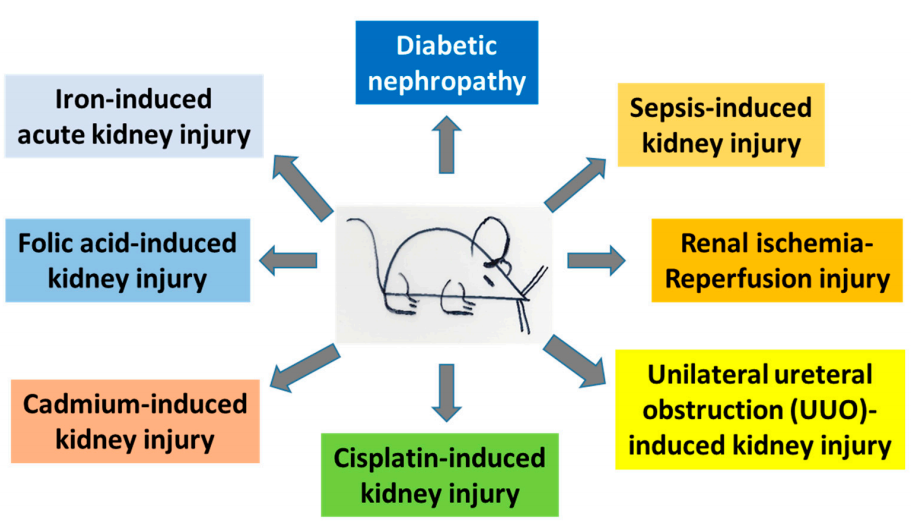
Abbildung 1. In diesem Artikel werden Tiermodelle für Nierenschäden besprochen. Diese Modelle umfassen sowohl akute Nierenschäden als auch chronische Nierenerkrankungen.
2. Alpha-Liponsäure
ALA ist eine natürlich vorkommende Dithiolverbindung [22]. Es ist ein Cofaktor für die -Ketoglutarat-Dehydrogenase, die Dehydrogenase verzweigtkettiger Aminosäuren und die Pyruvat-Dehydrogenase [23–25] (Abbildung 2). Daher ist ALA ein Energiemodulator [26,27] (Abbildung 3). Darüber hinaus wird ALA aufgrund seiner Fähigkeit, Thiolgruppen mit anderen Thiol-haltigen Molekülen wie Glutathion und den Cysteinresten von Proteinen auszutauschen, auch als Redoxmodulator bezeichnet [26–28] (Abbildung 3). ALA wird oft als universelles Antioxidans bezeichnet, da es sowohl in lipophilen als auch in hydrophilen Umgebungen als Antioxidans wirken kann, um Nebenprodukte des oxidativen Stoffwechsels, wie reaktive Sauerstoffspezies (ROS) und reaktive Stickstoffspezies (RNS), zu reduzieren (Abbildung 4) [29]. ]. ALA kann auch Metalle wie Zink, Eisen und Kupfer chelatisieren und endogene Antioxidantien – wie Glutathion – und exogene Vitaminantioxidantien – wie Vitamin C und E – mit minimalen Nebenwirkungen regenerieren [30] (Abbildung 4). Noch wichtiger ist, dass ALA auch Entzündungen hemmen kann, indem es auf NF-KB abzielt und die Freisetzung entzündungsfördernder Zytokine verringert (Abbildung 4). Daher wurde gezeigt, dass ALA durch das Abfangen freier Sauerstoffradikale die glomeruläre Funktion erhöhen und Nierenentzündungen verringern kann [31]. Studien haben auch gezeigt, dass die Behandlung mit ALA akute Nierenschäden verringern kann, indem sie den Harnstoffstickstoff im Serum senkt.Kreatininspiegel TumornekroseFaktor-Alpha (TNF-), Interleukin-6 (IL-6) und Interleukin-1 Beta (IL-1).abnehmendes Endothelin-1Vasokonstriktion, Neutrophilendiffusion und Entzündung in den Nieren.

Abbildung 2. Liponsäure ist ein Cofaktor des mitochondrialen 2--Ketosäure-Dehydrogenase-Komplexes, einschließlich des Pyruvat-Dehydrogenase-Komplexes, des -Ketoglutarat-Dehydrogenase-Komplexes und des verzweigtkettigen Aminosäure-Dehydrogenase-Komplexes. Die E1-Untereinheit ist 2-Ketosäuredecarboxylase mit TPP als Cofaktor; die E2-Untereinheit ist eine Dihydrolipoamid-Acyltransferase, die Liponsäure als Cofaktor verwendet; Die E3-Untereinheit ist eine Dihydrolipoamid-Dehydrogenase, die NAD+ als Elektronenakzeptor für die Oxidation der an die E2-Untereinheit gebundenen Lipoylgruppe nutzt. E3 katalysiert die Bildung der oxidierten Form der Liponsäure und erzeugt dabei NADH [32–34].

Abbildung 3. Liponsäure ist am Thiol-Disulfid-Austausch beteiligt, der den Redox- und Energiestatus der Zelle moduliert.
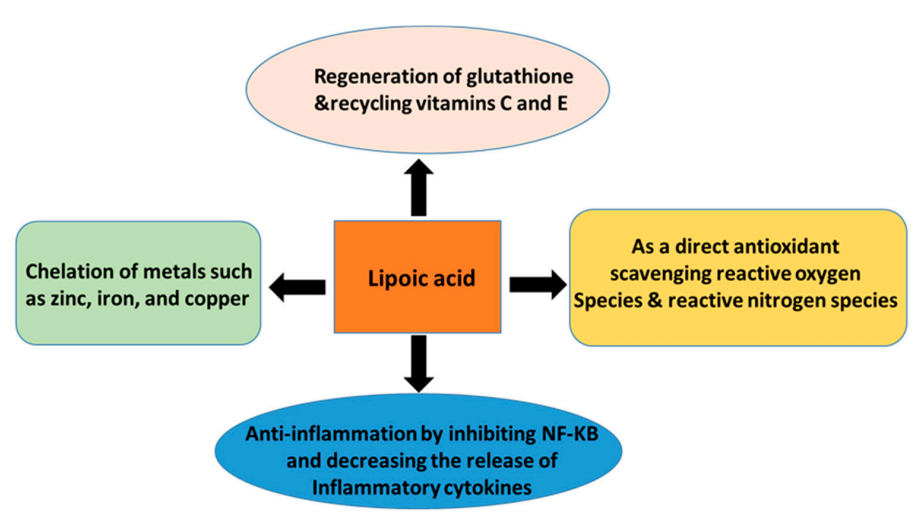
Abbildung 4. Biologische Wirkungen von Liponsäure und ihre möglichen Mechanismen, zu denen die Regeneration von Glutathion, den Vitaminen C und E, das Abfangen von ROS, die Chelatisierung von Metallionen und die entzündungshemmende Wirkung gehören

3. Schutzfunktionen von -Liponsäure (ALA) bei Nierenverletzungen
Nierenerkrankungen können durch eine Reihe von Beeinträchtigungen wie Diabetes, ischämische Reperfusion, Arzneimitteltoxizität, Kontrastmittel und Medikamente hervorgerufen werden [7]. Wenn AKI nicht kontrolliert wird, kann es zu Nierenversagen mit einer Sterblichkeitsrate von 20 % führen [25]. AKI ist gekennzeichnet durch einen Anstieg des Serumkreatinins, Oligurie und das Vorhandensein von Nierenschädigungsmarkern wie Albuminurie, Elektrolytanomalien aufgrund von tubulären Störungen oder strukturelle Schäden, die in der Bildgebung oder Histologie beobachtet werden [9]. Es wurde gezeigt, dass die ALA-Prophylaxe die Werte für Nierentubulusverletzungen, Harnschädigungsmarker und strukturelle Schädigungen des Serumkreatinins senkt und die glomeruläre Filtration erhöht [35]. In den folgenden Abschnitten werden wir die nephroprotektiven Wirkungen und die zugrunde liegenden Schutzmechanismen von ALA in verschiedenen Tiermodellen für Nierenschäden diskutieren, wie in Abbildung 1 dargestellt
3.1. Diabetische Nephropathie
Diabetische Nephropathie (DN), auch bekannt als diabetische Nierenerkrankung (DKD) [36–38], ist eine der Hauptursachen für CKD und Nierenversagen im Endstadium bei Diabetikern [39–41]. Es ist allgemein bekannt, dass eine mitochondriale Dysfunktion zur DKD beiträgt und das Mitochondrium ein Ziel für die Bekämpfung der DKD ist [42–44]. DN kann als mikrovaskuläre Komplikation bei Diabetes mellitus Typ 1 oder Typ 2 angesehen werden [7,41]. Diese diabetische Nierenerkrankung ist durch eine verminderte glomeruläre Filtration, Proteinurie und Nierenfibrose gekennzeichnet [7]. Hyperglykämie erhöht den oxidativen Stress und führt zu einer frühen Überproduktion reaktiver Sauerstoffspezies (ROS) [45] und einer Fehlregulation der Glutathion-Stoffwechselwege [7]. Malondialdehyd (MDA) ist das Endprodukt der Lipidperoxidation und wird häufig als guter Marker für freie Radikale und oxidativen Stress verwendet [46–49]. Studien haben gezeigt, dass eine Vorbehandlung mit ALA den MDA-Gehalt senkte und den oxidativen Stress der Nieren verbesserte [32,50]. Es wurde gezeigt, dass Lipoamid, ein ALA-Derivat, die Nierenfibrose bei Diabetes hemmt, indem es die Mitochondrienfunktion verbessert und die Expression der Aktivierung des Transkriptionsfaktors Retinal X-Rezeptor Alpha reguliert [51]. In einem Rattenmodell für Diabetes, der durch Nikotinamid zusammen mit Streptozotocin induziert wurde, einem weniger zeitaufwändigen Ansatz zur Erstellung von Nagetiermodellen für Diabetes [52], haben Dugbartey et al. haben auch gezeigt, dass der renale Schutzmechanismus von ALA die Aktivierung des renalen Cystathionin-Lyase/Schwefelwasserstoff-Systems beinhaltet [53]. Es wurde auch gezeigt, dass ALA in Kombination mit dem Angiotensin-II-Rezeptor-Inhibitor Valsartan eine synergistische Wirkung auf die Senkung der Serumspiegel entzündlicher Zytokine und die Verbesserung der Nierenfunktion bei diabetischen Tieren hat [54]. Abbildung 5 zeigt überzeugende Beweise für die histologische Färbung, dass ALA in einem Typ-2-Diabetes-Tiermodell eine starke schützende Wirkung auf die Nieren von Diabetikern hat. [55] Der Mechanismus des Nephroschutzes von ALA bei Diabetes ist seine Fähigkeit, den Nrf2-Signalweg zu aktivieren, was zu einer Hochregulierung des zweiten Phasenzytoprotektive Proteine wie Hämoxygenase-1 (HO-1) und NAD(P)H-Chinondehydrogenase 1 (NQO1) [56–58]. Es sollte darauf hingewiesen werden, dass ALA zwar nephroprotektiv bei diabetischer Nierenerkrankung ist, jedoch möglicherweise prooxidative oder toxische Wirkungen hat und unter bestimmten pathophysiologischen Bedingungen möglicherweise nicht als Nrf2-Induktor dient [59–61]. Darüber hinaus wurde zwar angenommen, dass ALA Insulinsignalwege zur Bekämpfung von Diabetes aktiviert [28] und nachweislich kardiometabolische Störungen und Nierenfunktionsstörungen, die durch einen hohen Fruchtzuckergehalt verursacht werden, verhindert [62], es wurde jedoch auch berichtet, dass ALA nur Proteinurie und oxidative Prozesse abschwächen kann Stress, ohne das Fortschreiten des diabetischen Nierenversagens zu verlangsamen [63].
3.2. Sepsis-induzierte Nierenverletzung
Sepsis ist ein potenziell lebensbedrohlicher pathologischer Zustand, der auf eine überschießende Entzündungsreaktion auf eine bakterielle Infektion zurückzuführen ist [64–66]. Eine schwere Sepsis kann zum Versagen mehrerer Organe führen, wobei die Niere das am stärksten betroffene Organ ist [67,68]. Es wurde geschätzt, dass fast 50 % der septischen Patienten eine akute Nierenschädigung entwickeln würden, und es gibt keine wirksamen Behandlungen für septisches AKI [69]. In diesem Zusammenhang haben zahlreiche Forscher die schützenden und therapeutischen Werte von ALA bei Sepsis-induziertem AKI, modelliert durch Injektion von Lipopolysacchariden, umfassend bewertet, obwohl gelegentlich durch Cacalpunktion und Ligatur (CPL) induzierte septische AKI eingesetzt wurde [22,70]. Es wurde gezeigt, dass ALA durch die Verbesserung der Autophagie vor septischen Nierenschäden schützen kann [71]. Darüber hinaus kann ALA auch Sepsis-induziertes AKI lindern, indem es Entzündungen durch Hemmung des NF-KB-Signalwegs entgegenwirkt [72], mitochondrialen oxidativen Stress abschwächt und den Na+/H+-Austauscher Typ 3 und die Aquaporin-2-Expression in der Niere aufrechterhält [73]. . ALA kann auch die Freisetzung von Tumornekrosefaktor, Interleukin (IL)-6 und IL-1 in das Serum hemmen und die Expression der induzierbaren Stickoxidsynthase [22] bei septischem AKI unterdrücken. Daher könnte ALA ein vielversprechendes Naturprodukt zur Behandlung septischer AKI sein.

3.3. Renale ischämische Reperfusion
Ischämie tritt auf, wenn die Blutperfusion abnimmt und die Durchblutung der Organe verringert ist [74]; Dies ist auf viele Ursachen zurückzuführen, wie zum Beispiel Thromben, Traumata und Arteriosklerose [75]. Um Gewebeschäden und Nekrose zu verhindern, wird die Ischämie durch Reperfusion behoben [75]. Obwohl eine ischämische Reperfusion zur Verhinderung von Gewebenekrose unerlässlich ist, kann sie auch Entzündungen und einen Anstieg reaktiver Sauerstoffspezies und reaktiver Stickstoffspezies verursachen [75–77]. Studien haben gezeigt, dass eine Vorbehandlung von ALA Schäden an Nieren, Netzhaut, Nervensystem, Leber, Darm und mehr lindern kann [75]. Die zugrunde liegenden Schutzmechanismen von ALA bei Nierenischämie-Reperfusionsschäden können multifaktoriell sein, einschließlich der Bekämpfung oxidativer Schäden [32,75] und der Herunterregulierung von Kanälen, Enzymen und Transportern wie Aquaporinen und Natriumtransportern sowie der Natrium-Kalium-ATPase und Stickstoffmonoxid-Synthase-Isoformen [78]. ALA kann auch Nierenischämie-Reperfusionsschäden schützen, indem es die Infiltration von Neutrophilen abschwächt und die Freisetzung von Entzündungsmediatoren hemmt [79]. Studien haben auch gezeigt, dass Schäden an der Nierenrindenstruktur, die durch eine Ischämie-Reperfusionsschädigung der Gliedmaßen verursacht werden, durch ALA gelindert werden können [80] und ALA zeigt in Kombination mit dem Xanthinoxidase-Inhibitor Febuxostat überlegene Schutzwirkungen bei Nierenischämie-Reperfusionsschäden [81] . ALA kann auch Nierenfunktionsstörungen und Nierenschäden verhindern, indem es die Überexpression von Endothelin-1 bei Nierenischämie-Reperfusionsschäden unterdrückt [82].
3.4. Durch einseitige Harnleiterobstruktion (UUO) verursachte Nierenverletzung
Das Tiermodell der unilateralen Harnleiterobstruktion (UUO) für Nierenschäden wurde häufig verwendet, um die Mechanismen von Nierenschäden und den therapeutischen Nutzen zahlreicher Wirkstoffe zu untersuchen [83–87]. Dieses Modell hat bestimmte Vorteile, da es sich um eine nichturämische normotensive Störung handelt, bei der keine offensichtliche entzündliche oder toxische Schädigung der Nieren vorliegt [88]. Darüber hinaus ist das UUO-Modell der Nierenschädigung auch ein gutes Modell für die Untersuchung der Pathophysiologie der Nierenfibrose [89–93]. Daher kann das UUO-Modell der Nierenschädigung die zugrunde liegende Pathophysiologie der menschlichen obstruktiven Nierenschädigung sehr gut nachahmen [94,95]. Es wurde gezeigt, dass ALA renoprotektiv gegen UUO-induzierte Nierenschäden ist [88]. Wongmekiat et al. haben herausgefunden, dass, wenn ALA (60/mg/kg Körpergewicht) Ratten zwei Tage vor der UUO-Induktion per ip-Injektion verabreicht wurde und eine Woche nach der UUO-Induktion fortgesetzt wurde, UUO-induzierte Nierenfunktionsstörung, oxidativer Stress und die Produktion von Stickoxid und Transformation verursacht wurden Faktor-1 wurden durch die ALA-Behandlung stark abgeschwächt [88]. Darüber hinaus wurde gezeigt, dass ALA den epithelial-mesenchymalen Übergang in einem Mausmodell einer UUO-Nierenschädigung verbessert [96]. Diese Studien zeigen somit, dass ALA nephroprotektiv gegen UUO-induzierte Nierenschäden ist.
3.5. Cisplatin-induzierte Nephrotoxizität
Cisplatin ist ein Chemotherapeutikum, das Krebs behandelt, indem es in die Tumorzellen eindringt, Chloridionen freisetzt und hydratisiert wird, um sich mit der DNA zu vernetzen und DNA-Addukte zu bilden, um die Tumorzellreplikation zu hemmen [97,98]. Cisplatin-Medikamente haben jedoch viele Nebenwirkungen, wie Ototoxizität, Neurotoxizität, Nephrotoxizität, Übelkeit und Erbrechen [35,97–99]. Nephrotoxizität tritt auf, weil Cisplatin von den proximalen Tubuluszellen aufgenommen wird und sich im Serum bis zu fünfmal stärker konzentrieren kann als Cisplatin [35,97]. Die Nephrotoxizität von Cisplatin führt zu einer verringerten Kreatinin-Clearance, einem erhöhten Serumkreatininspiegel, einem erhöhten Harnstoffspiegel, einer erhöhten Urinausscheidung und einer verringerten glomerulären Filtrationsrate 100,1011. Cisplatin verringert auch die Antioxidantien Glutathion-S-Transferase, Glutathionperoxidase und Superoxiddismutase, was zu einem Anstieg der ROS und oxidativen Markern wie MDA führt, die aus der Lipidperoxidation stammen [35,100,102]. Proximale Tubuli in den Nieren enthalten große Mengen an Mitochondrien (35). Hydrolysiertes Cisplatin erzeugt einen Metaboliten mit einer positiven Ladung, der sich aufgrund der negativ geladenen Moleküle der Mitochondrien in den Mitochondrien ansammelt und ein hohes Maß an oxidativem Stress erzeugt (35). Um dies zu bewältigen, müssen Mitochondrien Verwenden Sie endogene Antioxidantien wie Liponsäure, um ROS zu reduzieren (351. Studien haben gezeigt, dass ALA Nierenzellen vor der Toxizität von Cisplatin schützt (98), strukturelle Schäden an den proximalen Tubuli verringert und die glomeruläre Filtration in den Nieren erhöht (99,103). ALA hat sich auch gezeigt senken den Plasma-Kreatininspiegel und die Urinausscheidung, erhöhen die Kreatinin-Clearance und die Urinosmolalität und normalisieren die Natriumausscheidung bei Cisplatin-Nierenschäden [101].

3.6. Folsäure-induzierte Nephrotoxizität
Ein hoher Folsäurespiegel kann durch die Ablösung und Erweiterung tubulärer Zellen zu tubulären Schäden führen [104] und zum Zelltod führen [105]. Ferroptose ist eine Art von Zelltod, der durch Eisen- und Lipidperoxidation verursacht wird und während einer Folsäure-induzierten AKI auftritt [106]. Wenn große Mengen Eisen im Körper vorhanden sind, werden ROS erzeugt, die eine Lipidperoxidation verursachen, die Lipidmembranen schädigen und zum Zelltod führen [105]. Es wurde festgestellt, dass die antioxidative Wirkung von ALA zu einer Renoprotektion gegen Folsäure-induzierte Nierenschäden führte [105]. In der Studie von Li et al. gab es keinen signifikanten Unterschied zwischen niedrigen und hohen ALA-Dosen, was darauf hindeutet, dass der Nutzen von ALA nicht dosisabhängig ist [105]. Darüber hinaus kann ALA wirken, indem es p53 daran hindert, Ferroptose zu verursachen, und indem es Ferritin- und Ferroportin-Eisenexporteure hochreguliert, wodurch Folsäure-induzierter AKI verhindert wird [105]. Abbildung 6 zeigt histologisch die Visualisierung des ALA-Schutzes gegen durch Folsäure induzierte Nierenschädigung [105].
3.7. Cadmium-induzierte Nephrotoxizität
Cadmium ist ein natürlich vorkommendes toxisches Schwermetall, das nephrotoxisch wirkt [104,107–109]. Durch Cadmium induzierte Nephrotoxizität erhöht den MDA-Spiegel und verursacht Schäden an den Nierenmitochondrien und der Nierenrinde [110]. Es wurde auch gezeigt, dass Cadmium Glutathion-Antioxidans (GSH), Glutathionperoxidase, Katalase und Superoxiddismutase (SOD) verringert [110].
Die Behandlung mit ALA wirkte als Antioxidans, um MDA und Apoptose zu verringern und Cadmium zu chelatisieren, um Cadmiumschäden an den Nieren zu verringern [111]. ALA senkte auch den oxidativen Stress, förderte mit Glutathion in Zusammenhang stehende endogene Enzyme und verhinderte mitochondriale Apoptose bei Cadmium-induzierter Nierenschädigung [110–112].
3.8. Eiseninduzierte akute Nierenschädigung
Es wird angenommen, dass Eisen sowohl zu AKI als auch zu CKD beiträgt [113–118]. Tatsächlich wurde beobachtet, dass die Nierentubuli bei Patienten mit Nierenerkrankungen erhöhten Eisenwerten ausgesetzt sind, was wahrscheinlich auf eine erhöhte Filtration von Eisen und eisenhaltigen Proteinen durch den glomerulären Apparat zurückzuführen ist [114,117,119]. Eisen kann auch eine diabetische Nierenerkrankung verschlimmern, indem es den oxidativen Stress erhöht [120,121]. Daher waren eiseninduzierte Tiermodelle für Nierenschäden ein wertvolles Instrument zur Untersuchung der Mechanismen eiseninduzierter Nierenschäden und zum Testen der therapeutischen Wirkung von Naturprodukten oder Arzneimitteln [122–125]. In dieser Hinsicht hat sich gezeigt, dass ALA bei ioneninduzierter Nierenschädigung nephroprotektiv wirkt [126,127]. In einem Modell einer Nierenschädigung bei Ratten mit Eisenüberladung wurde festgestellt, dass ALA eine antioxidative Wirkung entfaltet, indem es oxidative Schäden abschwächt [128]. Es wurde auch festgestellt, dass ALA die p38-MAPK-Signalübertragung und die NADPH-Oxidase-4-Expression bei eiseninduzierter Nierenschädigung hemmt [127]. Es ist zu beachten, dass alle diese schützenden Wirkungen von ALA bei eiseninduzierten Nierenschäden teilweise auf seine eisenchelatbildende Eigenschaft zurückzuführen sein können [128–131], die die Verfügbarkeit von freiem Eisen verringert.
Unterstützender Service:
E-Mail:wallence.suen@wecistanche.com
WhatsApp/Tel:+86 15292862950
Geschäft:
https://www.xjcistanche.com/cistanche-shop






