Übersicht über Gentests bei Patienten mit Nierenerkrankungen: Diagnostische Ausbeute einzelner Nukleotidvarianten und Variationen der Kopienzahl, bewertet über und innerhalb von Nierenphänotypgruppen
Aug 16, 2023
AbstraktGenetische Nierenerkrankungumfasst eine vielfältige Gruppe von Störungen. Diese lassen sich grob in die Phänotypgruppen angeborene Anomalien einteilenNiere und Harnwege, Ziliopathien, Glomerulopathien, Steinerkrankungen, tubulointerstitielle Nierenerkrankung und Tubulopathien. Viele Ursachen können zu einer chronischen Nierenerkrankung führen, die zu einer Nierenerkrankung im Endstadium führen kann. Obwohl jede einzelne Krankheit selten ist, machen diese genetischen Störungen zusammen einen großen Teil der Fälle von Nierenerkrankungen aus. Mit der Einführung der massiv parallelen Sequenzierung sind Gentests zugänglicher geworden, eine umfassende Analyse der diagnostischen Ausbeute fehlt jedoch. Diese Übersicht gibt einen Überblick über die diagnostische Ausbeute von Gentests im gesamten Spektrum der Phänotypen von Nierenerkrankungen anhand einer systematischen Literatursuche, die 115 eingeschlossene Artikel ergab. Patienten-, Test- und Kohortenmerkmale, die den diagnostischen Ertrag beeinflussen können, werden hervorgehoben. Die Erkennung von Variationen der Kopienzahl und ihr Beitrag zur diagnostischen Ausbeute wird für alle Phänotypgruppen beschrieben. Auch die Auswirkungen einer genetischen Diagnose auf einen Patienten und Familienmitglieder, die diagnostisch sein können,therapeutisch, und prognostisch, wird durch die dargestelltenthaltene Artikel. Mithilfe dieser Überprüfung können Ärzte a priori die Wahrscheinlichkeit abschätzen, bei ihren Patienten eine genetische Ursache für eine Nierenerkrankung zu finden.
SCHLÜSSELWÖRTER:CHRONISCHE Nierenerkrankung, CNV,diagnostische Ausbeute, Gentests, MPS, Nephrogenese, Übersicht

KLICKEN SIE HIER, UM CISTANCHE ZUR CNI-BEHANDLUNG ZU KENNEN
1|EINFÜHRUNG
Genetische Nierenerkrankungenbilden eine heterogene Gruppe von Störungen, die zwar einzeln meist selten sind, aber zusammengenommen häufig und wichtig zu etablieren sind (Groopman et al., 2019). Die Identifizierung einer genetischen Ursache bei Patienten mit Nierenerkrankungen ist für Patienten und ihre Familienangehörigen von entscheidender Bedeutung. Für den Patienten kann eine genetische Diagnose zu Erkenntnissen über die Ätiologie, einer individuellen Behandlung und der Möglichkeit führen, über Prognose und Möglichkeiten der Familienplanung beraten zu werden. Familienmitglieder können über präsymptomatische Tests und Screening-Optionen beraten werden. Auch bei einer Lebendnierenspende kann eine genetische Diagnostik wichtig sein. Es können verschiedene Kategorien genetischer Nierenerkrankungen unterschieden werden (Hildebrandt, 2010). Ein wichtiges klinisches Erscheinungsbild ist die chronische Nierenerkrankung (CKD), die sich zu einer Nierenerkrankung im Endstadium (ESKD) entwickeln kann, die eine hohe Krankheitslast mit sich bringt (Coresh, 2017). Viele Ursachen können zu diesem letzten gemeinsamen Endpunkt führen (Groopman et al., 2019). Insgesamt können bei genetisch bedingten Nierenerkrankungen pathogene Varianten in mehreren Genen einen einzigen Phänotyp verursachen (genetische Heterogenität), und pathogene Varianten in einem bestimmten Gen können mehrere klinische Erscheinungsformen aufweisen (Pleiotropie) (Stokman et al., 2016).
Die Einführung des Massively Parallel Sequencing (MPS), früher als Next-Generation-Sequencing bezeichnet, hat Tests auf monogene Nierenerkrankungen (MKD) zugänglicher und damit die Diagnose von MKD einfacher gemacht. Dies hat zu vielen neuen Erkenntnissen geführt, es fehlt jedoch eine umfassende Analyse der diagnostischen Ausbeute über und innerhalb von Phänotypen. Die Schätzung des wahrscheinlichen diagnostischen Ertrags eines Gentests bei einem bestimmten Patienten ist wichtig, um die Wahrscheinlichkeit der Diagnose einer monogenen Erkrankung bei der Durchführung eines Gentests zu bestimmen. Dieser geschätzte Ertrag fließt zusammen mit Faktoren wie Kosten, Verfügbarkeit, aber auch spezifischen Bedürfnissen des Patienten und/oder der Eltern, beispielsweise im Hinblick auf Familienplanung oder lebensbezogene Nierenspende, in die gemeinsame Entscheidungsfindung in Bezug auf Gentests ein. Mehrere Studien berichten über unterschiedliche diagnostische Ergebnisse von Gentests für potenziell genetisch bedingte Phänotypen von Nierenerkrankungen. Die unterschiedlichen gemeldeten diagnostischen Ergebnisse könnten eine Folge von Unterschieden in (a) Patientenmerkmalen, (b) genetischen Testmerkmalen und/oder (c) Kohortenmerkmalen sein. Patientenfaktoren, die den diagnostischen Ertrag beeinflussen können, sind eine positive Familienanamnese, extrarenale Merkmale, ein syndromales Erscheinungsbild und eine schwere Erkrankung, einschließlich eines frühen Krankheitsausbruchs und des Vorhandenseins von ESKD (Knoers et al., 2022). Testmerkmale, die den gemeldeten Ertrag beeinflussen können, sind die Anzahl der analysierten Gene (maximal alle Gene [Exom] oder genomweit), ob Kopienzahlvariationen (CNVs) bewertet werden, ob zusätzliche Tests für schwierige Genomregionen durchgeführt werden ( B. MUC1 und Exon 1 von PKD1), sondern auch, ob Trioanalysen (Kind und beide Eltern getestet) und Segregation zur zusätzlichen Variantenklassifizierung durchgeführt werden. Auch die Besonderheiten der Kohorte können von Bedeutung sein. In einer klinischen Kohorte (aus aufeinanderfolgenden Fällen) sind die Phänotypen häufig weniger homogen und die Population ist möglicherweise repräsentativer für Patienten, die in der eigenen Klinik behandelt werden. In einer Forschungskohorte werden unterschiedliche Einschluss- und Ausschlusskriterien angewendet. Bei den Patienten handelt es sich häufig um aus vielen Zentren ausgewählte Fälle, bei denen der größte Verdacht auf eine genetische Diagnose besteht, und die Ergebnisse der diagnostischen Ausbeute sind nicht immer auf eine diagnostische Situation übertragbar. Eine weitere relevante Variable könnte die Kohortengröße sein.

In diesem Review wollen wir die diagnostische Ausbeute von Gentests innerhalb und über das gesamte Spektrum potenzieller genetischer Nierenerkrankungen-Phänotypen bestimmen. Patienten-, Test- und Kohortenmerkmale, die die verschiedenen Erträge beeinflussen, werden hervorgehoben. Wir bieten einen detaillierten und differenzierten Überblick, der dabei helfen kann, die Bedeutung der verschiedenen Veröffentlichungen abzuwägen, und potenziell nützliche Informationen für die klinische Praxis liefert. Wir beleuchten auch die klinischen Auswirkungen genetischer Diagnosen auf der Grundlage der gesammelten Studien und zeigen, wie sich genetische Testansätze im Laufe der Jahre entwickelt haben.
TABELLE 1 Die Sätze von Begriffen, die zur Durchführung der PubMed-Suche verwendet wurden. Die Sätze (1) und (2) wurden mit dem booleschen Operator „AND“ zu einer Suche kombiniert. Dasselbe wurde für die Sätze (1) und (3) durchgeführt Titel/Zusammenfassung
(1) Niere ODER Nieren ODER Alport ODER ADPKD ODER ARPKD ODER CAKUT ODER Ciliopathie ODER Nephronophthisis ODER Nephrol* ODER Nephron* ODER nephrogen ODER Glomeruli* ODER Urol* ODER Harntrakt ODER Tubulopathie* ODER nephrotisch
(2) Diagnostische Ausbeute ODER Ausbeute ODER Gentest ODER WES ODER WGS ODER Gesamt-Exom-Sequenzierung ODER Gesamt-Exom-Sequenzierung ODER Gesamt-Exom ODER Gesamt-Genom ODER Gesamt-Exom ODER Gesamt-Genom ODER Gen-Panel ODER Gen-Panels ODER Multigen-Panel ODER Multigen-Panels ODER Gesamtgenomsequenzierung ODER MPS ODER massive Parallelsequenzierung ODER massiv parallele Sequenzierung ODER NGS ODER Next-Generation-Sequenzierung ODER Next-Generation-Sequenzierung ODER exomische Sequenzierung ODER Genomsequenzierung ODER gezielte Gensequenz* ODER gezielte Sequenz* ODER gezieltes Panel*
(3) CNV ODER Kopienzahlvariante ODER Kopienzahlvariation ODER Kopienzahlvarianz ODER SNP-Array ODER SNP-Array ODER Array-CGH ODER Array-CGH
2|METHODEN
2.1|Studienauswahl
Zur Beantwortung der Übersichtsfrage wurde eine systematische Literaturrecherche durchgeführt: „Wie hoch ist die diagnostische Ausbeute von Gentests bei jeder Art von Nierenerkrankung und welche Patienten-, Kohorten- und Testmerkmale wirken sich auf die diagnostische Ausbeute aus?“ Diese Bewertung wurde nicht in einer Bewertungsdatenbank registriert. Die PubMed-Datenbank wurde am 2. April 2021 mit den in Tabelle 1 angezeigten Begriffen durchsucht. Zwei Rezensenten wählten unabhängig voneinander Artikel auf der Grundlage vorgegebener Einschlusskriterien unter Verwendung von Rayyan aus (Ouzzani, Hammady, Fedorowicz & Elmagarmid, 2016). Meinungsverschiedenheiten wurden im Konsens oder mit Hilfe eines dritten Gutachters gelöst.
Alle diese Einschlusskriterien waren obligatorisch: (a) Originalartikel, der in den letzten 10 Jahren veröffentlicht wurde, (b) menschliche Teilnehmer, (c) diagnostisches Ergebnis der Gentests gemeldet oder ableitbar, (d) Patienten hatten irgendeine Art von Nierenerkrankung und (z ) Kohorte von mindestens 30 unabhängigen Patienten. Artikel mit Schwerpunkt auf Nierenkrebs wurden ausgeschlossen. Weitere Artikel wurden durch Schneeballanalyse identifiziert und einbezogen.
2.2|Datenextraktion
Die Datenextraktion erfolgte mithilfe vordefinierter Datenfelder. Die Studien wurden in die folgenden Phänotypgruppen für Nierenerkrankungen eingeteilt: autosomal-dominante tubulointerstitielle Nierenerkrankung (ADTKD), angeborene Anomalien der Niere und des Harntrakts (CAKUT), Ziliopathien (unterteilt in autosomal-dominante polyzystische Nierenerkrankung [ADPKD] und andere/gemischte Ziliopathien) , Glomerulopathie (nephrotisches Syndrom [NS] und andere/gemischte), Nephrolithiasis/Urolithiasis, Tauopathien, ESKD und gemischte Phänotypen von Nierenerkrankungen. Zu allen Studien, Details.

wurden anhand von Patientenmerkmalen, Kohortenmerkmalen und dem durchgeführten Gentest extrahiert. Zu den Details der extrahierten Kohorte gehörten die Anzahl der eingeschlossenen Patienten, der Phänotyp und die Art der Kohorte (klinische Kohorte oder Forschungskohorte). Eine Kohorte wurde als klinische Kohorte betrachtet, wenn die Kohorte aus einem klar definierten klinischen Umfeld stammte (z. B. alle aufeinanderfolgenden Patienten, die eine Nierentransplantation erhielten) und/oder über genetische Testergebnisse aus einem diagnostischen Umfeld berichtete (z. B. alle Patienten, die wegen Genüberweisung überwiesen wurden). Panel-Tests). Zu den extrahierten Patientenmerkmalen gehörten: der Prozentsatz familiärer Fälle, der Prozentsatz der Blutsverwandtschaft, der Prozentsatz der Fälle mit extrarenalen Merkmalen, das Alter bei Krankheitsbeginn und der Prozentsatz der Personen mit ESKD. Zu den extrahierten Details für den Gentest gehörten: die Anzahl der untersuchten Gene und ob eine Einzelnukleotidvarianten- (SNV) und/oder CNV-Analyse durchgeführt wurde. Es wurde davon ausgegangen, dass eine CNV-Analyse durchgeführt wurde, auch wenn nur ein Gen untersucht wurde. CNVs wurden hier als Deletionen oder Duplikationen definiert, die zu groß sind, um durch herkömmliche Sequenzierung erfasst zu werden. Art des Gentests (z. B. MPS-basiertes Multigen-Panel, Single Nucleotide Polymorphism [SNP]-Array, Whole Exome Sequencing [WES], Whole Genome Sequencing [WGS] usw.), einschließlich der Art der CNV-Analyse, wurden extrahiert. Die diagnostische Ausbeute wurde entweder aus der Arbeit übernommen oder aus den Daten berechnet. Wahrscheinliche pathogene Varianten und pathogene Varianten wurden in die diagnostische Ausbeute einbezogen, es sei denn, die Autoren machten keine Angaben zur Variantenklassifizierung. In diesem Fall wurde der von den Autoren angegebene Ertrag extrahiert. Wenn Autoren einen abweichenden Begriff zur Beschreibung von Varianten verwendeten (dh einen anderen Begriff als [wahrscheinlich] pathogen, z. B. „wahrscheinlich krankheitserregend“ oder „potenziell pathogen“), wurden dieser Begriff und der zugehörige Ertrag extrahiert. Es wurden auch die Kriterien angegeben, die zur Bewertung der Varianten in jedem Artikel verwendet wurden. Kandidatengene wurden nicht in die diagnostische Ausbeute einbezogen, sondern unter „bemerkenswert“ hervorgehoben. Der diagnostische Ertrag wurde pro Phänotyp in Kohorten mit gemischten Phänotypen berechnet und notiert. Wenn Details zu der Kohorte verfügbar waren, aus der die getestete Population stammte, wurde auch ein diagnostischer Ertrag berechnet, der auf die größere Kohorte extrapoliert wurde (z. B. wenn eine bestimmte Untergruppe von Transplantationspatienten genetisch getestet wurde, wurde der diagnostische Ertrag auf die gesamte Kohorte extrapoliert). Kohorte transplantierter Patienten). Sofern gemeldet, wurde der Prozentsatz der Fälle mit einer Variante unbekannter Bedeutung extrahiert. Wir haben die Ausbeute auch ausschließlich auf der Grundlage von CNVs berechnet und ermittelt, wie viel Prozent der gemeldeten diagnostischen Ausbeute durch CNVs erklärt werden kann. Wenn in der Studie ein Patientenmerkmal gemeldet wurde, das sich positiv auf die diagnostische Ausbeute auswirkte, wurde dies vermerkt. Alle weiteren relevanten Details wurden ebenfalls extrahiert. Schließlich ermittelten wir die Anzahl der Gene, die für die oberen 50 % der diagnostischen Ausbeute verantwortlich waren. Die verantwortlichen Gene wurden notiert, es sei denn, die Gene waren nur für einen positiven Fall verantwortlich und/oder mehrere Gene machten die endgültigen Prozentsätze aus.
2.3|Datenvisualisierung
Die Daten wurden zusammengefasst, indem die Kohorten-, Patienten- und Testmerkmale sowie die Ergebnisse zum diagnostischen Ertrag pro Phänotypgruppe in einer Übersichtstabelle zusammengefasst wurden. Detailliertere Übersichten aller Studien wurden in separaten Tabellen pro Krankheitsgruppe zusammengefasst. Wir haben uns zunächst die Patientenmerkmale angesehen, die sich innerhalb einer einzelnen Studie positiv auf die Diagnoseausbeute auswirken, und dies in der Übersichtstabelle beschrieben. Als nächstes bewerteten wir die Auswirkungen von Patienten-, Kohorten- und Testmerkmalen zwischen den verschiedenen Studien. Um den Einfluss dieser Merkmale zu visualisieren, wurden Streudiagramme, Boxdiagramme und Kreisdiagramme mit SPSS (Version 26, IBM, New York, NY) erstellt, um die Beziehung zwischen zwei quantitativen Variablen innerhalb einer einzelnen Studie über alle Studien hinweg zu untersuchen. Um eine Überinterpretation der aus den sehr variablen Studien abgeleiteten Daten zu vermeiden, haben wir uns entschieden, nur eine visuelle Darstellung der Daten darzustellen und keine statistischen Tests durchzuführen.
3|ERGEBNISSE
Die PubMed-Suche ergab 5.361 Artikel. Nach Sichtung von Titel, Zusammenfassung und Volltext blieben 98 Beiträge übrig, die die Einschlusskriterien erfüllten. Siebzehn Artikel wurden zusätzlich durch Schneeballanalyse identifiziert und einbezogen.
Tabelle 2 gibt einen Überblick über die gemeldeten Erträge pro Krankheitsgruppe. Pro Krankheitsgruppe wurden 4 bis 25 Artikel mit unterschiedlichen Patienten-, Test- und Kohortenmerkmalen pro Studie eingeschlossen. Die diagnostischen Ergebnisse unterschieden sich stark innerhalb jeder Krankheitsgruppe und zwischen den verschiedenen Krankheitsgruppen (Tabelle 2; Abbildung 1a). Wir finden die niedrigste diagnostische Ausbeute in der CAKUT-Krankheitsgruppe und die höchste diagnostische Ausbeute in der Ciliopathie-Gruppe und innerhalb dieser Gruppe eine sogar noch höhere Ausbeute für die ADPKD-Gruppe. Allerdings fanden wir in der CAKUT-Erkrankungsgruppe die höchste diagnostische Ausbeute, die ausschließlich auf CNVs beruhte (Abbildung 1b). Wenn wir die auf die größere Kohorte hochgerechnete Rendite betrachten, stellen wir erwartungsgemäß häufig eine niedrigere Rendite fest als ursprünglich angegeben (Tabelle 2). Diese Werte stellen eine minimale diagnostische Ausbeute für die Ursprungspopulation dar.
In der Ergänzungstabelle 1 werden die Krankheitsgruppen detaillierter dargestellt. Patienten-, Kohorten- und Testmerkmale, einschließlich bemerkenswerter Details, werden für jede einzelne Studie beschrieben. Sofern verfügbar, sind der diagnostische Ertrag pro Phänotyp (insbesondere in der Ergänzungstabelle 1h, der Phänotypen gemischter Nierenerkrankungen abdeckt) und der auf eine größere Ursprungspopulation extrapolierte diagnostische Ertrag enthalten.
Fünf Studien berichteten über eine ESKD-Population, die auf der Warteliste für eine Transplantation stand oder eine Nierentransplantation erhalten hatte (Ergänzungstabelle 1g). Die diagnostische Ausbeute in diesen Studien reichte von 0,5 % (nur vollständige Gendeletionen in 20 untersuchten Genen) bis 50,9 % bei den genetisch getesteten Patienten zum Zeitpunkt der Studie. Bei der Extrapolation auf die einzelnen extrapolierten Kohorten von Nierentransplantationspatienten (Warteliste) lag die Ausbeute zwischen 12,5 und 24,6 %.

Zehn Studien aus unterschiedlichen Krankheitsgruppen berichteten über Nierenerkrankungen unbekannter Ursache (Patienten, bei denen der klinische Phänotyp nicht auf eine bestimmte Diagnose hinweist). Die Phänotypgruppen umfassen die Phänotypen ADTKD (1), ESKD (3) und gemischte Nierenerkrankungen (6). Die diagnostische Ausbeute in einer Population von Patienten mit familiärer Nephropathie unbekannter Ursache, die auf ADTKD untersucht wurden, betrug 29,5 %. In Studien zur Untersuchung von ESKD ungeklärter Ätiologie lag die diagnostische Ausbeute zwischen 11,6 und 44,4 %. In den sechs Studien mit gemischten Nierenerkrankungen-Phänotypen lag die Ausbeute bei Patienten mit Nephropathie unbekannter Ursache über fünf Studien hinweg zwischen 17,1 und 56,3 %, und eine Studie berichtete über eine Ausbeute von 0 % (nur fünf Patienten hatten eine Nephropathie unbekannter Ursache). eine Kohorte von 204 Patienten). Tabelle 3 gibt einen Überblick über die klinischen Auswirkungen genetischer Diagnosen, die in den verschiedenen Studien hervorgehoben wurden, unterteilt in diagnostische Auswirkungen, therapeutische Auswirkungen und prognostische Auswirkungen.
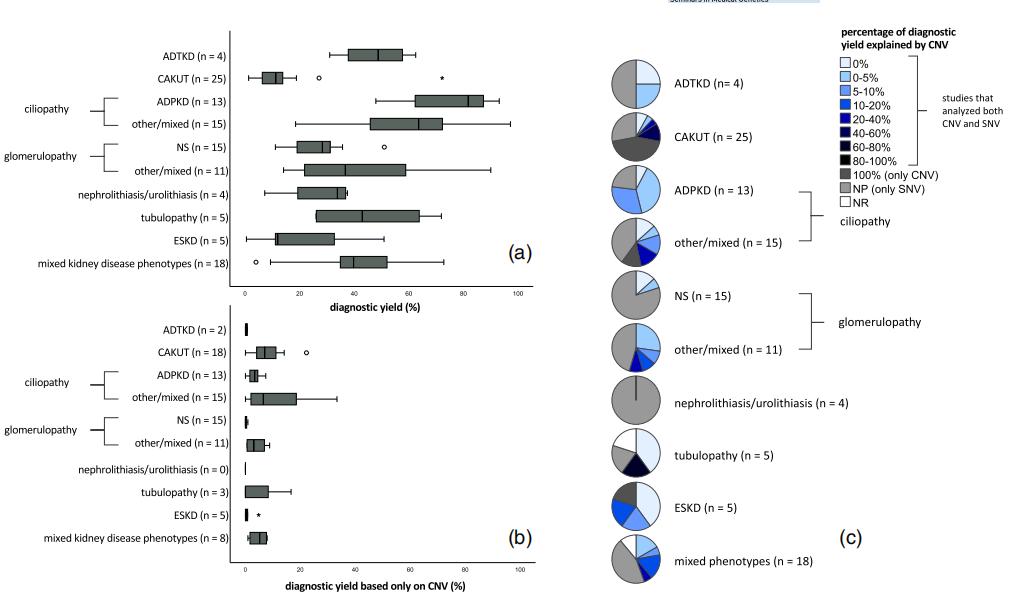
ABBILDUNG 1 Diagnoseausbeute über Krankheitskategorien hinweg. (a) Diagnoseausbeute pro Krankheitskategorie. Die Unterteilung der spezifischen Phänotypen innerhalb der Gruppe „gemischte Nierenerkrankungen-Phänotypen“ wird nicht zu den entsprechenden separaten Krankheitsgruppen addiert, da in den Studien dieser Gruppe keine Patienten-/Test-/Kohortenmerkmale pro Phänotyp verfügbar sind. In Klammern steht die Anzahl der eingeschlossenen Studien. (b) Die diagnostische Ausbeute basiert nur auf der Erkennung der Kopienzahlvariation (CNV). In Klammern steht die Anzahl der Studien, die eine CNV-Analyse durchgeführt haben. (c) Prozentsatz der gesamten diagnostischen Ausbeute (a), erklärt durch CNVs (b). In Klammern steht die Gesamtzahl der Studien. Dies ist ein Verhältnis zwischen den Teilpanels (b) und (a), das zeigt, wie viel CNV-Tests zum diagnostischen Ertrag pro Studie beitrugen
3.1|Merkmale, die den diagnostischen Ertrag beeinflussen
3.1.1|Patienteneigenschaften
Bei der Betrachtung von Patientenmerkmalen, die die diagnostische Ausbeute innerhalb einer bestimmten Studie beeinflussen, stellen wir fest, dass mehrere Studien einen positiven Einfluss auf die diagnostische Ausbeute berichteten, basierend auf einer positiven Familienanamnese (n=18-Studien), Blutsverwandtschaft (n=12) und extrarenaler Verwandtschaft Merkmale (n=16), früher Krankheitsausbruch (n=14) und ESKD (n=8), wie in Tabelle 2 und Ergänzungstabelle 1 beschrieben. Einige zusätzliche Merkmale werden ebenfalls erwähnt , wie spezifische Phänotypen, geringere Rezidive nach der Transplantation und fehlende Reaktion auf Immunsuppressiva für den steroidresistenten NS (SRNS)-Phänotyp (Tabelle 2).
Wenn wir dieselben Variablen (Familienanamnese, extrarenale Merkmale, früher Krankheitsausbruch und ESKD) zwischen den Studien bewerten, sehen wir deutlich, dass in Kohorten mit einem hohen Prozentsatz familiärer Fälle und in Kohorten mit einem hohen Prozentsatz extrarenaler Fälle die Diagnose Die Ausbeute ist höher (Abbildung 2a,b). Allerdings sehen wir dieses klare Muster nicht in Kohorten mit einem hohen Prozentsatz an Blutsverwandtschaft oder einem hohen Prozentsatz an ESKD (Abbildung 2c,d). Wenn wir Kohorten mit einem hohen Prozentsatz an Fällen im Erwachsenenalter betrachten, finden wir sowohl niedrige als auch hohe Prozentsätze der diagnostischen Ausbeute (Abbildung 2e). In den Kohorten, in denen es keine (0 %) Fälle mit Beginn im Erwachsenenalter gibt, sehen wir dasselbe, wobei ein großer Teil der Studien mit geringer Ausbeute durch die CAKUT-Gruppe erklärt wird. Die Bedeutung der CNV-Analyse wird in Abbildung 2f hervorgehoben, wo eine hohe diagnostische Ausbeute bei Erkrankungen im Kindesalter im Vergleich zu Erkrankungen im Erwachsenenalter festgestellt wird.
3.1.2|Kohortenmerkmale
In Abbildung 3a zeigen wir die Anzahl der getesteten Patienten in einer Kohorte im Verhältnis zur diagnostischen Ausbeute. Wir stellen fest, dass die diagnostische Ausbeute in größeren Kohorten abnimmt. Wenn wir die Boxplots vergleichen, die den diagnostischen Ertrag in klinischen Kohorten mit Forschungskohorten darstellen, scheint kein klarer Unterschied vorhanden zu sein (Abbildung 3b). Wir verwendeten die diagnostische Ausbeute in der getesteten klinischen Kohorte und nicht in der extrapolierten Kohorte, da für die extrapolierte Kohorte nicht immer Daten verfügbar waren.
3.1.3|Testmerkmale Abbildung 4 stellt die Testmerkmale zwischen den Studien dar. Es scheint, dass die diagnostische Ausbeute umso geringer ist, je höher die Anzahl der analysierten Gene ist (Abbildung 4a). Als wir Sequenzierungsansätze mit der diagnostischen Ausbeute in Beziehung setzten, stellten wir fest, dass das Testen eines einzelnen Gens eine geringere diagnostische Ausbeute hatte als wenn mehrere Gene (2–10) getestet wurden, und wir fanden das Gleiche auch bei kleinen Genpanels (<100) versus large gene panels (Supplementary Figure 1). However, the categories WES/WGS and SNP-array had a lower yield than the previously mentioned categories. 47/115 studies assessed SNVs, 12/115 assessed only CNVs and 55/115 assessed both (Figure 4b). As shown in Figure 4c, we found that the diagnostic yield was highest in cohorts where both SNVs and CNVs were assessed, and lowest in cohorts that only assessed CNVs. We saw that over the years there has been a shift from focusing either on SNVs or CNVs to including both in genetic testing (Supplementary Figure 2). There has also been a shift from enrichment-based panels to an exome-based approach. Noticeably in CNV testing, there is a shift toward the use of MPS-based CNV-calling.
3.1.4|CNV-Analyse
CNVs wurden am häufigsten in den Krankheitsgruppen CAKUT, Ciliopathie, Tauopathien, ESKD und gemischten Nierenerkrankungsphänotypen beurteilt. Bei Nephrolithiasis/Urolithiasis wurden die CNVs nie beurteilt. Die ausschließlich auf CNV-Tests basierende diagnostische Ausbeute war bei CAKUT-Patienten am höchsten, gefolgt von der Krankheitsgruppe mit gemischten Phänotypen und Ziliopathien. Der Beitrag von CNVs zur diagnostischen Ausbeute war auch in den CAKUT- und Ciliopathie-Gruppen am höchsten. Als Studien sowohl CNVs als auch SNVs untersuchten, fanden wir den höchsten Prozentsatz an CNVs bei CAKUT und Tauopathien (Abbildung 1c). HNF1B-Deletionen, die eine Gitelman-Tubulopathie (wie) verursachten, erklärten den hohen Prozentsatz an CNVs in letzterer. Es wurden verschiedene CNV-Testansätze verwendet, wobei die höchste Ausbeute durch Einzelgentests und Array-basierte CNV-Tests erzielt wurde (ergänzende Abbildung 3).
3.2|Kerngene
In allen eingeschlossenen Studien war eine begrenzte Anzahl von Genen für einen großen Prozentsatz der erklärten Fälle verantwortlich, wie in Abbildung 5 dargestellt. Wir fanden heraus, dass maximal 10 Gene für mindestens 50 % der gelösten Fälle verantwortlich waren, oft nur eins bis vier Gene verantwortlich. In den Phänotypgruppen ADTKD und APDKD war in einer einzigen Studie nur ein Gen (UMOD bzw. MUC1 und PKD1) für 50 % des gemeldeten Ertrags verantwortlich. Aber auch in den Phänotypgruppen mit unterschiedlichen Phänotypen der Nierenerkrankung stellten wir fest, dass Varianten in maximal 10 Genen 50 % der diagnostischen Ausbeute ausmachten. Die Gene, die für den Spitzenertrag von 50 % verantwortlich sind, werden in Panel (b) angezeigt. Einzelheiten zu den einzelnen Studien finden Sie in der Ergänzungstabelle 3.
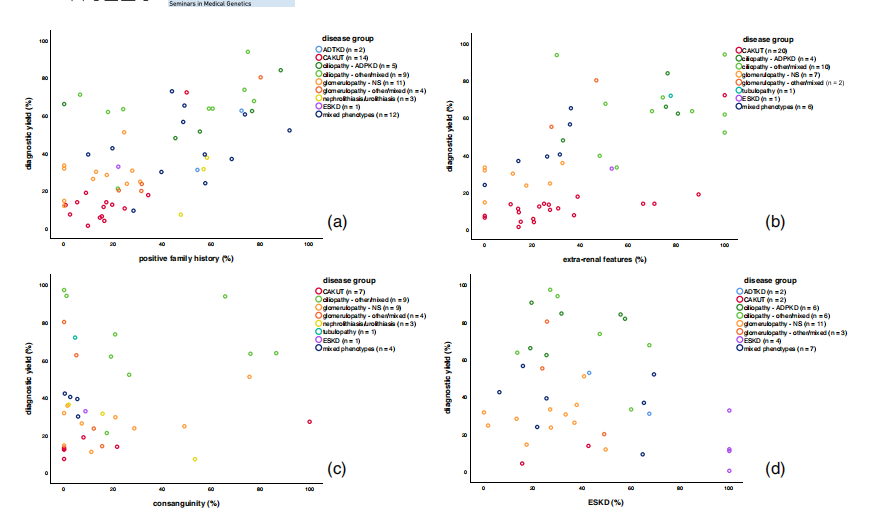
ABBILDUNG 2 Streudiagramme, die die Beziehung zwischen diagnostischem Ertrag und Patienteneigenschaften zeigen. Die Legende beschreibt eine Reihe von Studien, für die Daten zu diesem spezifischen Patientenmerkmal verfügbar waren. Farben geben die Krankheitsgruppe an, aus der die Studie stammt. Jeder Punkt repräsentiert für eine Studie den Prozentsatz eines bestimmten Merkmals in dieser Kohorte und welche diagnostische Ausbeute aus derselben Studie erzielt wurde. (a) Prozentsatz der Fälle mit positiver Familienanamnese im Verhältnis zur diagnostischen Ausbeute. (b) Prozentsatz der Fälle mit extrarenalen Merkmalen im Verhältnis zur diagnostischen Ausbeute. (c) Prozentsatz der Fälle aus einer blutsverwandten Familie im Verhältnis zum diagnostischen Ergebnis. (d) Prozentsatz der Fälle mit terminaler Niereninsuffizienz (ESKD) im Verhältnis zum diagnostischen Ergebnis. (e) Prozentsatz der Fälle mit Krankheitsbeginn im Erwachsenenalter im Verhältnis zum diagnostischen Ergebnis. (f) Prozentsatz der Fälle mit Krankheitsausbruch im Erwachsenenalter im Verhältnis zur diagnostischen Ausbeute, nur basierend auf Kopienzahlvariationen (CNVs).
Unterstützender Service:
E-Mail:wallence.suen@wecistanche.com
WhatsApp/Tel:+86 15292862950
Geschäft:
https://www.xjcistanche.com/cistanche-shop






