Auswahl und Charakterisierung von Tyrosinase-Inhibitoren aus Atractylodis macrocephalae Rhizoma basierend auf Spektrum-Aktivitäts-Beziehung und molekularem Docking
Mar 30, 2023
Copyright © 2021 Yong-Qin Liu et al. 2is ist ein Open-Access-Artikel, der unter der Creative Commons Attribution License vertrieben wird, die die uneingeschränkte Nutzung, Verbreitung und Vervielfältigung in jedem Medium erlaubt, vorausgesetzt, das Originalwerk wird ordnungsgemäß zitiert.
Cistanchehat die Funktion, die Kollagenproduktion zu fördern, was die Elastizität und den Glanz der Haut erhöhen und helfen kann, beschädigte Hautzellen zu reparieren.CistanchePhenylethanol-Glykoside haben eine signifikant herunterregulierende Wirkung auf die Tyrosinase-Aktivität, und die Wirkung auf die Tyrosinase ist nachweislich eine kompetitive und reversible Hemmung, die eine wissenschaftliche Grundlage für die Entwicklung und Verwendung der aufhellenden Inhaltsstoffe in Cistanche liefern kann. Daher spielt Cistanche eine Schlüsselrolle bei der Hautaufhellung. Es kanndie Melaninproduktion hemmenVerfärbung und Mattheit zu reduzieren; und fördern die Kollagenproduktion, um die Elastizität und Ausstrahlung der Haut zu verbessern. Aufgrund der weit verbreiteten Anerkennung dieser Wirkungen von Cistanche haben viele Hautaufhellungsprodukte damit begonnen, pflanzliche Inhaltsstoffe wie Cistanche zu infundieren, um die Nachfrage der Verbraucher zu befriedigen, wodurch der kommerzielle Wert von Cistanche erhöht wirdHautaufhellungProdukte. Zusammenfassend ist die Rolle von Cistanche bei der Hautaufhellung entscheidend. Seine antioxidative Wirkung und kollagenbildende Wirkung kann Verfärbungen und Mattheit reduzieren,verbessern die Elastizität und den Glanz der Haut, und erzielen so einen Whitening-Effekt. Auch die breite Anwendung von Cistanche in Hautaufhellungsprodukten zeigt, dass seine Rolle im kommerziellen Wert nicht unterschätzt werden darf.

Klicken Sie auf Organic Cistanche zum Aufhellen
Fragen Sie nach mehr: david.deng@wecistanche.com WhatApp:86 13632399501
Atractylodis macrocephalus Rhizoma (AMR) ist eine berühmte klassische chinesische traditionelle Medizin (CTM), die seit Tausenden von Jahren als Tonikum für viele Krankheiten verwendet wird. Im alten China wurde es als ergänzendes Nahrungsmittel für die Schönheit im Palast verwendet. In vorläufigen Studien wurden die Funktion der Hautaufhellung und die signifikante Hemmwirkung auf Tyrosinase (TYR), das reaktive Enzym in der Zusammensetzung von Melanin von AMR, entdeckt, und die entsprechende Forschung wurde selten berichtet. In dieser Studie wurde Hochleistungsflüssigkeitschromatographie (HPLC) zusammen mit partieller Regressionsanalyse der kleinsten Quadrate (PLS) angewendet, um die Kohärenz zwischen den chemischen Bestandteilen und der hemmenden Aktivität von 11 Chargen von AMR auf die TYR-Aktivität zu untersuchen. Die Ergebnisse von PLS zeigten, dass die chromatographischen Peaks 11 (Atractylenolid III) und 15 wichtige wirksame Inhaltsstoffe für die Hemmung der TYR-Aktivität sein könnten, wie durch Spektrum-Aktivitäts-Beziehungen festgestellt wurde. Darüber hinaus wurde die TYR-Hemmaktivität von Atractylenolid III durch einen In-vitro-Test validiert, indem -Arbutin als positives Kontrollarzneimittel diente.DerDie Ergebnisse des In-vitro-Tests und des Molecular Docking zeigten, dass Atractylenolid III eine hohe TYR-Inhibitoraktivität aufweist und an die Reste in der katalytischen TYR-Tasche binden könnte.DerDaher sind Bioassay, molekulares Docking und Spektrum-Aktivitäts-Beziehungen geeignet, um die Qualität von Proben mit pharmazeutisch relevanten Wirkstoffen zu verknüpfen. Und unsere Studie würde eine theoretische Grundlage für die Anwendung der Wasserextrakte von AMR in aufhellenden Kosmetika legen.
1. Einleitung
Tyrosinase (TYR), auch als Polyphenoloxidase bezeichnet, ist ein polyfunktionelles glykosyliertes kupferhaltiges Enzym, das im Organismus von Tieren, Pflanzen und Mikroorganismen weit verbreitet ist [1–3]. In Gegenwart von molekularem Sauerstoff wird Tyrosin zuerst durch TYR katalysiert, um zu Dopa zu oxidieren, und dann weiter zu Dopachinon oxidiert, das isomerisiert, um Dopa-Pigment zu bilden. Dopa-Pigment bildete schließlich Melanin unter Beteiligung von CO2 und TRP-2, die verschiedene Hauterkrankungen wie Hyperpigmentierung, Melasma, Sommersprossen und Altersflecken verursachen [4, 5]. TYR spielt eine wichtige Rolle, da es das kritische Enzym und Restriktionsenzym im Verlauf der Melaninzusammensetzung ist [6–8]. Pigmentflecken und Melanome nahmen durch zunehmende TYR-Aktivität und -Menge deutlich zu [9]. Heutzutage haben TYR-Hemmer aufgrund ihrer latenten Verwendung als hypopigmentierte Mittel breite Aufmerksamkeit erfahren [10].
Atractylodis macrocephalus rhizoma (AMR), das trockene Rhizoma von Atractylodes macrocephalaKoidz., ist eines der chinesischen Kräuterarzneimittel, das im Chinesischen Arzneibuch zusammengestellt ist [11–15]. Im alten China wurde AMR ausgewählt, um die berühmte klassische Formel zum Aufhellen mit der Bezeichnung „Sieben-Weiße-Salbe“ zu bilden und als zusätzliche Nahrung für die Schönheit im Palast verwendet zu werden [16]. Es wurde berichtet, dass AMR hauptsächlich Sesquiterpenoide und Triterpenoide (einschließlich Atractylenolid I, Atractylenolid II und Atractylenolid III), Polyacetylene, Cumarine und Phenylpropanoide, Flavonoide und Flflavonoidglykoside, Polysaccharide, Steroide, Benzochinone und andere Bestandteile enthielt [17, 18]. Allerdings wurde selten über seine Auswirkungen auf die Aufhellung der Haut und die Wirkstoffe berichtet.DerDie Untersuchung der Spektrum-Aktivitäts-Beziehung wurde angewendet, um ihre Relevanz zu untersuchen.
Die Erforschung der Spektrum-Aktivitäts-Beziehung kann nicht nur das Defizit der Trennung zwischen chemischen Inhaltsstoffen und Pharmakodynamik umgehen, sondern durch das mathematische Modell auch Fingerprints ausreichend mit Pharmakodynamik assoziieren [19, 20].ThDie Spektrum-Aktivitäts-Beziehung untersucht die Relevanz zwischen dem Fingerabdruck und der Pharmakodynamik, um eine glaubwürdige Methode zur Klärung der materiellen Basis der chinesischen Kräutermedizin anzubieten [21].DerFingerabdrücke wurden normalerweise durch HPLC, UPLC, GC, GC-MS und LC-MS erstellt [19, 22–24]. „Pharmakodynamische“ Daten werden von den Modellen üblicherweise erfasst [25].DerMethoden der Datenverarbeitung umfassen hauptsächlich Hauptkomponentenanalyse (PCA), partielle Regressionsanalyse der kleinsten Quadrate (PLS), orthogonale partielle kleinste Quadrate-Diskriminanzanalyse (OPLS-DA), kanonische Korrelationsanalyse (CCA) und graue relationale Analyse (GRA) meist [26–29].

Um die Komponenten des AMR zu klären, die zur Hemmaktivität von TYR beitragen [30, 31], wurden die Fingerabdrücke von 11 Chargen von AMR durch HPLC erstellt; die Pharmakodynamik der TYR-Inhibitionsaktivität in vitro wurde durch das biochemische enzymatische Verfahren bewertet. 2e wirksame Verbindungen wurden durch das Spektrum-Aktivitäts-Beziehungsmodell ausgewählt, das durch Korrelieren von Fingerprint-Peaks mit pharmakodynamischen Daten erstellt wurde. Darüber hinaus würden Wirkstoffe durch In-vitro-Tests und molekulare Docking-Experimente validiert. 2diese Studie könnte eine theoretische Grundlage für die Anwendung von AMR als Behandlungsmedizin für pigmentierte Hautkrankheiten und die Entwicklung als ergänzende Aufhellungskosmetik schaffen.
2. Materialien und Methoden
2.1. Chemikalien und Materialien.Methanol (mehr als oder gleich 99,5 Prozent) wurde von Sinopharm Chemical Reagent Co., Ltd. (Shanghai, China) gekauft. Phosphorsäure (mehr als oder gleich 99 Prozent) wurde von Chengdu Jinshan Chemical Reagent Co., Ltd. (Chengdu, China) bezogen. Acetonitril wurde von Tiandi Reagent Co., Ltd. (USA) gekauft. Atractylodes III (mehr als oder gleich 98 Prozent), Phosphatpuffer, Tyrosinase und L-Tyrosin wurden von Beijing Soleibao Technology Co., Ltd. (Peking, China) gekauft. -Arbutin (größer oder gleich 99,7 Prozent) wurde von der China Academy of Food and Drug Identification erworben. Tyrosinase und L-Tyrosin wurden vor der Verwendung in Phosphatpuffer (pH 6,8) gelöst. Atractylosen III und -Arbutin wurden in 50 Prozent Methanol (v/v) gelöst.Derreines Wasser wurde von Hangzhou Wahaha Baili Food Co., Ltd., (Hangzhou, China) bezogen. Die Comix C18-Säule (250 × 4,6 mm, 5 μm) wurde von Guangzhou Philemon Scientific Instrument Co., Ltd. (Guangzhou, China) gekauft.
2.2. Pflanzenmaterialien.DerEs wurden 11 Chargen von AMR-Arzneimittelproben gesammelt und sind in Tabelle 1 aufgeführt.DerDie obigen Proben wurden von Professor Ronggui Qin (School of Pharmacy, Guizhou Medical University) authentifiziert.
2.3. Extraktion.Kräuterstücke jeder Probe (etwa 10 g) wurden genau gewogen und dann in einen Rundkolben gegeben, Wasser zugegeben und zum Extrahieren unter Rückfluss erhitzt. Die Produkte wurden unter reduziertem Druck getrocknet, um den Wasserextrakt von AMR zu erhalten. 2en wurden die Wasserextrakte von AMR (ca. 30,00 mg) genau gewogen und mit 50 Prozent Methanol (v/v) gelöst.
2.4. HPLC-Analyse.Comix C18-Umkehrphasen-Chromatographiesäule (250 × 4,6 mm, 5 μm).Dermobile Phase 0.1 Prozent Phosphor war eine Mischung aus saurem Wasser (A)-Acetonitril (B); das Elutionssystem ist ausgelegt und in Tabelle 2 aufgeführt.DerDie folgende Rate wurde auf 0,6 ml/min festgelegt. Die Temperatur der 2e-Säule betrug 30 Grad.DerDie UA-Wellenlänge betrug 210 nm.DerDas Injektionsvolumen betrug 30 μl.
Das Nachweisverfahren wurde durch einen Präzisionstest, Wiederholbarkeitstest und Stabilitätstest verifiziert.
2.5. Chemometrische Analyse.In dieser Studie wurden die gemeinsamen Spitzeninformationen von Fingerabdrücken von 11 Chargen von AMR in die Software SIMCA14.1 für HCA, PCA und OPLS-DA importiert.
2.6. TYR-Inhibitionstest in vitro. DerExtrakte von AMR wurden mit Phosphatpuffer (pH 6,8) gelöst, bei 4 Grad gelagert und dann für den Assay des Enzyms verwendet.
In dieser Studie wurde L-Tyrosin als Substrat verwendet, um die Hemmung der TYR-Aktivität zu bestimmen.DerReaktionslösungen wurden gemäß Tabelle 3 hergestellt, und die Hemmrate von AMR auf TYR-Aktivität wurde bestimmt. Zunächst wurden die Reaktionslösungen für 10 min in ein 37 Grad Wasserbad gestellt. Zweitens wurde die TYR-Lösung sofort zu den T2- und T4-Reaktionslösungen gegeben. Zweitens reagierten die Reaktionslösungen bei einer konstanten Wasserbadtemperatur von 37 Grad für 10 min, nachdem sie vollständig gemischt worden waren. Abschließend wurden von den Reaktionslösungen sofort die Extinktionswerte bei 475 nm gemessen. Die Hemmraten (Prozent) wurden aus der folgenden Gleichung erhalten: Hemmrate (Prozent) =[(AT2− AT1) − (AT4 − AT3)]/(AT2− AT1) × 100 Prozent.

2.7. Spektrum-Aktivitäts-Beziehungsanalyse. DerDie Software „Chinese Traditional Medicine Chromatographic Fingerprint Similarity Evaluation System 2012 A Edition“ wurde verwendet, um die Retentionszeiten jedes Peaks einzustellen, und die Peakfläche (PA) wurde durch Ausgleich verarbeitet.Dern wurden die quantitativen Daten erhalten.DerDie PLS-Regressionsgleichung wurde mit der Software SIMCA14.1 erstellt; die Peakfläche wurde als unabhängige Variable (X) genommen und die TYR-Inhibitionsrate wurde als abhängige Variable (Y) gesetzt.


2.8. Hemmende Wirkung von Atractylodes III auf TYR und molekulares Docking.Um die inhibitorische Wirkung von Atractylenolid III auf TYR zu belegen, wurden enzymatische In-vitro-Aktivitätstests mit -Arbutin durchgeführt, das als positives Kontrollarzneimittel diente.
Das Programm AutoDock4.2 wurde in Andocksimulationen eingesetzt. Die Kristallstruktur von Agaricus bisporus (PDB ID: 2Y9X) wurde als 3D-Struktur von TYR genommen [32]. Wir haben Simulationen des Andockens von TYR an Atractylodes III durchgeführt. Zum Andocken an AutoDock Vina wurde die Rastergröße auf (x, y, z) =(16, 12, 14) und die Rastermitte auf (x, y, z) { {10}} (–10,348, –28,279, –45,925). In jedem Simulationsverfahren arbeitet der Fortschritt mit Standardparametern von AutoGrid und AutoDock. Der genetische Algorithmus von Lamarck (LGA) wurde übernommen, um die am besten geeigneten Ligandenbindungsorientierungen zu ermitteln.
3. Ergebnisse und Diskussion
3.1. Methodenvalidierung.Präzision, Wiederholbarkeit und Stabilität wurden für die Analysemethode validiert. Bei Präzisionstests überstieg die Präzision der relativen Retentionszeiten (RRTs) und relativen Peakflächen (RPAs) nicht {{0}}.02 Prozent bzw. 4 Prozent in RSD; die Ähnlichkeit war 1. Die Wiederholbarkeit von RRTs und RPAs war kleiner als 0,11 Prozent und 4 Prozent in RSD, und die Ähnlichkeit war größer als oder gleich 0,998. Die Stabilität wurde abgeschätzt, indem eine bei Laborumgebungstemperatur aufbewahrte Probenlösung nach 0, 6, 8, 12 und 18 h getestet wurde. Die RSDs von RRTs und RPAs der gemeinsamen Peaks waren kleiner als 0,1 Prozent bzw. 4 Prozent; die Ähnlichkeit war mehr als 0,999.DerDiese Ergebnisse legten nahe, dass das AMR-Experimentalsystem für die Fingerabdruckanalyse stabil und zuverlässig ist.
3.2. HPLC-Fingerabdruck-Etablierung und Ähnlichkeitsanalyse.Der Fingerabdruck von Atractylodes III-Referenzsubstanzen ist in Abbildung 1(a) dargestellt. Die AMR-Probe zeigte eine günstige Segregation zwischen ihren Peaks (Abbildung 1(b)). Unter perfekten Bedingungen wurden die HPLC-Fingerabdrücke der 11 verschiedenen Chargen von AMR-Proben erstellt (Abbildung 1(c)) und die Ähnlichkeiten berechnet. Die Ergebnisse der Ähnlichkeiten sind in Tabelle 4 gezeigt, die zeigte, dass alle Ähnlichkeitswerte der 11 Proben größer als 0,8 waren, was darauf hinweist, dass alle Proben ähnlich in der Art der chemischen Zusammensetzung waren. Sechzehn gemeinsame Peaks wurden durch Vergleich ihrer Retentionszeit des UV-Spektrums beobachtet. Peak 11 wurde durch Referenzsubstanzen als Atractylodes III identifiziert. Die RSDs von PAs von 16 gemeinsamen Peaks lagen zwischen 1,18 Prozent und 58,68 Prozent (Tabelle 5). Diese Ergebnisse zeigten, dass die Gehalte der chemischen Substanzen in AMR aus verschiedenen Produktionsbereichen unterschiedlich waren.
3.3. Chemometrische Analyse
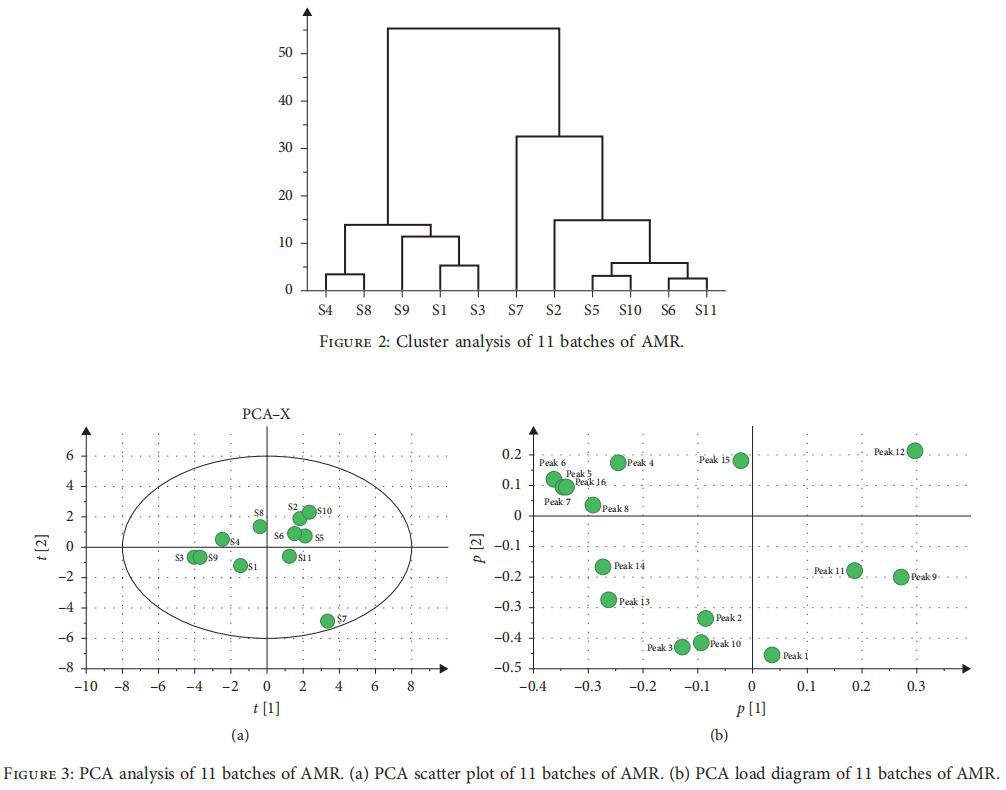
3.3.1. HCA. HCA wurde angewendet, um AMR aus verschiedenen Produktionsbereichen basierend auf verschiedenen Clustern und der Ähnlichkeit von Fingerabdrücken zu identifizieren. Die gemeinsame Peakfläche in 11 Chargen von AMR wurde als Indikator verwendet, und die Clusteranalyse wurde von der Software SIMCA14.1 durchgeführt. Die Ergebnisse sind in Abbildung 2 dargestellt. Die Proben von 11 Chargen von AMR wurden in 3 Kategorien eingeteilt, wenn die Klassenabstände zwischen 20 und 30 lagen, von denen S4, S8, S9, S1 und S3 in die Kategorien I und S7 eingeteilt wurden in Kategorie II gruppiert, während S2, S5, S10, S6 und S11 in Kategorie III gruppiert wurden.
3.3.2. PCA. In dieser Studie wurde der PCA von 11 Chargen AMR berechnet; in 16 Hauptkomponenten betrug der kumulierte Beitrag der Varianz der ersten fünf Hauptkomponenten 91,3 Prozent.DerDie Bewertungsmatrix der ersten beiden Komponenten würde für die Analyse verwendet, da die kumulative Varianz 65,9 Prozent überstieg.DerKonstruieren Sie daher in Ermangelung einiger Informationen eine zweidimensionale Ebene der Hauptkomponente, bei der die Abszisse eine Hauptkomponente und die Ordinate eine andere Hauptkomponente war. Dann wurden die 11 Proben auf die 2D-Ebene projiziert, so dass ihre natürliche Ansammlung beobachtet wurde (Abbildung 3(a)). Es wurde festgestellt, dass S4, S8, S9, S1 und S3 offensichtliche Klassifikationen hatten, S7 in einen Typ unterteilt werden konnte und S2, S5, S10, S6 und S11 in einen anderen Typ unterteilt werden konnten.DerDas PCA-Ergebnis stimmte mit dem HCA-Ergebnis überein.
Jeder Punkt im Belastungsdiagramm stellte einen chromatographischen Peak dar, der den Beitrag jedes chromatographischen Peaks zum umfassenden Effekt darstelltHauptbestandteile.DerGewichtswert der Variablen kannspiegeln die Korrelation zwischen der chemischen Zusammensetzung widerund die Probe in größtem Umfang.Derweiter weg vonUrsprung des Belastungsdiagramms, desto größer die VariableGewicht.DerDas Ergebnis ist in Abbildung 3(b) gezeigt, die vorgeschlagen wirddass die chromatographischen Peaks 9, 11 (Atractylenolid III),und 12 hatte einen größeren Einfluss auf die erste Hauptkomponente. Jedoch die chromatographischen Peaks 4, 5, 6, 15 und 16hatte einen größeren Einfluss auf die zweite Hauptkomponente. Eszeigte, dass die obigen chromatographischen Peaks a haben könntengrößeren Einfluss auf die Einstufung.


3.3.3. OPLS-DA.Der11 Proben wurden in zwei Gruppen eingeteilt, wobei S1, S3, S4, S8 und S9 die erste Gruppe waren und S2, S5, S6, S7, S10 und S11 die zweite Gruppe waren.DerGemeinsame Peak-Informationen aller Proben wurden in die SIMCA14.1-Software für OPLS-DA importiert. R2 X und R2 Y charakterisieren die Erklärungsrate des Modells für x- und y-Matrizen einzeln, und Q2 charakterisiert die Vorhersagefähigkeit des Modells.DerDie Ergebnisse zeigten, dass die Werte von R2 X, R2 Y und Q2 jeweils 0,939, 0,992 und 0,583 waren, die alle größer waren als {{ 9}}.5, was darauf hinweist, dass das Modell die beiden Gruppen von Proben unterscheiden konnte und eine bessere Anpassungs- und Vorhersagefähigkeit bei der Datenverarbeitung hatte. Es könnte verwendet werden, um AMR von verschiedenen Produktionsbereichen zu unterscheiden (Abbildung 4(a)).

DerDas Profil der für die Projektion wichtigen Variablen (VIP) im OPLS-DA-Modell kann den Beitrag jedes chromatographischen Peaks zur Probe widerspiegeln.DerDie VIP-Werte der 16 chromatographischen Peaks spiegelten die Einflussstärke auf jede AMR-Probe wider. Basierend auf dem Auswahlprinzip, dass der VIP-Wert größer als 1,0 und der Fehlerbalken kleiner als der Ursprung war (Abbildung 4(b)), wurden die 4 wichtigen chromatographischen Peaks ausgewählt, die der Reihe nach angeordnet wurden: Spitze 1 > Spitze 6 > Spitze 16 > Spitze 5.
DerDie Analyseergebnisse des Belastungsdiagramms sind in Fig. 4(c) gezeigt, die zeigten, dass die Positionen der obigen 4 wichtigen chromatographischen Peaks weit vom Ursprung entfernt waren. Es wurde vermutet, dass die 4 chromatographischen Peaks die Klassifikation von AMR signifikant beeinflussten und diese durch 4 chromatographische Peaks repräsentierten Komponenten die Hauptmarkerkomponenten jeder Probe sein könnten.

3.4. Bewertung der inhibitorischen Aktivität von AMR auf TYR in vitro.DerHemmwirkungen von AMR aus verschiedenen Produktionsgebieten auf die TYR-Aktivität wurden durch die biochemische Enzymmethode bestimmt.DerWirkungen von Proben auf die TYR-Aktivität sind in Tabelle 6 aufgeführt. Jede Probe mit einer Konzentration von 10 mg/ml konnte die TYR-Aktivität hemmen, und die pharmakologische Aktivität war bemerkenswert unterschiedlich, wobei die Hemmungsrate von S5 am höchsten war, während S6 am niedrigsten war.
3.5. Analyse von Spektrum-Effekt-Beziehungen. In diesem Artikel wurde PLS angewendet, um die Spektrum-Aktivitäts-Beziehung zu analysieren.Derpartieller Regressionskoeffizient und VIP-Wert sind in den Abbildungen 5(a) und 5(b) dargestellt, die zeigten, dass die chromatographischen Peaks 1, 2, 5, 6, 7, 9, 10, 11, 15 und 16 positiv mit dem korrelierten Hemmung der TYR-Aktivität, aber die chromatographischen Peaks 3, 4, 8, 12, 13 und 14 waren negativ mit ihnen korreliert. Unter den chromatographischen Peaks, die positiv mit der Hemmung der TYR-Aktivität korrelierten, waren die VIP-Werte der chromatographischen Peaks 11 (Atractylodes III) und 15 größer als 1, was darauf hinweist, dass diese beiden Komponenten die Hemmung der TYR-Aktivität signifikant beeinflussen.

3.6. Hemmende Wirkung von Atractylodes III auf TYR und molekulares Docking.DerDie inhibitorische Wirkung von Atractylodes III auf die TYR-Aktivität wurde durch das biochemische Enzymverfahren in vitro mit -Arbutin als Positivkontrolle bestimmt.DerDie Ergebnisse zeigten, dass die Hemmraten von Atractylodes III und -Arbutin auf die TYR-Aktivität 63,68 ± 2,36 Prozent bzw. 94,85 ± 0,35 Prozent betrugen, wenn die Konzentration der Proben 1 mg/ml betrug.
Molekulares Andocken wurde verwendet, um den Bindungsmechanismus von Atractylodes III zu untersuchen, der mit TYR interagiert (Abbildungen 6(a)–6(c)).DerDie Bindungsstelle der Pilztyrosinase besteht aus einem engen, flachen Hohlraum mit zwei Kupferionen (Cu2 plus ), die jeweils durch drei Histidinreste (z. B. His 61) im aktiven Zentrum des Enzyms stabilisiert werden. In dieser Studie ist Atractylodes III eine kleine Molekülverbindung, die sich im aktiven Zentrum des Enzyms befindet und mit den umgebenden Resten interagiert (His 244, Phe 264, Ala 286, His 263, Val 283, His259, His 85, Asn 260). Bemerkenswerterweise bildete Atractylodes III eine stabile Wasserstoffbrücke zu Asn 260 mit einer Bindungslänge von 1.9 ˚ A.


4. Schlussfolgerung
In dieser Studie wurde eine systematische Methode etabliert, die die HPLC-Fingerabdrücke mit chemometrischer Analyse verbindet, um AMR-Proben unterschiedlichen Ursprungs zu unterscheiden, und die aufhellende Wirkung von AMR wurde durch die biochemische Enzymmethode nachgewiesen. Die Beziehungen zwischen Spektrum und Wirkung zeigten an, dass die chromatographischen Peaks 1, 2, 5, 6, 9, 10, 11, 15 und 16 positiv mit der AMR-Hemmwirkung auf die TYR-Aktivität korreliert waren, darunter die Peaks 11 (Atractylenolid III) und 15 wichtige Wirkstoffe. Unterdessen hat Atractylenolid III im In-vitro-Test eine hohe TYR-Hemmaktivität, und das Ergebnis des molekularen Andockens zeigte, dass sein Mechanismus mit der Bindung von Aminosäureresten in der katalytischen TYR-Kapsel zusammenhängen könnte.DerDaher bewiesen diese Ergebnisse, dass Bioassay, molekulares Docking und Spektrum-Aktivitäts-Beziehungen geeignet sind, um die Qualität von Proben mit pharmazeutisch relevanten Wirkstoffen zu verknüpfen.

Datenverfügbarkeit
Die zur Stützung der Ergebnisse dieser Studie verwendeten Daten sind auf Anfrage beim korrespondierenden Autor erhältlich.
Offenlegung
Yong-Qin Liu und Chang-Yan Xu gelten als Co-Erstautoren.
Interessenskonflikte
Die Autoren erklären, dass bei dieser Studie keine Interessenkonflikte bestehen.
Autorenbeiträge
Yong-Qin Liu und Chang-Yan Xu trugen zu der Arbeit bei.
Danksagungen
Diese Studie wurde vom Innovation and Entrepreneurship Training Program for College Students in der Provinz Guizhou (Nr. 20195200925) gesponsert.
Verweise
[1] Y.-L. Wang, G. Hu, Q. Zhang, et al., "Screening und Charakterisierung von Tyrosinase-Inhibitoren aus Salvia miltiorrhiza und Carthamus tinctorius durch Spektrum-Effekt-Beziehungsanalyse und molekulares Docking", Journal of Analytical Methods in Chemistry, vol. 2018, Beitrags-ID 2141389, 10 Seiten, 2018.
[2] HX Cui, FF Duan, SS Jia, FR Cheng und K. Yuan, „Antioxidative und tyrosinasehemmende Aktivitäten von Samenölen aus Torreya grandis fort. ex Lindl“, BioMed Research International, vol. 2018, Beitrags-ID 5314320, 10 Seiten, 2018.
[3] Y. Tian, Z. Zhang, N. Gao, P. Huang und FY Wu, „Ein markierungsfreier Lumineszenz-Assay zur Überwachung der Tyrosinase-Aktivität und zum Inhibitor-Screening mit responsiven Lanthanoid-Koordinationspolymer-Nanopartikeln“, Spectrochimica Acta Teil A: Molecular and Biomolecular Spectroscopy, vol. 228, 2020.
[4] H. Liu, B. Liu, P. Huang, Y. Wu, FY Wu und L. Ma, "Colorimetrische Bestimmung von Tyrosinase basierend auf einer durch Goldnanopartikel katalysierten In-situ-Silbermetallisierung", MikroChim Acta, vol. 187, Nr. 10, p. 551, 2020.
[5] DC Franco, GS de Carvalho, PR Rocha, R. da Silva Teixeira, AD da Silva und NR Raposo, "Hemmende Wirkungen von Resveratrol-Analoga auf die Pilz-Tyrosinase-Aktivität", Molecules (Basel, Schweiz), vol. 17, Nr. 10, S. 11816– 11825, 2012.
[6] HH Kim, JK Kim, J. Kim, S.-H. Jung und K. Lee, "Charakterisierung von Caffeoylchinasäuren aus Episoden von Thunbergianus und ihrer Melanogenese-Hemmaktivität", ACS Omega, vol. 5, nein. 48, S. 30946–30955, 2020.
[7] F. Pintus, D. Span`o, A. Corona und R. Medda, "Anti-Tyrosinase-Aktivität von Euphorbia-characia-Extrakten", PeerJ, vol. 3, p. e1305, 2015.
[8] M. Shi, Y. Zhang, M. Song, Y. Sun, C. Li und W. Kang, „Screening der Markerkomponenten in Psoralea corylifolia L. mit Hilfe der Spektrum-Effekt-Beziehung und Komponenten-Knock- heraus durch UPLC-MS(2)," International Journal of Molecular Sciences, vol. 19, Nr. 11., 2018.
[9] G.-H. Wang, C.-Y. Chen, T.-H. Tsai et al., "Bewertung der Tyrosinase-hemmenden und antioxidativen Aktivitäten von Angelica dahurica-Wurzelextrakten für vier verschiedene probiotische Bakterienfermentationen", Journal of Bioscience and Bioengineering, vol. 123, Nr. 6, S. 679–684, 2017.
[10] YS Lin, HJ Chen, JP Huang et al., "Kinetics of tyrosinase inhibitory activity using Viti's vinifera leaf extracts", BioMed Research International, vol. 2017, Beitrags-ID 5232680, 5 Seiten, 2017.
[11] S. Yang, J. Zhang, Y. Yan, et al., "Netzwerk-Pharmakologie-basierte Strategie zur Untersuchung der pharmakologischen Mechanismen von Atractylodes macrocephala Koidz. für die Behandlung von chronischer Gastritis", Frontiers in Pharmacology, vol. 10, p. 1629, 2019.
[12] H.-R. Yang, J. Yuan, L.-H. Liu, W. Zhang, F. Chen und C.-C. Dai, "Endophytische Pseudomonas-Fluoreszenz-induzierte Sesquiterpenoid-Akkumulation, vermittelt durch Gibberellinsäure und Jasmonsäure in Atractylodes macrocephala Koidz-Pflanzen", Plant Cell, Tissue and Organ Culture (PCTOC), vol. 138, Nr. 3, S. 445–457, 2019.
[13] L. Hu, X. Chen, J. Yang und L. Guo, „Geografische Authentifizierung der traditionellen chinesischen Medizin Atractylodes macrocephala Koidz. (Baizhu) unter Verwendung stabiler Isotopen- und Multielementanalysen“, Rapid Communications in Mass Spectrometry, vol . 33, Nr. 22, S. 1703–1710, 2019.
[14] H. Li und G. Yang, "Das vollständige Chloroplastengenom von Atractylodes macrocephala Koidz. (Asteraceae)," Mitochondrial DNA Part B, vol. 5, nein. 3, S. 2060-2061, 2020.
[15] S. Gu, L. Li, H. Huang, B. Wang und T. Zhang, „Antitumorale, antivirale und entzündungshemmende Wirksamkeit von ätherischen Ölen aus Atractylodes macrocephala Koidz“, hergestellt mit unterschiedlichen Verarbeitungsmethoden, Molecules , Bd. 24, Nr. 16., 2019.
[16] J. Wang, L. Peng, M. Shi, C. Li, Y. Zhang und W. Kang, „Spektrumeffektbeziehung und Komponenten-Knockout in Angelica dahurica radix durch Hochleistungsflüssigkeitschromatographie-Q Executive-Hybrid-Quadrupol-Orbitrap-Massenspektrometer", Molecules, vol. 22, Nr. 7, 2017.
[17] B. Zhu, Q.-L. Zhang, J.-W. Hua, W.-L. Cheng und L.-P. Qin, "DerTraditional Uses, Phytochemistry, and Pharmacology of Atractylodes macrocephala Koidz.: a review“, Journal of Ethnopharmacology, Bd. 226, S. 143–167, 2018.
[18] Y.-Y. Feng, H.-Y. Ji, X.-D. Dong und A.-J. Liu, "Ein alkohollösliches Polysaccharid aus Atractylodes macrocephala Koidz induziert die Apoptose von Eca-109-Zellen", Carbohydrate Polymers, vol. 226, Artikel-ID 115136, 2019.
[19] W. Li, Y. Zhang, S. Shi, et al., „Spektrum-Effekt-Beziehung der Antioxidans- und Tyrosinase-Aktivität mit Malus pumila-Anhängern durch UPLC-MS/MS und Komponenten-Knock-out-Methode“, Food and Chemical Toxikologie, Bd. 133, Artikel-ID 110754, 2019.
[20] B. Xu, J. Gao, S. Zhao, Y. Li, Y. Du und H. Pan, "DerSpektrum-Effekt-Beziehung zwischen HPLC-Fingerabdruck und dem belebenden Blut und dem auflösenden Stasis-Effekt von Weißdornblättern“, Chromatographia, Bd. 83, Nr. 3, S. 409–421, 2020.
[21] Y. Feng, Z. Jing, Y. Li et al., "Screening anaphylaktoider Komponenten der Injektion von Shuang Huang Lian durch Analyse von Spektrum-Effekt-Beziehungen in Verbindung mit UPLC-TOF-MS", Biomedical Chromatography, vol. 33, Nr. 2, Artikel-ID e4376, 2019.
[22] X. Jiang, L. Tao, C. Li u . 25, Nr. 14., 2020.
[23] Y. Zhao, X.-M. Sie, H. Jiang, G.-X. Zou und B. Wang, "Spektrum-Effekt-Beziehungen zwischen Hochleistungsflüssigkeitschromatographie-Fingerabdrücken und entzündungshemmenden Aktivitäten von Leontopodium leontopodioides (Willd.) Beauv", Journal of Chromatography B, vol. 1104, S. 11–17, 2019.
[24] X. Zhou, Y. Li, M. Zhang, et al., „Spektrum-Effekt-Beziehung zwischen UPLC-Fingerabdrücken und Anti-Lungenkrebs-Effekt von Si Jun Zi Tang“, Evidence-Based Complementary and Alternative Medicine, vol. 2019, Beitrags-ID 7282681, 9 Seiten, 2019.
[25] X. Sun, Q. Zhao, Y. Si et al., "Bioaktive strukturelle Basis von Proteoglykanen aus Sarcandra glabra basierend auf der Beziehung zwischen Spektrum und Wirkung", Journal of Ethnopharmacology, vol. 259, Artikel-ID 112941, 2020.
[26] S. Gao, H. Chen und X. Zhou, "Studie über die Spektrum-Effekt-Beziehung der Xanthinoxidase-Hemmaktivität von Ligustrum lucidum", Journal of Separation Science, vol. 42, Nr. 21, S. 3281–3292, 2019.
[27] J. Tan, J. Liu, H. Wang, et al., "Identification of blood-activating components from Xueshuan Xinmaining tablet based on the spectrum-effect relationship and network pharmacology analysis," RSC Advances, vol. 10, no. 16, pp. 9587–9600, 2020.
[28] J. Zhang, T. Chen, K. Li et al., "Screening aktiver Inhaltsstoffe von Rosmarin basierend auf Spektrum-Effekt-Beziehungen zwischen UPLC-Fingerprint und vasorelaxanter Aktivität unter Verwendung von drei Chemometrien", Journal of Chromatography B, vol. 1134-1135, Artikel-ID 121854, 2019.
[29] Y. Chen, G. Pan, W. Xu et al., "Spektrum-Effekt-Beziehungsstudie zwischen HPLC-Fingerabdrücken und antioxidativer Aktivität von Sabia parviflflora", Journal of Chromatography B, vol. 1140, Artikel-ID 121970, 2020.
[30] M. Liao, P. Yan, X. Liu, et al., „Spektrum-Effekt-Beziehung für die Anti-Tumor-Aktivität von Shikoninen und Shikonofuranen in medizinischem Zicao durch UHPLC-MS/MS und chemometrische Ansätze“, Journal of Chromatographie B, Bd. 1136, Artikel-ID 121924, 2020.
[31] JH Wu, YT Cao, HY Pan und LH Wang, "Identifizierung von Antitumorbestandteilen in Krötengift durch Spektrum-Effekt-Beziehungsanalyse und Untersuchung seines pharmakologischen Mechanismus", Molecules, vol. 25, Nr. 18., 2020.
[32] J. Tang, J. Liu und F. Wu, "Molekulare Docking-Studien und biologische Bewertung von 1,3, 4- Thiadiazol-Derivaten, die Schiffff-Basen-Einheiten als Tyrosinase-Inhibitoren tragen", Bioorganic Chemistry, vol. 69, S. 29–36, 2016.






