Vitamin-D3-Mangel führt zu Störungen der Immunität mit schwerer Müdigkeit und Depressionen bei einer Vielzahl von Krankheiten
Mar 18, 2022
ANNA DOROTHEA HÖCK
Praxis für Innere Medizin, Köln, Deutschland
Kontakt:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791

Abstrakt
Aktuelle Immundaten zu Vitamin-D3-Mangel helfen dabei, chronische Erschöpfungskrankheiten wie Autoimmunerkrankungen, Krebs und chronisches Erschöpfungssyndrom (CFS) besser zu verstehen. Der Vitamin-D3-Weg wird durch Stress aktiviert und erfordert ausreichende Vorräte an Vorläufer-25--Hydroxyvitamin D3 für ordnungsgemäße Zell- und Immunfunktionen. Bei Vitamin-D3-Mangel ist die Sekretion des antimikrobiellen Peptids Cathelicidin reduziert, was zu einer Beeinträchtigung der Auto-/Xenophagie führt. Als Ergebnis werden Phagozytose, Zytotoxizität, Antigenprozessierung und Antigenpräsentation dysreguliert. Darüber hinaus beeinflusst ein Vitamin-D3-Mangel die Aktivierung von T- und B-Lymphozyten sowie die Menge, Reifung und Funktion von regulatorischen natürlichen Killer-T-Zellen und ihren Gegenstücken im Darm, dh T-Zell-Rezeptor-Cluster der Differenzierung{{ 11}} positive intraepitheliale Lymphozyten. Folglich werden angeborene und adaptive Immunität dereguliert, wobei mikrobielle Effekte weiter dazu beitragen. Es folgen anhaltende Infektionen, chronische Entzündungen und Müdigkeit. Die Substitution von Vitamin D3 bei solchen Zuständen kann dazu beitragen, solche chronischen Zustände zu verhindern oder zu lindern, sogar bei Patienten mit Krebs. Vitamin-D3- und Kalziummangel treten bei verschiedenen Krankheiten auf, darunter Immunstörungen (1-6) und bei chronischer Müdigkeit (7-15). Einige positive Vitamin-D-Behandlungsberichte (11, 12, 15, 16) weisen auf einen möglichen Zusammenhang zwischen Vitamin-D3-Mangel und chronischer Müdigkeit, Erschöpfung und Depression hin. Dieser Artikel gibt einen Überblick über die Immunreaktivität in Bezug auf den Vitamin-D3-Spiegel und die Deregulierung der Energie bei Vitamin-D3-Mangel.
Schlüsselwörter: Vitamin D3, Müdigkeit, Depression
Eine ausreichende Versorgung mit Vitamin D3 ist wichtig für die ordnungsgemäße Funktion der menschlichen Zellen und die Reaktion auf Stress
Nach Lichtaktivierung in der Haut und weiterer enzymatischer Verarbeitung wird aus dem aktiven Metaboliten 1,25-Dihydroxyvitamin D3 [1,25(OH)2D3] der Vitamin-D3--Vorstufe, auch Calcitriol genannt, synthetisiert das unmittelbare Prohormon 25- Hydroxycholecalciferol (25OHD3) durch das Enzym Cytochrom p450-hydroxylase27B1 (CYP27B1). Die Reaktion wird in den Nieren durch Parathormon vermittelt und ist kalziumabhängig (17). Dieser endokrine Weg dient der strengen Regulierung des Serumkalziumspiegels (5, 6, 17). Die meisten Zellen wandeln jedoch auch 25OHD3 in aktives 1,25(OH)2D3 um, das als para- oder autokriner Transkriptionsfaktor dient, der an viele Genloci bindet (17-22). Darüber hinaus beeinflusst 1,25(OH)2D3 auf epigenetische Weise direkt Zellsignale und Zellfunktionen (21, 23-25). 1,25(OH)2D3 ist ein wichtiger Zellregulator und beeinflusst die Zellentwicklung, Differenzierung, Proliferation und Zellzykluskontrolle (20, 21). Verschiedene Arten von Zellstress verursachen eine Aktivierung des Vitamin-D-Signalwegs, und die Bildung von 1,25(OH)2D3 erfordert eine ausreichende Versorgung mit dem Vorläufer 25OHD3, um eine wirksame Schutzreaktion aufzubauen (17, 22). Insbesondere Immunfunktionen sind stark von 1,25(OH)2D3 abhängig. Eine ausreichende Funktion von Immunzellen hängt vom Vitamin-D3-Weg ab, der durch die Expression des Vitamin-D-Rezeptors (VDR) und des Vitamin-D-aktivierenden Enzyms CYP27B1 (1, 5, 17, 26-29) initiiert wird. Darüber hinaus vermittelt 1,25(OH)2D3 die Induktion von spannungsgesteuerten Chlorid- und Calciumionenkanälen und reguliert die Sekretion von Zellprodukten, z. B. Transmittern und Immungranula (23). Das komplexe Zusammenspiel von durch Vitamin D3-induzierten Wirkungen, die zu einer Immunwirksamkeit und zu ausgewogenen Immunreaktionen führen, sind in den Abbildungen 1-3 zusammengefasst.
Physikalische und funktionelle Epithelbarrieren werden durch 1,25(OH)2D3 verbessert
In der ersten Verteidigungsphase an Haut- und Schleimhautbarrieren reguliert 1,25(OH)2D3 die Genexpression wichtiger Proteine, die für die Versiegelung epithelialer Tight Junctions verantwortlich sind, dh Claudine, und stabilisiert so Haut- und Schleimhautbarrieren (28, 30-32) . 1,25(OH)2D3 verstärkt die Keratindifferenzierung (33-34), moduliert die mitogenaktivierte Proteinkinase-Signalgebung in Keratinozyten, indem es entzündungshemmende und schützende Wirkungen ausübt (35), und reguliert die Matrix-Metalloproteinase herunter {{16} } (36). Auch 1,25(OH)2D3 schützt vor Strahlungseffekten (37) und vor dem programmierten Zelltod in gestressten Keratinozyten (38). 1,25(OH)2D3 reduziert die Reaktionsfähigkeit von Interleukin-2(IL-2)-aktivierten T-Lymphozyten und verringert so stressinduzierte lokale Entzündungsreaktionen (39).
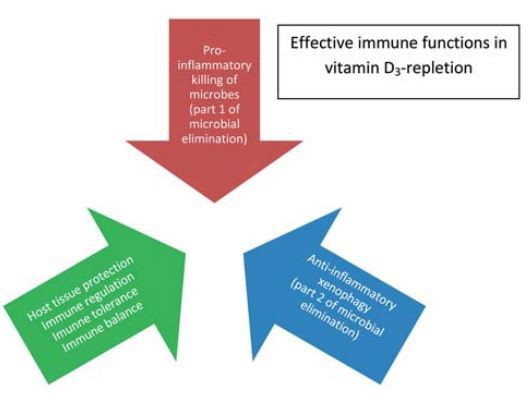
Abbildung 1.Die Vitamin-D3-Ergänzung gewährleistet eine effektive mikrobielle Eliminierung, kombiniert jedoch mit einer sofortigen schützenden Entzündungshemmung und Immunregulierung.
Einfluss von 1,25(OH)2D3 auf antimikrobielle Peptide (AMiPs)
AMiPs werden nach einer mikrobiellen Herausforderung von Epithelzellen, von natürlichen Killerzellen (NK), δ-T-Lymphozyten und auch von B-Lymphozyten (28, 29, 40, 41) produziert, die als wichtige biochemische Barrieren dienen. AMiPs destabilisieren Bakterienmembranen durch kationische und elektrostatische Effekte (28, 29, 40). Darüber hinaus sind sie multifunktional und binden an bestimmte Zellsignalrezeptoren und an DNA (42-45). Sie interagieren mit Immun-, Endothel- und Epithelzellen (42, 46, 47), verstärken Phagozytose, Auto/Xenophagie, zelluläre Zytotoxizität, Chemoattraktion von Immunzellen, Induktion von Gedächtnis-T-Zellen, Angiogenese und Wundheilung (28, 29, {{ 18}}, 46, 47). AMiPs besitzen auch immunregulatorische Wirkungen, indem sie entzündungsfördernde Zytokine unterdrücken, die Toll-like-Rezeptor(TLR)-Expression herunterregulieren und Endotoxine neutralisieren (27, 28, 42, 46, 47). Beim Menschen verstärkt 1,25(OH)2D3 signifikant die Expression von zwei antimikrobiellen Peptiden, genannt Cathelicidin und Defensin-4B (27-29, 40, 49, 50). Wichtig ist, dass AMiPs synergistisch mit 1,25(OH)2D3 wirken, die angeborenen Immunfunktionen verbessern sowie Entzündungen herunterregulieren und adaptive Immunregulation. Als Gegenmaßnahme reduzieren bakterielle Toxine die Cathelicidin-Expression (51). Interessanterweise regulieren Mäuse ohne Sonnenexposition im Gegensatz zu Menschen die Cathelicidin-Expression unabhängig von 1,25(OH)2D3 (52). Das sekretorische Immunglobulin A (sIgA), eine weitere biochemische Barriere von Haut und Schleimhaut, wird durch 1,25(OH)2D3 eher indirekt unterstützt, indem es die Expression des kristallisierbaren Immunglobulin-A-Fragment-Rezeptors (IgA Fc) auf Phagozyten induziert, was zu einer verstärkten Bindung von sIgA führt ( 53-55). Darüber hinaus induziert 1,25(OH)2D3 den CC-Motiv-Chemokinrezeptor -10 (CCR10) in menschlichen B-Zellen, was zu einer verstärkten B-Zell-Differenzierung zu IgA-sekretorischen Zellen führt, mit dem Potenzial für ein Homing in den Darm ( 56, 57).
Auto/Xenophagie als wichtiger zellulärer Rheostat und seine Beziehung zu 1,25(OH)2D3 und Cathelicidin
Autophagie, eine Infektion, die auch als Immun- oder Xenophagie bezeichnet wird, ist für die Zell- und Immunfunktion unerlässlich (58-62). Beschädigtes Material (z. B. Zelle oder Gewebe) wird in einem mehrstufigen Prozess abgebaut, dessen Produkte zur Funktionsanpassung, zum Recycling von Bausteinen und zur Energiegewinnung genutzt werden (58, 60). Die Autophagie funktioniert wie ein Rheostat und verbindet interne und externe Bedingungen mit Zellregulationswegen (60, 63). Unterschiedliche autophagische Schritte (Initiation/Induktion mit Keimbildung; Verlängerung und Schließung der autophagosomalen Doppelmembran; Reifung und Fusion mit dem Lysosom) erzeugen das Auto(phago)lysosom, das das aufgenommene Material mit größerer Wirksamkeit abbaut oder ausstößt als das Phagolysosom ( 52, 58, 60, 62, 64). Drei Zell-Signalisierungssysteme initiieren die Auto/Xenophagie. Erstens Hemmung des Säugetier-Targets Rapamycin (mTOR)-AuTophaGy-related -1 (ATG1)-Komplex; zweitens der Beclin1/Klasse-III-Phosphoinositol-3-Kinase-C3/vakuoläres Proteinsortierungs-assoziiertes Protein (PI3KC3)/VPS34)-Komplex (58, 65); und drittens die AuTophaGy-verwandten Proteine ATG5- ATG12-ATG16L1 und ATG7-ATG3-ATG8/Mikrotubuli-assoziiertes Protein 1A/1B-leichte Kette 3 (LC3) /Gamma-Aminobuttersäurerezeptor-assoziierter Proteinkomplex (GABARAP) (59). Diese Signalsysteme reagieren auf Stress, indem sie TLRs oder Nukleotid-bindende Oligomerisierungsdomänen (NOD)-ähnliche Rezeptoren, Kernfaktor-ĸB (NF-kB) und entzündungsfördernde Zytokine wie Interferon-Gamma (IFN-) und Tumor aktivieren Nekrosefaktor-alpha (TNF-) sowie durch Erhöhung des intra- oder subzellulären Calciums mit anschließender Aktivierung der Adenosinmonophosphat-aktivierten Proteinkinase (AMPK) (59, 63, 66, 67).

Wichtig ist, dass in Autophagolysosomen Selbst- und Nicht-Selbst-Peptide mit Antigen-präsentierenden Molekülen verbunden werden (58, 62), ein Prozess, der wesentlich zur Immunkontrolle, entzündungshemmenden Aktivität und dem Immungedächtnis beiträgt (59, 62, 68-70 ) und Induktion von selbsttoleranten T-Zellen (58, 65). Epithelzellen und Thymozyten des Thymus verwenden eine wirksame Auto/Xenophagie zur positiven und negativen Selektion von T- und B-Zellen (71). Es wurde berichtet, dass eine deregulierte Autophagie zu Autoimmunerkrankungen (62, 64) und Krebs (63, 72) führt. 1,25(OH)2D3 verstärkt die Auto/Xenophagie auf mehreren Ebenen, wie z. B. NOD2-Rezeptorexpression, ATG16L-Rekrutierung an der Stelle des Bakterieneintritts (73) oder PI3KC3-Aktivierung, wodurch die Initiierung, Nukleation und Verlängerung der autophagosomalen Membran unterstützt wird ( 64). Was jedoch noch effizienter bei der Auto/Xenophagie ist, ist die Zusammenarbeit von sowohl 1,25(OH)2D3 als auch Cathelicidin (26, 49, 52, 64, 66, 67, 74, 75). Beide Wirkstoffe verstärken die beclin-1-Genexpression (66, 75, 76) und fördern die Autophagosomenreifung sowie die lysosomale Fusion (26, 64, 74). Sie erhöhen auch den Säuregehalt und die Proteaseaktivität in Autophagolysosomen (66, 74). Interessanterweise beeinträchtigt eine gestörte Autophagie die Cathelicidin-Expression, was eine bidirektionale Kopplung zwischen Cathelicidin und Autoxenophagie offenbart (64). Auto/Xenophagie hängt ferner von negativen Kontrollmechanismen ab (77). Zu den negativen Kontrollregulatoren gehören Mitglieder der Autophagiemaschinerie selbst wie ATG16L1 und der ATG5-ATG12-Komplex, was zu einer verringerten Produktion von IL-1, IL-18 und Typ I IFN- führt (58, 62 , 77). 1,25(OH)2D3 trägt zur Negativkontrolle bei, indem es entzündungsfördernde Signale wie NF-kB, TNF-, IFN- hemmt und den Cyclin-abhängigen Kinase-Inhibitor P19INK4D fördert (64).

Figur 2.Die wichtigsten direkten und indirekten kooperativen und teilweise bidirektionalen Immuneffekte des Vitamin-D3-Wegs. 25-OHD3 25- Hydroxyvitamin D3; 1,25(OH)2D3 1 ,25-Dihydroxyvitamin D3; VDR-Vitamin-D-Rezeptor; mDC myeloische dendritische Zelle, NK T-Zellen Natürliche Killer-T-Zellen.
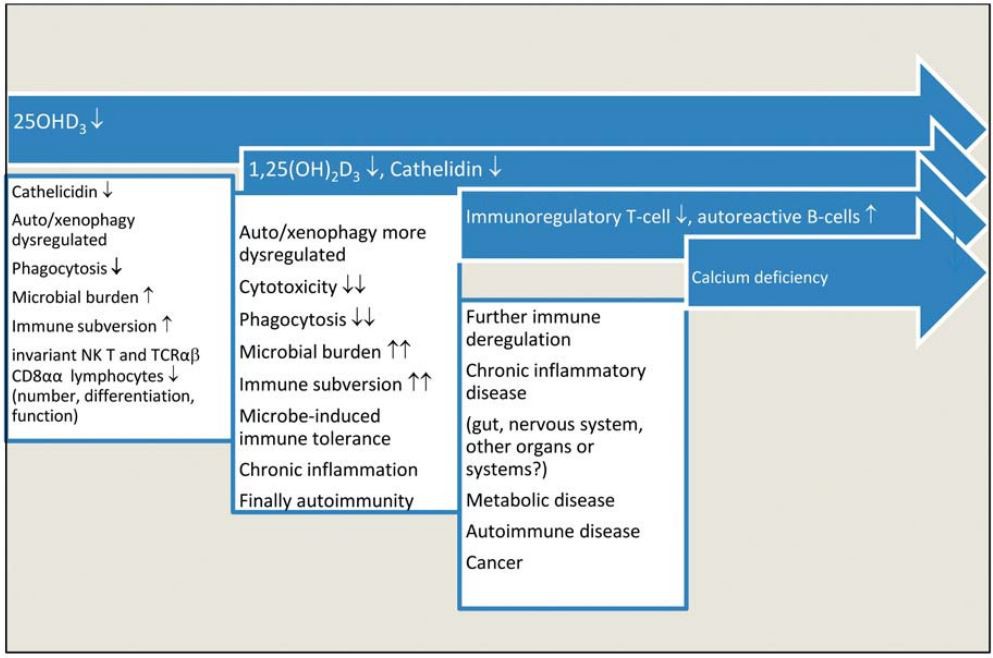
Figur 3.Vitamin-D3--Mangel führt zu einem erheblichen angeborenen Immundefekt, während die zu erwartende adaptive Immunintoleranz trotz schwelender chronischer Entzündung vermutlich durch mikrobielle Immunsubversionsmechanismen modifiziert wird, die durch ausgeprägte Immuntoleranz gekennzeichnet sind. Es folgt eine Hierarchie weiterer Immunderegulationsschritte, die im Problem des chronischen Kalziummangels mit einer Verschlimmerung der Immunregulation gipfeln.
Endo- und Phagozytose werden durch 1,25(OH)2D3 und Cathelicidin verstärkt
1,25(OH)2D3 verstärkt die Endozytose durch verstärkte Genexpression von Antigenaufnahmerezeptoren, einschließlich Mannoserezeptor und FC-Rezeptor II (CD32) (74, 78). Phagozytose wird durch 1,25(OH)2D3--vermittelte Verstärkung der Makrophagenreifung, lysosomale Produktion von sauren Phosphatasen und Wasserstoffsuperoxid (H2O2) und verstärkte Xenophagie gefördert (1, 5, 28, 50, 79). Obwohl 1,25(OH)2D3 die Endozytose und Phagozytose fördert, reduziert es die Antigenpräsentation, die T-Zell-Aktivierung und die Sekretion entzündungsfördernder Zytokine (80, 81). Die Zusammenarbeit von 1,25(OH)2D3, Cathelicidin und Autoxenophagie optimiert die Neutralisierung der Endotoxin-induzierten proinflammatorischen TNF- und Stickoxidproduktion (42, 52, 75, 82).
1,25(OH)2D3 induziert immuntolerante myeloische dendritische Zellen und regulatorische T-Zellen
Die angeborene und adaptive Immunität ist mit dendritischen Zellen (DCs) verbunden, die adaptive Immunantworten und entzündungshemmende Regulation orchestrieren (56, 83, 84). Die bekanntesten DC-Subtypen sind myeloide (mDCs) und plasmazytoide (pDCs) dendritische Zellen (56, 83, 85). mDCs sind Antigen-präsentierende Zellen (86) und tragen Antigen-bindende Oberflächenrezeptoren der Haupthistokompatibilitäts(MHC)-Gruppe (83, 86, 87), sowie MHCI-ähnliche Rezeptoren, wie z als Glykoprotein-Cluster des Differenzierungsproteins-1-Familienmitglieds (CD1d) (83). Aktivierte mDCs sezernieren IL-12 (87, 88) und induzieren unterschiedliche T-Zellpopulationen wie Th1--Zellen für intrazelluläre und Th17--Zellen für extrazelluläre Pathogene und Th{{24 }}Populationen mit regulatorischen T-Zellen (Treg) für unvollständig zerstörte Pathogene (86, 87). Ohne Aktivierung sind mDCs stark von 1,25(OH)2D3 abhängig, was eine erhebliche Immuntoleranz induziert (27, 56, 83, 84, 87, 89, 90). Unreife, noch nicht stimulierte mDCS und ihre Vorläuferzellen exprimieren reichlich VDRs, im Gegensatz zu stimulierten mDCs. Daher bewahren differenziertere mDCs mit geringerer VDR-Expression ihr erforderliches Abwehrpotential (56, 84, 88). Aber selbst bei antigener Stimulation sind mDCs toleranter, wenn 1,25(OH)2D3 vorhanden ist (56, 84, 88, 89). 1,25(OH)2D3-induzierte Immuntoleranz wird durch Herunterregulierung entzündungsfördernder Moleküle in mDCs wie CD40, CD80, CD86, MHCII, CD54, IL{{ 61}}/IL-23p40 und der CC-Motiv-Chemokinligand 17 (CCL17) (56, 84, 88). Darüber hinaus werden immunhemmende Moleküle hochreguliert, einschließlich des Immunglobulin-ähnlichen Transkripts -3 (ILT3) und des programmierten Todesliganden -1 (PDL-1) (56, 84). Infolgedessen sezernieren mDCs weniger IL-12, aber mehr IL-10 und den transformierenden Wachstumsfaktor (TGF) (26, 56, 91), wodurch eine Verschiebung von Th17 und Th9 zu regulatorischem CD4 plus CD25 gefördert wird plus Tregs (3, 92, 93).
Tregs exprimieren vermehrt inhibitorische Rezeptoren, einschließlich FOXP3 und zytotoxisches lymphozytisches Antigen-4 (CTLA-4) (27, 84, 94, 95). Von Interesse ist die zwischen DCs und Tregs beobachtete gegenseitige Toleranzinduktion (56, 96). Die Induktion einer signifikanten Th2--Polarität durch 1,25(OH)2D3 wurde jedoch kürzlich in Frage gestellt (97). 1,25(OH)2D3--induzierte T-Zell-Toleranz wird auch durch direkte Wirkung auf aktivierte T-Zellen vermittelt (26, 56, 98, 99). 1,25(OH)2D3 reduziert die proliferative Aktivität von Th1-Zellen, indem es die Expression entzündungsfördernder Zytokine wie IL-2, IFN- und TNF- (56, 98-100) reduziert. 1,25(OH)2D3 verstärkt auch die T-Zell-Sekretion von IL-4 und IL-13 (90) durch Induktion des Stress- und Translationsinhibitorproteins Cytidin-Cytidin-Adenosin-Adenosin-Thymidin-Box-Motiv (CCAAT )/Enhancer-bindendes Protein (EBP) homologes Protein (CHOP) (101, 102) und induziert wichtige Th2-Transkriptionsfaktoren, wie Signalumwandler und Aktivator der Transkription -6 und GATA-bindendes Protein und CD 200 , ein Immunglobulin-ähnliches Molekül auf CD4 plus T-Lymphozyten, das die Th17-Differenzierung hemmt (103). Schützende Schleimhauttoleranz wird auch durch 1,25(OH)2D3 induziert, indem das Schleimhaut-Homing von immunregulatorischen dendritischen Zellen verstärkt wird (1, 28, 104-106). Stress- und 1,25(OH)2D3--induzierte Induktion von Vitamin-D-hochregulierendem Protein (VDUP1) unterdrückt zusätzlich proinflammatorische Lymphozyten in der Lamina propria (107). Im Gegensatz zu mDCs sind pDCs auf die Viruskontrolle über IFN-Sekretion spezialisiert (56, 84, 89). Sie induzieren auch Tregs, scheinen jedoch unabhängig von 1,25(OH)2D3 zu sein (56). pDCs induzieren Tregs und adaptive Immuntoleranz auf verschiedene Weise: i) durch Hochregulierung des induzierbaren costimulatorischen Liganden (ICOSL) mit oder ohne Sekretion von Indolamin 2, 3- Dioxygenase (IDO) (84, 108), ii ). ) bei Zuständen wie chronischer Entzündung und/oder Autoimmunität (109) und iv) durch thymisches stromales Lymphopoietin (TSLP) durch pDCs oder Epithelzellen (84, 110). Tregs werden auch durch Retinsäure induziert (84, 111).

Cathelicidin und NK-Zellen in der angeborenen und adaptiven Immunität
NK-Zellen werden durch direkten DC/NK-Kontakt aktiviert und kooperieren mit CD8 plus zytotoxischen T-Zellen (112, 113). Weitere bidirektionale Aktivierungssignale können von Makrophagen, polymorphkernigen Leukozyten, T- und B-Lymphozyten, Mast- und Epithelzellen oder als inhibitorische Signale von Tregs empfangen und an diese gesendet werden (112, 114, 115, 116). NK-Zellen sezernieren antimikrobielle Peptide wie -Defensin und Cathelicidin (48, 115, 117) und induzieren entzündungshemmende, immunregulatorische (118) und Immungedächtniseffekte (112, 113, 115). Ihre Reifung und Funktion hängen vom Signalmilieu der Umwelt ab (112-114, 118, 119). Eine zuverlässige In-vivo-Bewertung der NK-Zellfunktionen ist jedoch durch komplexe Zellkinetiken und variable Signale aus der Umgebung begrenzt (114, 120, 121). „Erschöpfte“ NK-Effektorzellen wurden bei chronischen Infektionsprozessen beschrieben (113). Aufgrund dieser komplexen Beziehungen bleiben die berichteten Wirkungen von 1,25(OH)2D3 auf NK-Zellen widersprüchlich. Einige Berichte beschreiben Hemmwirkungen (122) mit verminderter NK-Zellaktivierung und Zytotoxizität bei Ratten (123-125), reduzierter NK-Zell-Chemotaxis gegen Eosinophile und reduzierter IL-15--induzierter IL-8-Sekretion ( 126). Andere zeigten eine Hemmung der NK-Zellaktivierung durch 1,25(OH)2D3, aber keine Hemmung der Zytotoxizität, mit umgekehrter Hemmung nach Immunaktivierung mit IL-2-Sekretion oder exogener IL-2-Zugabe (127, 128) . Im offensichtlichen Gegensatz dazu wurde eine verstärkte Zytotoxizität der NK-Zellen nach der Behandlung mit aktivem Vitamin D3 (Calcitriol) bei Hämodialysepatienten beobachtet (129). Eine verstärkte NK-Zytotoxizität gegenüber Krebszellen resultierte aus einem 1,25(OH)2D3--induzierten Anstieg von Cathelicidin (46, 48). Indirekte positive Wirkungen auf die NK-Zytotoxizität wurden durch eine 1,25(OH)2D3--induzierte Erhöhung der Glutathionsynthese (130, 131) und durch eine 1,25(OH)2D3--induzierte Erhöhung der Extrazellulärität vermittelt Kalziumspiegel mit erhöhter Aktivität von Proteinkinase C (PKC) und N alpha-Benzyl-Oxycarbonyl-L-Lysin-Thiobenzylester (BLT)-Esterase (132). Darüber hinaus wurden die Differenzierung und Reifung von NK-Zellen durch die VDUP1-Expression verstärkt, ein Effekt, der durch einen unterschiedlichen zellulären Calciumeinstrom weiter verstärkt werden könnte (107, 133).
Vitamin-D-Rezeptor und 1,25(OH)2D3 sind am wichtigsten für invariante NK-T-Zellen
NK-T-Zellen exprimieren NK- und T-Zelltyp-spezifische Rezeptoren (134, 135). Die meisten NK-T-Zellen gehören zur Untergruppe der invarianten NK-T-Zellen, auch Klasse-I-NK-Zellen genannt (110, 136- 139), die funktionell eher Tregs als NK-Zellen ähneln (134, 135). Sie gelten als am wichtigsten für das gesamte Immunsystem (134, 140, 141). Der Begriff „invariant“ bezieht sich auf ihren semi-invarianten speziellen T-Zell-Rezeptor (TCR) mit einer invarianten Alpha- und einer eingeschränkten Beta-Kette (140). Anders als herkömmliche T-Zellen sezernieren sie konstitutionell IL-4 und IFN- und erhöhen die Sekretion schnell nach Immunherausforderung (134-136). IL-4 ist wichtig für die Aktivierung der B-Zellen des Immunsystems (142) und verhindert eine Überstimulation des Immunsystems, chronische Entzündungen und Autoimmunität (136). Im Gegensatz dazu ist IFN- wichtig für die virale Clearance, weitere Immunaktivierung, antimikrobielle Abwehr (143, 144) und Phagosomenreifung (52). Wie NK-Zellen üben invariante NK-T-Zellen sowohl immunaktivierende als auch immunregulatorische Aktivität aus und verbinden angeborene und adaptive Immunfunktionen durch eine gegenseitige und mehrdimensionale Wechselwirkung (145-148). Sie verstärken die zytotoxischen CD8 plus T-Zell-Antworten durch Induktion der CD70-Expression auf dendritischen Zellen (147). Invariante NK-T-Zellen bestehen aus mehreren Untergruppen mit funktionellen Unterschieden (145, 146). Ihre Zahl scheint bei bestimmten Autoimmunerkrankungen verringert zu sein (145, 146). Invariante NK-T-Zellen sind eng mit dem Vitamin-D-Weg verbunden (100, 136-139). Entwicklung und Funktion eines doppelt positiven intrathymischen invarianten NK-T-Zellvorläufers hängen ausschließlich von der intrathymischen VDR-Expression und der VDR-abhängigen Induktion des nichtklassischen MHCI-Rezeptors CD1d ab (100, 136-139). CD1d ist strukturell mit 2--Mikroglobulin assoziiert, ähnlich dem MHCI-Rezeptor (134, 140). Der CD1d-Rezeptor präsentiert Selbstantigene, vorzugsweise endogene Lipide und Glykolipide (136, 138, 141). Invariante NK-T-Zellen sind selbstreaktiv, aber nicht selbstzerstörerisch (134, 136-138).
Während die Agonistenselektion von invarianten NK-T-Zellen im Thymus abgeschlossen wird, wird die vollständige Reifung in der Peripherie abgeschlossen, wo invariante NK-T-Zellen bevorzugt Leber und Milz bewohnen (140, 141, 143, 145). Invariante NK-T-Zellen verlieren während ihrer spezifischen Differenzierungsschritte CD8-, oft auch CD4-Co-Rezeptor (100). Sie beginnen, Rezeptoren der NK-Linie zu exprimieren, wie z. B. den aktivierenden integralen Membranproteinrezeptor vom Typ II (NKG2D), Mitgliederder Ly-49-Familie und schließlich der mit natürlichen Killerzellen (NK) assoziierte Marker NK1.1 (CD161) (138) und der T-Zell-Gedächtnis-CD44-Rezeptor (137). Während dieser Reifungsschritte werden immunregulatorische Eigenschaften mit Schutz vor Krankheitserregern, Krebs und Autoimmunität erworben (145, 146). Interessanterweise ist nicht nur 1,25(OH)2D3, sondern auch VDUP1 für die invariante Entwicklung von NK-T-Zellen erforderlich (133). Studien an Mäusen mit ausgeschaltetem VDR zeigten reduzierte invariante NK-T-Zellzahlen und reduzierte IFN- und Il{-4}-Sekretion nach Antigenexposition (100, 136, 149, 150). Die Zellreifung war beeinträchtigt, da CD44 plus- und NK1.1 plus-Rezeptoren nicht hochreguliert werden konnten (100, 138, 149-151). Vitamin-D3--defiziente Wildtyp-Mäuse hatten aufgrund erhöhter Apoptose im Thymus eine reduzierte Anzahl invarianter NK-T-Zellen, hatten aber nach Vitamin-D3-Supplementierung eine fast normale Zellfunktion (100, 106, 138, 150). Die Substitution von 1,25(OH)2D3 stellte jedoch die invarianten NK-T-Zellzahlen nicht vollständig wieder her, ein Effekt, der sogar auf ihre Nachkommen übertragen wurde, möglicherweise aufgrund epigenetischer Veränderungen, die durch Vitamin-D3-Mangel induziert wurden (150). Sowohl VDR- als auch Vitamin-D-defiziente Tiere neigten dazu, entzündliche Darmerkrankungen und experimentell induzierte Enzephalomyelitis zu entwickeln (32, 100, 106, 149).

Intraepitheliale CD8-TCR-Zellen sind invariante NK-T-Zell-äquivalente Darmschleimhautzellen und für das lokale Immungleichgewicht unerlässlich
Im Darmepithel wurde eine Zellpopulation gefunden, die funktionell invarianten NK-T-Zellen ähnelt (32, 100, 106, 136). Sie entwickeln sich auch aus derselben intrathymischen invarianten NK-T-Vorläuferzelle. Wie invariante NK-T-Zellen hängen sie von intrathymischer Agonistenselektion ab, sind selbstreaktiv ohne Selbstzerstörung und weisen Phänotypen von regulatorischen oder Gedächtniszellen auf (32, 100). Im Gegensatz zu invarianten NK-T-Zellen exprimieren sie in Gegenwart von IL-15 eine darmspezifische homodimere CD8-Plus-Kette (152) und werden als TCR plus CD8 plus intraepitheliale Lymphozyten identifiziert (100, 106, 136). . Die Darmschleimhaut von VDR-Knockout-Tieren enthält nur halb so viele CD8-Plus-Zellen, und die intraepithelialen CD4/CD8-Lymphozyten fehlen vollständig, vermutlich aufgrund eines fehlgeschlagenen Darm-Homings (3, 100, 106, 136).
Aktivierte B-Zellen exprimieren VDR und Interaktionen zwischen B-Zellen und invarianten NK-T-Zellen modulieren Immunantworten
Aktivierte B-Zellen exprimieren wie aktivierte T-Zellen VDR. Vermittelt durch ihren Antigen-spezifischen B-Zell-Rezeptor präsentieren auch B-Lymphozyten Antigene und unterstützen die Phagozytose (153, 154). Schließlich sezernieren aktivierte B-Zellen Cathelicidin und tragen durch Interaktion mit 1,25(OH)2D3 und Cathelicidin zu einer optimalen Immunabwehr und einem optimalen Gleichgewicht bei (155, 156). 1,25(OH)2D3 hemmt direkt die B-Zell-Proliferation durch Stabilisierung des Cyclin-abhängigen Kinase-Inhibitors p27 (157). Es hemmt auch die Differenzierung von „Post-Switch“-Gedächtnis-B-Zellen und Plasmazellen und reduziert die Immunglobulinproduktion und -sekretion, z. B. durch Hemmung der CD40-Signalgebung (56, 157, 158), insbesondere von IgE (158). 1,25(OH)2D3 fördert die B-Lymphozyten-Apoptose, die IL-10-Sekretion und die Expression von CCR10 (56, 157). Von Bedeutung ist, dass über mehrere Arten von Wechselwirkungen zwischen B-Zellen und invarianten NK-T-Zellen berichtet wurde. Erstens unterstützen invariante NK-T-Zellen die B-Zell-Antikörperproduktion und die Proliferation von Gedächtnis-B-Zellen, sogar ohne CD4--T-Zell-Hilfe (159). Zweitens reduzieren invariante NK-T-Zellen die Proliferation und fördern die Apoptose von selbstreaktiven, CD1d- und IL-18--exprimierenden Marginalzonen-B-Zellen (MZBs) der Milz, die ein angeborenes Autoimmunpotential besitzen (160-163). Drittens verstärken invariante NK-T-Zellen die Proliferation von immunregulatorischen follikulären B-Zellen (162), während umgekehrt MZBs und DCs invariante NK-T-Zellen aktivieren (164). Zusätzlich scheint eine hohe Oberflächenexpression von CD1d auf unreifen B-Zellen essentiell für die Proliferation und Differenzierung von invarianten NK-T-Zellen (165). Patienten mit systemischem Lupus erythematodes (SLE) haben einen B-Zell-spezifischen subzellulären Transportdefekt von CD1d, der reduzierte Mengen an Oberflächen-CD1d verursacht. Sie haben auch eine verringerte Anzahl unveränderlicher NK-T-Zellen mit verringerter IL-2-Stimulation und verringerter IFN- und TNF-Sekretion, während die IL-10-Sekretion erhöht ist (165). Dieser Transportdefekt wurde bei anderen Immunzellen nicht gefunden. Ein intrinsischer invarianter NK-T-Zell-Defekt wurde in diesen Experimenten ausgeschlossen. Aus unbekannten Gründen konnte eine normale CD1d-Oberflächenexpression auf anderen Zelltypen, wie z. B. kortikalen Thymozyten, Lymphknotenmantelzone und Milz-MZBs, und ruhenden Monozyten diesen SLE-spezifischen intrinsischen B-Zell-Defekt nicht kompensieren (165). Interessanterweise zeigten Patienten mit SLE, die auf eine Behandlung mit Rituximab ansprachen, wiederhergestellte CD1d-Eigenschaften in unreifen CD1dhi-B-Zellen und eine Normalisierung der Anzahl, Aktivierung und Funktion von invarianten NK-T-Zellen (165).
Diskussion
Wie hier gezeigt, sind Vitamin-D3-Spiegel, Metabolismus und physiologische Immunreaktivität eng miteinander verbunden. Unzureichende Spiegel und Aktivitäten von D3 können eine Fehlregulation des Immunsystems verursachen, was zu verschiedenen Krankheiten führt und den Verlauf einer Vielzahl von Krankheiten negativ beeinflussen kann. Erste Symptome niedriger 25OHD3-Spiegel sind intermittierende Müdigkeit und wiederkehrende Infektionen, die saisonal oder nach dem Urlaub abklingen. Im Laufe der Zeit kann sich schleichend ein chronisches Erschöpfungssyndrom entwickeln, das typischerweise durch stressige und erschöpfende Lebensbedingungen, Infektionen, traumatische oder toxische Verletzungen gefördert wird. Merkmale des chronischen Erschöpfungssyndroms/Myalgie
Enzephalopathie (CFS/ME) sind schwere und beeinträchtigende Erschöpfung, Fieberfreiheit trotz allgemeinem Unwohlsein, das einem akuten Infekt ähnelt, und anstrengungsbedingte Verschlimmerung von Funktionsbeeinträchtigungen, sowie viele weitere Symptome, insbesondere generalisierte Schmerzen, Schlafstörungen und Magen-Darm-Beschwerden. Offensichtliche Organschäden fehlen, während reaktive depressive Symptome überwiegen. Symptomverschiebungen hin zu Fibromyalgie (FMS) scheinen mit zunehmendem Alter die Regel zu sein. Typischerweise korreliert FMS mit chronischen Skeletterkrankungen mit geringer Entzündungsaktivität und neuropathischen Schmerzen. Dennoch erwerben viele Menschen kein CFS/ME oder FMS. Sie leiden an eindeutigen Krankheiten, die angeblich durch Vitamin-D3-Mangel oder -Insuffizienz ausgelöst werden sollen. Üblicherweise begleitet lähmende Erschöpfung chronische Entzündungs- und Autoimmunerkrankungen sowie Krebs, wohingegen Patienten mit chronischer Gewebedegeneration von einer weniger schweren Erschöpfung berichten. Schwere chronische Müdigkeit wurde auch bei psychiatrischen Erkrankungen beobachtet. Oft betrachten Patienten Müdigkeit als das am stärksten beeinträchtigende unter allen anderen Krankheitssymptomen. Obwohl es Hinweise darauf gibt, dass ein niedriger 25OHD3 chronische Müdigkeit verursachen kann, würde dies auch durch einen veränderten Lebensstil und ein verändertes Verhalten erklärt werden, insbesondere in Bezug auf Patienten, die depressiv oder erschöpft erscheinen. Außerdem ist die Messung der chronischen Erschöpfung höchst subjektiv.
Allerdings ist die Diagnose Depression oder Erschöpfung auch subjektiv, insbesondere wenn die Differenzialdiagnose CFS/FMS oder FMS nicht berücksichtigt wird. Bei chronisch entzündlichen, Autoimmun- oder bösartigen Erkrankungen hingegen schätzen Mediziner Fatigue zweifellos als krankheitsbedingt ein. Um das übliche Vorurteil gegen chronische Erschöpfung zu überwinden, sollte berücksichtigt werden, dass Entzündungen nicht nur Ermüdung, sondern auch eine Veränderung der mitochondrialen Funktion, der Auto-/Xenophagie oder der Erregungs-Stoffwechsel-Kopplung aufgrund verringerter subzellulärer Calciumspeicher hervorrufen können (22, 166, 167). Glücklicherweise erkennen immer mehr Autoren die Bedeutung von Vitamin D für die Immunregulation an (168-180). Epidemiologische Studien berichten von einer Korrelation zwischen einem unzureichenden 25OHD3-Spiegel und mehreren Immunerkrankungen wie chronischen Lungeninfektionen (168-170), Multipler Sklerose (171-174), SLE (175, 180), Diabetes und Herz-Kreislauf-Erkrankungen Krankheiten (22, 176) und Krebs (7, 177-179). Darüber hinaus wurden niedrige 25OHD3-Spiegel und eine erhöhte Immunreaktivität gegen das Epstein-Barr-Virus vor dem Ausbruch der Multiplen Sklerose festgestellt (171), und eine Hochregulierung von VDR und CYP27B1 wurde in aktiven Läsionen festgestellt (174). Niedrige 25OHD3-Spiegel korrelierten auch mit dem Wiederauftreten von entzündlichen Wirbelsäulenläsionen (172) und einem verringerten Überleben bei Eierstockkrebs (179). Es wurde festgestellt, dass genetische Variationen in Enzymen des Vitamin-D-Signalwegs das Risiko für Multiple Sklerose (173) und differenziertes Schilddrüsenkarzinom (178) erhöhen. Niedrige 25OHD3-Spiegel waren auch bei Patienten mit FMS und CFS weit verbreitet (2, 6, 8, 9, 11, 12, 14, 15). Im Gegensatz zu diesen epidemiologischen Studien sind Interventionsstudien noch selten und klein. Nach einjähriger Behandlung mit 2,000 IE (50 ug)/Tag Cholecalciferol verbesserten sich die Entzündungs- und hämostatischen Marker und die Krankheitsaktivität bei SLE (180).

Das ist unser Produkt gegen Ermüdung! Klicken Sie auf das Bild für weitere Informationen!
Eine Dosis von 800 IE (20 ug) Cholecalciferol/Tag, angewendet für 2,5-10 Monate, verbesserte die Müdigkeit bei Patienten mit Myasthenia gravis (10). Die Rehabilitationsergebnisse verbesserten sich nach einer Vitamin-D-Ergänzung bei Patienten mit mehreren Erkrankungen (16). 4,000 I.E. (100 μcg) Cholecalciferol/Tag für ein Jahr reduzierte wiederkehrende Infektionen der Atemwege signifikant (169). Wichtig ist, dass eine Pilotstudie eine deutlich verbesserte mitochondriale oxidative Funktion nach Normalisierung der 25OHD3-Spiegel bei 12 Patienten mit schwerem Vitamin-D3--Mangel mit chronischer Müdigkeit und Myopathie zeigte (166). Große Interventionsstudien und eindeutige Beweise für den Nutzen einer Vitamin-D3-Behandlung fehlen jedoch noch. Ein Grund für die offensichtliche Zurückhaltung, größere Interventionsstudien durchzuführen, könnte die anhaltende Debatte und allgemeine Unsicherheit über Dosierungen und mögliche Nebenwirkungen der Vitamin-D3-Behandlung sein. Eine rechtzeitige Diagnose eines zugrundeliegenden Vitamin-D3-Mangels oder einer Vitamin-D3-Insuffizienz und eine angemessene Behandlung, selbst im Stadium unerklärlicher chronischer Müdigkeit, sind gerechtfertigt. Die Messung des Blutspiegels der Vorstufe 25OHD3 ist einfach und kostengünstig. Im Gegensatz dazu weist ein erhöhter Spiegel des aktiven Metaboliten 1,25(OH)2D3 nicht auf eine Vitamin-D-Suffizienz hin, könnte aber ein wichtiger Hinweis auf einen Kalziummangel sein, der vermutlich mit einer Autoimmunität einhergeht (2).
Ausreichend ist definiert als 25OHD3-Spiegel über 30-100 ng/ml (75-250 nmol/l). Werte von 10-30 ng/ml (25-75 nmol/l) weisen auf eine Insuffizienz hin, Werte unter 10 ng/ml (25 nmol/l) auf einen eindeutigen Mangel. Die Therapie ist ebenso einfach. Cholecalciferol kann oral verabreicht werden, und eine kontinuierliche tägliche Substitution wird empfohlen. Die therapeutische Dosis reicht von 4,000 bis 10,000 IE (100-250 ug)/Tag. Höhere Dosen von etwa 10,000 IE/Tag und eine gleichzeitige Substitution von Mineralstoffen oder anderen Co-Faktoren sind gerechtfertigt, um eine eventuelle Vitamin-D3-Resistenz, wie z. B. bei Kalziummangel, zu überwinden. Im Gegensatz zu Medikamenten, die üblicherweise bei chronisch entzündlichen, Autoimmun- oder bösartigen Erkrankungen empfohlen werden, ist Cholecalciferol sehr preiswert. Eine frühzeitige Behandlung von chronischer Müdigkeit und wiederkehrenden Infektionen könnte ein ausgewachsenes CFS/ME verhindern. Die Erhöhung der 25OHD3-Spiegel in den frühen Stadien der Erkrankung kann den Verlauf verbessern und die für die Induktionstherapie erforderliche Zeit verkürzen, wodurch die Gesamtbehandlungskosten gesenkt werden. Schädliche, oft lebensbedrohliche Nebenwirkungen moderner biologischer, zytostatischer oder immunsuppressiver Verbindungen können vermieden oder zumindest reduziert werden. Die Rückfallhäufigkeit und die Behandlungsresistenz können ebenso wie die Krankheitslast und die Therapiekosten sinken. Der Nutzen und die Kosteneffizienz einer Vitamin-D3-Co-Behandlung bedürfen jedoch weiterer Untersuchungen durch leistungsstarke und sorgfältig konzipierte klinische Studien.
Verweise
1. Adams JS, Ren S, Liu PT, Chun RF, Lagishetty V, Gombart AF, Borregaard N, Modlin RL und Hewison M: Vitamin D zur Verteidigung der menschlichen Immunantwort. Ann NY Acad Sci 1117: 94-105, 2007.
2 Blaney GP, Albert PJ und Proal AD: Vitamin-D-Metaboliten als klinische Marker bei Autoimmun- und chronischen Erkrankungen. Ann NY Acad Sci 1173: 384-390, 2009.
3 Bruce D, Yu S, Ooi JH und Cantorna MT: Konvergierende Signalwege führen zu einer Überproduktion von IL-17 in Abwesenheit von Vitamin-D-Signalen. Int. Immunol. 23(8): 519-528, 2011.
4 Hepburn AL: Zöliakie bei Erwachsenen: Rheumatische Präsentationen sind häufig. BMJ 335(7621): 627, 2007.
5 Hewison M: Vitamin D und das Immunsystem: Neue Perspektiven auf ein altes Thema. Endocrinol Metab Clin North Am 39(2): 365-379, 2010.
6 Holick MF und Chen TC: Vitamin-D-Mangel: Ein weltweites Problem mit gesundheitlichen Folgen. Am J Clin Nutr 87(4): 1080S-1086S, 2008.
7 Dev R, Del Fabbro E, Schwartz GG, Hui D, Palla SL, Gutierrez N und Bruera E: Vorläufiger Bericht: Vitamin-D-Mangel bei fortgeschrittenen Krebspatienten mit Symptomen von Müdigkeit oder Anorexie. Onkologe 16(11): 1637-1641, 2011.
8 Antiel RM, Caudill JS, Burkhardt BE, Brands CK und Fischer PR: Eiseninsuffizienz und Hypovitaminose D bei Jugendlichen mit chronischer Müdigkeit und orthostatischer Intoleranz. South Med J 104(8): 609-611, 2011.
9 Berkovitz S, Ambler G, Jenkins M und Thurgood S: Serum-25--Hydroxyvitamin-D-Spiegel bei chronischem Müdigkeitssyndrom: Eine retrospektive Umfrage. Int J Vitam Nutr Res 79(4): 250-254, 2009.
10 Askmark H, Haggård L, Nygren I und Punga AR: Vitamin-D-Mangel bei Patienten mit Myasthenia gravis und Verbesserung der Müdigkeit nach Supplementierung von Vitamin D3: Eine Pilotstudie. Eur J Neurol 19(12): 1554-1560, 2012.
11 Gerwin RD: Eine Übersicht über myofasziale Schmerz- und Fibromyalgiefaktoren, die ihre Persistenz fördern. Acupunct Med 23(3): 121-134, 2005.
12 Höck AD. Zweiwertige Kationen, Hormone, Psyche und Soma: Vier Fallberichte. In: Chronisches Erschöpfungssyndrom. Kritische Bewertungen und klinische Fortschritte. De Meileir K. und Patarca-Montero R. (Hrsg.) New York, Haworth Medical Press. S. 117-131, 2000. 13 Hoskin L, Clifton-Bligh O, Hansen R, Fulcher G und Gates F: Knochendichte und Körperzusammensetzung bei jungen Frauen mit chronischer Müdigkeit. Ann NY Acad Sci 904: 625-627, 2000.
14 Knutsen KV, Brekke M, Gjelstad S und Lagerløv P: Vitamin-D-Status bei Patienten mit muskuloskelettalen Schmerzen, Müdigkeit und Kopfschmerzen: Eine beschreibende Querschnittsstudie in einer multiethnischen Allgemeinpraxis in Norwegen. Scand J Prim Health Care 28: 166-171, 2010.
15 McCarty DE: Auflösung von Hypersomnie nach Erkennung und Behandlung von Vitamin-D-Mangel. J Clin Sleep Med 6(6): 605-608, 2010.
16 Shinchuk LM und Holick MF: Vitamin D und Rehabilitation: Verbesserung der funktionellen Ergebnisse. Nutr Clin Pract 22(3): 297-304, 2007.
17 Adams JS und Hewison M: Update in Vitamin D. J Clin Endocrinol Metab 95: 471-478, 2010.
18 Christakos S, Dhawan P, Porta A, Mady LJ und Seth T: Vitamin D und intestinale Kalziumabsorption. Mol Cell Endocrinol 347(1-2): 25-29, 2011.
19 Chun RF, Adams JS und Hewison M: Back to the future: A new look at 'old' vitamin D. J Endocrinol 198(2): 261-269, 2008.
20 Haussler MR, Whitfield GK, Haussler CA, Hsieh JC und Jurutka PW. Nuklearer Vitamin-D-Rezeptor: natürliche Liganden, molekulare Strukturfunktion und transkriptionelle Kontrolle lebenswichtiger Gene. In: Vitamin D. Dritte Auflage. Feldman D, Pike JW und Adams JS (Hrsg.). New York, Academic Press, S. 137-170, 2011.
21 Morris HA und Anderson PH: Autokrine und parakrine Wirkungen von Vitamin D. Clin Biochem Rev 31: 129-138, 2010.
22 Peterlik M und Cross HS: Durch Vitamin D und Kalziummangel bedingte chronische Erkrankungen: Molekulare und zelluläre Pathophysiologie. Eur J Clin Nutr 63(12): 1377-1386, 2009.
23 Mizwicki MT und Norman AW. Vitamin-D-Sterol/VDR-Konformationsdynamik und nichtgenomische Wirkungen. In: Vitamin D. Dritte Auflage. Feldman D, Pike JW und Adams JS (Hrsg.). New York, Academic Press, S. 271-297, 2011.
24 Norman AW: Kurzrezension: Neue Aufgaben für einen bereits beschäftigten Empfänger. Endokrinologie 147(12): 5542-5548, 2006.
25 Pike JW und Meyer MB: Der Vitamin-D-Rezeptor: Neue Paradigmen für die Regulation der Genexpression durch 1,25-Dihydoxyvitamin D3. Rheum Dis Clinic North Am 38(1): 13-27, 2012.
26 Hewison M: Vitamin D und die Intrakrinologie der angeborenen Immunität. Mol Cell Endocrinol 321(2): 103-111, 2010.
27 Kamen DL: Vitamin D und molekulare Wirkungen auf das Immunsystem: Modulation der angeborenen und Autoimmunität. J Mol Med (Berl) 88(5): 441-450, 2010.
28 Liu PT: Die Rolle von Vitamin D bei der angeborenen Immunität: antimikrobielle Aktivität, oxidativer Stress und Barrierefunktion. In: Vitamin D. Dritte Auflage. Feldman D, Pike JW und Adams JS (Hrsg.) New York, Academic Press, S. 1811-1823, 2011.
29 Weiß JH. Vitamin D und angeborene Immunität. In: Vitamin D. Dritte Auflage. Feldman D, Pike JW und Adams JS (Hrsg.). New York, Academic Press, S. 1777-1787, 2011.
30 H. Fujita, K. Sugimoto, S. Inatomi, T. Maeda, M. Osanai, Y. Uchiyama, Y. Yamamoto, T. Wada, T. Kojima, H. Yokozaki, T. Yamashita, S. Kato, N. Sawada und H. Chiba: Tight Junction Proteins Claudin{{1 }} und -12 sind entscheidend für die Vitamin-D-abhängige Ca2-Plus-Absorption zwischen Enterozyten. Mol Biol Cell 19(5): 1912-1921, 2008.
31 Kong J, Zhang Z, MW Musch, G Ning, J Sun, J Hart, M Bissonnette und YC Li: Neuartige Rolle des Vitamin-D-Rezeptors bei der Aufrechterhaltung der Integrität der Darmschleimhautbarriere. Am J Physiol Gastrointest Liver Physiol 294(1): G208-G216, 2008.
32 Sun J: Vitamin D und Immunfunktion der Schleimhaut. Curr Opin Gastroenterol 26(6): 591-595, 2010.
33 Ramot Y, Paus R, Tiede S und Zlotogorsky A: Endocrine controls of keratin expression. Biotests 31(4): 389-399, 2009.
34 Zbytek B, Janjetovic Z, Tuckey RC, Zmijewski MA, Sweatman TW, Jones E, Nguyen MN und Slominski AT: 20-Hydroxyvitamin D3, ein Produkt der Vitamin-D3-Hydroxylierung durch Cytochrom P450scc, stimuliert die Keratinozytendifferenzierung. J Invest Dermatol 128(9): 2271-2280, 2008.
35 Miodovnik M, Koren R, Ziv E und Ravid A: Die Entzündungsreaktion von Keratinozyten und ihre Modulation durch Vitamin D: Die Rolle von MAPK-Signalwegen. J Cell Physiol 227(5): 2175- 2183, 2012.
36 Bahar-Shany K, Ravid A und Koren R: Up-regulation of MMP- 9 productions by TNF in keratinocytes and its attenuation by vitamin D. J Cell Physiol 222(3): 729-737, 2010 .
37 Langberg M, Rotem C, Fenig E, Koren R und Ravid A: Vitamin D schützt Keratinozyten vor schädlichen Wirkungen ionisierender Strahlung. Br J Dermatol 160(1): 151-161, 2009.
38 Diker-Cohen T, Koren R und Ravid A: Programmierter Zelltod gestresster Keratinozyten und seine Hemmung durch Vitamin D: Die Rolle von Todes- und Überlebenssignalwegen. Apoptose 11(4): 519-534, 2006.
39 Koren R, Liberman UA, Maron L, Novogrodsky A und Ravid A: 1,25-Dihydroxyvitamin D3 wirkt direkt auf menschliche Lymphozyten und stört die zelluläre Antwort auf Interleukin-2. Immunopharmacology 18(3): 187-194, 1989.
40 Gombart AF: Der Vitamin-D-antimikrobielle Peptidweg und seine Rolle beim Schutz vor Infektionen. Future Microbiol 4(9): 1151-1165, 2009.
41 Agerberth B., Charo J., Werr J., Olsson B., Idali F., Lindbom L., Kiessling R., Jörnvall H., Wigzell H. und Gudmundsson GH: Die humanen antimikrobiellen und chemotaktischen Peptide LL-37 und Alpha-Defensine werden exprimiert durch spezifische Lymphozyten- und Monozytenpopulationen. Blut 96(9): 3086-3093, 2000.
42 Alalwani SM, Sierigk J, Herr C, Pinkenburg O, Gallo R, Vogelmeier C und Bals R: Das antimikrobielle Peptid LL-37 moduliert die Entzündungs- und Wirtsabwehrreaktion menschlicher Neutrophiler. Eur J Immunol 40(4): 1118-1126, 2010.
43 Cederlund A, Gudmundsson GH und Agerberth B: Antimikrobielle Peptide wichtig für die angeborene Immunität. FEB J 278(20): 3942-3951, 2011.
44 Kai-Larsen Y und Agerberth B: Die Rolle des multifunktionellen Peptids LL-37 in der Wirtsabwehr. Front Biosci 13: 3760-3767, 2008.
45 Yang D, Chertov O und Oppenheim JJ: Die Rolle von antimikrobiellen Peptiden und Proteinen bei Säugetieren beim Erwachen der angeborenen Wirtsabwehr und der adaptiven Immunität. Cell Mol Life Sci 58(7): 978- 989, 2001.
46 Allaker RP: Wirtsabwehrpeptide_Eine Brücke zwischen der angeborenen und der adaptiven Immunantwort. Trans R Soc Trop Med Hyg 102(1): 3-4, 2008.
47 Bowdish DM, Davidson DJ und Hancock RE: Immunomodulatory properties of defensins and cathelicidins. Curr Top Microbiol Immunol 306: 27-66, 2006.
48 Büchau AS, Morizane S, Trowbridge J, Schauber J, Kotol P, Bui JD und Gallo RL: Das Wirtsverteidigungspeptid Cathelicidin ist für die NK-Zell-vermittelte Unterdrückung des Tumorwachstums erforderlich. J Immunol 184(1): 369-378, 2010.
49 Campbell GR und Spector SA: Autophagy induction by vitamin D inhibits both Mycobacterium tuberculosis and human immunodeficiency virus type 1. Autophagy 8(10): 1523-1525, 2012.
50 Di Rosa M, Malaguarnera M, Nicoletti F und Malaguarnera L: Vitamin D3: Ein hilfreicher Immunmodulator. Immunologie 134(2): 123-139, 2011.
51 McGillivray SM, Ebrahimi CM, Fisher N, Sabet M, Zhang DX, Chen Y, Haste NM, Aroian RV, Gallo RL, Guiney DG, Friedlander AM, Koehler TM und Nizet V: ClpX trägt zur angeborenen Abwehrpeptidresistenz und Virulenz bei Phänotypen von Bacillus anthracis. J Angeborenes Immunsystem (5): 494-506, 2009.
52 Fabri M, Stenger S, Shin DM, Yuk JM, Liu PT, Realegeno S, Lee HM, Krutzik SR, Schenk M, Sieling PA, Teles R, Montoya D, Iyer SS, Bruns H, Lewinsohn DM, Hollis BW, Hewison M, Adams JS, Steinmeyer A, Zügel U, Cheng G, Jo EK, Bloom BR und Modlin RL: Vitamin D is required for IFN- -mediated antimicrobial activity of human macrophages. Sci Transl Med 3(104): 104ra102, 2011.
53 G. Boltz-Nitulescu, M. Willheim, A. Spittler, F. Leutmezer, C. Tempfer und S. Winkler: Modulation der IgA-, IgE- und IgG-Fc-Rezeptorexpression auf humanen mononukleären Phagozyten durch 1 , 25- Dihydroxyvitamin D3 und Zytokine. J. Leukoc Biol. 58(2): 256-262, 1995.
54 Maliszewski CR, Shen L und Fanger MW: Die Expression von Rezeptoren für IgA auf menschlichen Monozyten und mit Calcitriol behandelten HL-60-Zellen. J Immunol 135(6): 3878-3881, 1985.
55 Shen L, Maliszewski CR, Rigby WF und Fanger MW: IgA-vermittelte Effektorfunktion von HL-60-Zellen nach Behandlung mit Calcitriol. Mol Immunol 23(6): 611-618, 1986.
56 Adorini L: Kontrolle der adaptiven Immunität durch Vitamin-D-Rezeptoragonisten. In: Vitamin D. Dritte Auflage. Feldman D, Pike JW und Adams JS (Hrsg.). New York, Academic Press, S. 1789-1809, 2011.
57 Shirakawa AK, Nagakubo D, Hiroshima K, Nakayama T, Jin Z und Yoshie O: 1,25-Dihydroxyvitamin D3 induziert die CCR10-Expression in sich in der Endphase differenzierenden menschlichen B-Zellen. J Immunol 180(5): 2786-2795, 2008.
58 Deretic V und Levine B: Autophagie, Immunität und mikrobielle Anpassungen. Cell Host Microbe 5(6): 527-549, 2009.
59 Deretic V: Autophagie als Paradigma der angeborenen Immunität: Erweiterung des Anwendungsbereichs und Repertoires von Mustererkennungsrezeptoren. Curr Opin Immunol 24(1): 21-31, 2012.
60 Kroemer G, Mariño G und Levine B: Autophagy and the integrated stress response. Mol Cell 40(2): 280-293, 2010.
61 Mehrpour M, Esclatine A, Beau I und Codogno P: Autophagy in health and disease. 1. Regulation und Bedeutung der Autophagie: Ein Überblick. Am J Physiol Cell Physiol 298: C776-C785, 2010.
62 Oh JE und Lee HK: Autophagie bei der angeborenen Erkennung von Krankheitserregern und der adaptiven Immunität. Yonsei Med J 53(2): 241- 247, 2012.
63 Levine B und Kroemer G: Autophagy in the pathogenesis of the disease. Zelle 132(1): 27-42, 2008.
64 Wu S und Sun J: Vitamin D, Vitamin-D-Rezeptor und Makroautophagie bei Entzündungen und Infektionen. Discov Med 11(59): 325-335, 2011.
65 Choi AMK, Ryter SW und Levine B: Autophagy in human health and disease. N Engl J Med 368(7): 651-661, 2013. 66 Høyer-Hansen M, Bastholm L, Mathiasen IS, Elling F and Jäättelä M: Vitamin D analog EB1089 triggers dramatische lysosomal changes and beclin 1- vermittelter autophagischer Zelltod. Zelltod-Differenzierung 12: 1297-1309, 2005.
67 Høyer-Hansen M: AMP-aktivierte Proteinkinase. Ein universeller Regulator der Autophagie. Autophagie 3(4): 381-383, 2007.
68 Glick D, Barth S und Macleod KF: Autophagie: Zelluläre und molekulare Mechanismen. J Pathol 221(1): 3-12, 2010.
69 He MX, MacLeod IX, Jia W und He YW: Macroautophagy in T lymphocyte development and function. Front Immunol. 3: 22, 2012
70 Legion LA, Temime-Smaali N und Lafont F: Ubiquitylierung und Autophagie bei der Kontrolle bakterieller Infektionen und damit verbundener Reaktionen. Cell Microbiol 13(9): 1303-1311, 2011.
71 Nedjic J, Aichinger M und Klein L: Autophagy and T cell education in the thymus: Iss dich selbst, um dich selbst zu kennen. Zellzyklus 7(23): 3625-3628, 2008.
72 Winiarska M., Bil J., Nowis D. und Golab J.: Proteolytische Wege, die an der Modulation von CD20-Spiegeln beteiligt sind. Autophagie 6(6): 810- 812, 2010.
73 Travassos LH, Carneiro LA, Girardin S und Philpott DJ: Nod-Proteine verknüpfen bakterielle Wahrnehmung und Autophagie. Autophagie 6(3): 409-411, 2010.
74 Z. Hmama, K. Sendide, A. Talal, R. Garcia, K. Dobos und NE Reiner: Quantitative Analyse der Phagolysosomenfusion in intakten Zellen: Hemmung durch mycobakterielles Lipoarabinomannan und Rettung durch ein 1 ,25-Dihydroxyvitamin D{{3} }Phosphoinositid-3--Kinase-Weg. J Cell Sci 117: 2131-2139, 2004.
75 Yuk JM, Shin DM, Lee HM, Yang CS, Jin HS, Kim KK, Lee ZW, Lee SH, Kim JM und Jo EK: Vitamin D3 induces autophagy in human monocytes/macrophages via cathelicidin. Cell Host Microbe 6(3): 231-243, 2009.
76 Wang J: Beclin 1 überbrückt Autophagie, Apoptose und Differenzierung. Autophagie 4(7): 947-948, 2008.
77 Liang C: Negative Regulation der Autophagie. Cell Death Differ 17(12): 1807-1815, 2010.
78 Chandra G, Selvaraj P, Jawahar MS, Banurekha VV und Narayanan PR: Effect of vitamin D3 on the phagocytic potential of macrophages with live Mycobacterium tuberculosis and lymphoproliferative response in pulmonary tuberculosis. J. Clin. Immunol. 24(3): 249-257, 2004.
79 Abu-Amer Y und Bar-Shavit Z: Beeinträchtigte Makrophagen-Differenzierung aus dem Knochenmark bei Vitamin-D-Mangel. Cell Immunol 151(2): 356-368, 1993.
80 H. Korf, M. Wines, B. Stijlemans, T. Takaishi, S. Robert, M. Miani, DL Eizirik, C. Gysemans und C. Mathieu: 1,25-Dihydroxyvitamin D3 hemmt die entzündliche und T-Zell-stimulierende Kapazität von Makrophagen durch einen IL-10--abhängigen Mechanismus. Immunbiologie 217(12): 1292-1300, 2012.
81 Tokuda N und Levy RB: 1,25-Dihydroxyvitamin D3 stimuliert die Phagozytose, unterdrückt aber die HLA-DR- und CD13-Antigenexpression in menschlichen mononukleären Phagozyten. Proc Soc Exp Biol Med 211(3): 244-250, 1996.
82 Zughaier SM, Shafer WM und Stephens DS: Antimikrobielle Peptide und Endotoxin hemmen die Zytokin- und Stickoxidfreisetzung, verstärken aber die respiratorische Burst-Reaktion in menschlichen und murinen Makrophagen. Cell Microbiol 7(9): 1251-1262, 2005.
83 Blanco P, Palucka AK, Pascual V und Banchereau J: Dendritische Zellen und Zytokine bei menschlichen Entzündungs- und Autoimmunerkrankungen. Cytokine Growth Factor Rev. 19(1): 41-52, 2008.
84 Kushwa R und Hu J: Role of dendritic cells in the induction of regulator T-cells. Cell Biosci 1(1): 20, 2011.
85 R. M. Steinman, D. Hawiger, K. Liu, L. Bonifaz, D. Bonnyay, K. Mahnke, T. Iyoda, J. Ravetch, M. Dhodapkar, K. Inaba und M. Nussenzweig: Dendritische Zellfunktion in vivo während des Steady State: Eine Rolle bei der peripheren Toleranz. Ann NY Acad Sci 987: 15-25, 2003.
86 Singh VK, Mehrotra S und Agarwal SS: Das Paradigma der Th1- und Th2-Zytokine. Seine Bedeutung für Autoimmunität und Allergie. Immunol Res 20: 147-161, 1999.
87 Alberts B., Johnson A., Lewis J., Raff M., Roberts K. und Walter P. Das adaptive Immunsystem. In: Molekularbiologie der Zelle. Anderson M und Granum S (Hrsg.). New York, Garland Science, S. 1539-1601, 2008.
88 Canning MO, Grotenhuis K., de Wit H., Ruwhof C. und Drexhage HA: 1- ,25-Dihydroxyvitamin D3 (1,25(OH)(2)D(3)) hemmt die Reifung von voll aktive unreife dendritische Zellen aus Monozyten. Eur J Endocrinol 145(3): 351-357, 2001.
89 Adler HS und Steinbrink K: Tolerogene dendritische Zellen in Gesundheit und Krankheit: Freund und Feind! Eur J Dermatol 17(6): 476- 491, 2007.
90 Sloka S, Silva C, Wang J und Yong VW: Prädominanz der Th2-Polarisation durch Vitamin D durch einen STAT6--abhängigen Mechanismus. J Neuroinflammation 8: 56, 2011.
91 Jeffery LE, Burke F, Mura M, Zheng Y, Qureshi OS, Hewison M, Walker LSK, Lammas DA, Raza K und Sansom DM: 1,25- Dihydroxyvitamin D3 und Interleukin-2 verbinden sich zu hemmen die T-Zell-Produktion von entzündlichen Zytokinen und fördern die Entwicklung regulatorischer T-Zellen, die CTLA-4 und FOXP3 exprimieren. J Immunol 183(9): 5458-5467, 2009.
92 Afzali B, Mitchell P, Lechler RI, John S und Lombardi G: Translational mini-review series on Th17 cells: Induction of interleukin-17 production by regulator T-cells. Clin Exp Immunol 159(2): 120-130, 2010.
93 Prietl B, Pilz S, Wolf M, Tomaschitz A, Obermayer-Pietsch B, Graninger W und Pieber TR: Vitamin-D-Supplementierung und regulatorische T-Zellen bei scheinbar gesunden Probanden: Vitamin-D-Behandlung bei Autoimmunerkrankungen? Isr Med Assoc J 12(3): 136-139, 2010.
94 Peterson RA: Regulatorische T-Zellen: verschiedene Phänotypen, die integraler Bestandteil der Immunhomöostase und -unterdrückung sind. Toxicol Pathol 40(2): 186-204, 2012.
95 Schmidt SV, Nino-Castro AC und Schultze JL: Regulatorische dendritische Zellen: Es gibt mehr als nur eine Immunaktivierung. Front Immunol. 3: 274, 2012.
96 K. Mahnke, S. Ring, T. Bedke, S. Karakhanova und AH Enk: Interaktion regulatorischer T-Zellen mit antigenpräsentierenden Zellen bei Gesundheit und Krankheit. Chem Immunol Allergy 94: 29-39, 2008.
97 Kreindler JL, Steele C, Nguyen N, Chan YR, Pilewski JM, Alcorn JF, Vyas YM, Aujla SJ, Finelli P, Blanchard M, Zeigler SF, Logar A, Hartigan E, Kurs-Lasky M, Rockette H, Ray A und Kolls JK: Vitamin D3 dämpft die Th2-Antworten auf Aspergillus fumigatus, die von CD4 plus T-Zellen von Mukoviszidose-Patienten mit allergischer bronchopulmonaler Aspergillose aufgebaut werden. J Clin Invest 120(9): 3242-3254, 2010.
98 von Essen MR, Kongsbak M, Schjerling P, Olgaard K, Odum N und Geisler C: Vitamin D steuert die T-Zell-Antigenrezeptor-Signalübertragung und Aktivierung menschlicher T-Zellen. Nat Immunol 11(4): 344-349, 2010.
99 Willheim M, Thien R, Schrattbauer K, Bajna E, Holub M, Gruber R, Baier K, Pietschmann P, Reinisch W, Scheiner O und Peterlik M: Regulatory effects of 1 ,25-Dihydroxyvitamin D3 on the cytokine production menschlicher peripherer Blutlymphozyten. J Clin Endocrinol Metab 84(10): 3739-3744, 1999.
100 Cantorna MT: Warum exprimieren T-Zellen den Vitamin-D-Rezeptor? Ann NY Acad Sci 1217: 77-82, 2011.
101 Chang SH, Chung Y und Dong C: Vitamin D unterdrückt die Produktion von Th17-Zytokinen, indem es die Expression von homologem C/EBP-Protein (CHOP) induziert. J. Biol. Chem. 285(50): 38751-3855, 2010.
102 Joshi S, Pantalena LC, Liu XK, Gaffen SL, Liu H, RohowskyKochan C, Ichiyama K, Yoshimura A, Steinman L, Christakos S und Youssef S: 1,25-Dihydroxyvitamin D(3) verbessert die Th17-Autoimmunität über transkriptionelle Modulation von Interleukin- 17A. Mol Cell Biol 31(17): 3653-3669, 2011.
103 Dimeloe S, Richards DF, Urry ZL, Gupta A, Stratigou V, Farooque S, Saglani S, Bush A und Hawrylowicz CM: 1 ,25- Dihydroxyvitamin D3 fördert die CD200-Expression durch menschliche periphere und in den Atemwegen befindliche T-Zellen . Thorax 67(7): 574-581, 2012. 104 Enioutina EY, Bareyan D und Daynes RA: TLR-Liganden, die den Metabolismus von Vitamin D3 in aktivierten murinen dendritischen Zellen stimulieren, können als wirksame Schleimhautadjuvantien für subkutan verabreichte Impfstoffe fungieren. Impfstoff 26(5): 601-613, 2008.
105 Ivanov AP, Dragunsky EM und Chumakov KM: 1,25- Dihydroxyvitamin D3 verstärkt die systemische und mukosale Immunantwort auf inaktivierten Poliovirus-Impfstoff bei Mäusen. J Infect Dis 193(4): 598-600, 2006.
106 Yu S, Bruce D, Froicu M, Weaver V und Cantorna MT: Fehler beim T-Zell-Homing, reduzierte intraepitheliale CD4/CD8-Lymphozyten und Entzündung im Darm von Vitamin-D-Rezeptor-KO-Mäusen. Proc Natl Acad Sci USA 105(52): 20834-20839, 2008. 107 Kim SY, Suh HW, Chung JW, Yoon SR und Choi I: Verschiedene Funktionen von VDUP1 bei Zellproliferation, -differenzierung und -krankheiten. Cell Mol Immunol 4(5): 345-351, 2007.
108 Fallarino F. und Grohmann U.: Using an Ancient Tool for Igniting and Propaging Immune Tolerance: IDO as a Inducer and Amplifier of regulator T-cell functions. Curr Med Chem 18(15): 2215-2221, 2011.
109 Delgado M: Generierung tolerogener dendritischer Zellen mit Neuropeptiden. Hum Immunol 70(5): 300-307, 2009.
110 Spadoni I, Iliev ID, Rossi G und Rescigno M: Dendritische Zellen produzieren TSLP, das die Differenzierung von Th17-Zellen einschränkt, die Treg-Entwicklung fördert und vor Colitis schützt. Schleimhaut-Immunol (2): 184-193, 2012.
111 Clark DA: Toleranzsignalmoleküle. Chem Immunol Allergy 89: 36-48, 2005.
112 Strowig T, Brilot F und Münz C: nicht-zytotoxische Funktionen natürlicher Killerzellen: Direkte Pathogenbeschränkung und Unterstützung der adaptiven Immunität. J Immunol 180(12): 7785-7791, 2008.
113 Vivier E, Raulet DH, Moretta A, Caligiuri MA, Zitvogel L, Lanier LL, Yokoyama WM und Ugolini S: Angeborene oder adaptive Immunität? Das Beispiel natürlicher Killerzellen. Wissenschaft 331(6013): 44-49, 2011.
114 Brady J, Carotta S, Thong RP, Chan CJ, Hayakawa Y, Smyth MJ und Nutt SL: Die Wechselwirkungen mehrerer Zytokine kontrollieren die NK-Zellreifung. J Immunol 185(11): 6679-6688, 2010.
115 Souza-Fonseca-Guimaraes F, Adib-Conquy M und Cavaillon JM: Natürliche Killerzellen (NK) bei der antibakteriellen angeborenen Immunität: Engel oder Teufel? Mol Med 18: 270-285, 2010.
116 Walzer T, David M, Robbins SH, Zitvogel L und Vivier E: Natural-killer cells and dendritic cells: „l'union fait la force“. Blut 106(7): 2252-2258, 2005.
117 Ravid A, Koren R, Maron L und Liberman UA: 1,25(OH)2D3 erhöht die Zytotoxizität und Exozytose in Lymphokin-aktivierten Killerzellen. Mol Cell Endocrinol 96(1-2): 133-139, 1993.
118 Zafirova B, Wensveen FM, Gulin M und Polić B: Regulierung der Immunzellfunktion und -differenzierung durch den NKG2D-Rezeptor. Cell Mol Sci 68: 3519-3529, 2011.
119 Jamil KM und Khakoo SI: KIR/HLA-Wechselwirkungen und pathogene Immunität. J Biomed Biotech 2011: 298348, 2011.
120 Ben-Eliyahu S: Können wir wirklich wissen, ob ein Stressor die Aktivität der natürlichen Killerzellen erhöht oder verringert? Brain Behavi Immun 26(8): 1224-1225, 2012.
121 G. Meron, Y. Tishler, L. Shaashua, E. Rosenne, B. Levi, R. Melamed, N. Gotlieb, P. Matzner, L. Gorski und S. Ben-Eliyahu: PGE(2) unterdrückt die NK-Aktivität in vivo direkt und durch Nebennierenhormone: Effekte Dies kann nicht durch eine Ex-vivo-Bewertung der NK-Zytotoxizität widergespiegelt werden. Brain Behav Immun 28: 128- 138, 2013.
122 Lemire JM: Immunmodulatorische Rolle von 1,25-Dihydroxyvitamin D3. J Cell Biochem 49(1): 26-31, 1992.
123 Kaneno R, Duarte AJ und Borelli A: Natürliche Killeraktivität bei der experimentellen privationalen Rachitis. Immunol Lett 81(3): 183- 189, 2002.
124 Leung KH: Hemmung der Zytotoxizität und Differenzierung von menschlichen natürlichen Killerzellen und Lymphokin-aktivierten Killerzellen durch Vitamin D3. Scand J Immunol 30(2): 199-208, 1989.
125 Rebut-Bonneton C und Demignon J: Wirkung von Calcitriol auf die Zytotoxizität von Lymphozyten im peripheren Blut. Biomed Pharmacother 45(8): 369-372, 1991.
126 El-Shazly AE und Lefebvre P: Modulation of NK cell autocrine induced eosinophil chemotaxis by interleukin-induced eosinophil chemotaxis by interleukin-15 and vitamin D3: A possible NKeosinophil crosstalk via IL-8 in the pathophysiology of allergisch Schnupfen. Mediat Inflamm 2011: 373589, 2011.
127 Merino F, Alvarez-Mon M, de la Hera A, Alés JE, Bonilla F und Durantez A: Regulation of natural killer cytotoxicity by 1,25- Dihydroxyvitamin D3. Cell Immunol 118(2): 328-336, 1989.
128 Tamori S, Uchiyama T und Uchino H: 1 ,25-Dihydroxyvitamin D3 verstärkt die Hochregulierung des Interleukin-2-Rezeptors (p55) durch Interleukin-2. Nihon Ketsueki Gakkai Zasshi 52(6): 996- 1003, 1989.
129 Quesada JM, Serrano I, Borrego F, Martin A, Peña J und Solana R: Calcitriol-Effekt auf natürliche Killerzellen von hämodialysierten und normalen Probanden. Calcif Tissue Int 56(2): 113-117, 1995.
130 Garcion E, Sindji L, Leblondel G, Brachet P und Darcy F: 1, 25- Dihydroxyvitamin D3 reguliert die Synthese von -Glutamyl-Transpeptidase und Glutathionspiegel in primären Astrozyten der Ratte. J Neurochem 73(2): 859-866, 1999.
131 Kechrid Z, Hamdi M, Naziroğlu M und Flores-Arce M: Vitamin-D-Supplementierung moduliert Zink im Blut und Gewebe, Glutathion in der Leber und biochemische Parameter im Blut bei diabetischen Ratten mit Zinkmangeldiät. Biol Trace Elem Res 148(3): 371-377, 2012.
132 G. Balogh, AR. de Boland, R. Boland und P. Barja: Wirkung von 1,25(OH)2-Vitamin D(3) auf die Aktivierung natürlicher Killerzellen: Rolle von Proteinkinase C und extrazellulärem Calcium. Exp Mol Pathol 67(2): 63-74, 1999.
133 Lee KN, Kang HS, Jeon JH, Kim EM, Yoon SR, Song H, Lyu CY, Piao ZH, Kim SU, Han YH, Song SS, Lee YH, Song KS, Kim YM, Yu DY und Choi I: VDUP1 wird für die Entwicklung natürlicher Killerzellen benötigt. Immunität 22(2): 195-208, 2005.
134 Issazadeh-Navikas S: NKT-Zell-Selbstreaktivität: Evolutionärer Hauptschlüssel der Immunhomöostase? J. Mol. Cell Biol. 4(2): 70- 78, 2012.
135 Juno JA, Keynan Y und Fowke KR: Invariante NKT-Zellen: Regulierung und Funktion während einer Virusinfektion. PLOS Pathogens 8(8): e1002838, 2012.
136 Cantorna MT: Mechanismen, die der Wirkung von Vitamin D auf das Immunsystem zugrunde liegen. Proc Nutr Soc 69(3): 286-289, 2010.
137 Yassai M, Cooley B und Gorski J: Entwicklungsdynamik von Thymus-DN iNKT nach der Selektion. PLoS One 7(8): e43509, 2012.
138 Yu S und Cantorna MT: Der Vitamin-D-Rezeptor wird für die iNKT-Zellentwicklung benötigt. Nat Acad Sci USA 105(13): 5207- 5212, 2008.
139 Yue X, Izcue A und Borggrefe T: Essentielle Rolle der Mediator-Untereinheit MED 1 bei der Entwicklung invarianter natürlicher Killer-T-Zellen. Proc Natl Acad Sci USA 108(41): 17105-17110, 2011.
140 Bendelac A, Savage PB und Teyton L: Die Biologie von NKT-Zellen. Annu Rev Immunol 25: 297-336, 2007.
141 Brennan PJ, Tatituri RVV, Brigl M, Kim EY, Tuli A, Sanderson JP, Gadola SD, Hsu FF, Besra GS und Brenner MB: Invariante natürliche Killer-T-Zellen erkennen Lipid-Selbstantigen, das durch mikrobielle Gefahrensignale induziert wird. Nat Immunol 12(12): 1202-1211, 2012. 142 Morgan JW, Morgan DM, Lasky SR, Ford D, Kouttab N, and Maizel AL: Requirements for induction of vitamin D-mediated gene regulator in normal human B- Lymphozyten. J Immunol 157(7): 2900-2908, 1996.
143 Cecere TE, Todd SM und LeRoith T: Regulatorische T-Zellen bei Arterivirus- und Coronavirus-Infektionen: Schützen sie vor Krankheiten oder verstärken sie? Viren 4: 833-846, 2012.
144 Pappworth IY, Wang EC und Rowe M: Der Wechsel von einer latenten zu einer produktiven Infektion in Epstein-Barr-Virus-infizierten B-Zellen ist mit einer Sensibilisierung für das Abtöten von NK-Zellen verbunden. J Virol 81(2): 474-482, 2007.
145 Subleski JJ, Jiang Q, Weiss JM und Wiltrout RH: Die gespaltene Persönlichkeit von NKT-Zellen bei malignen, Autoimmun- und allergischen Erkrankungen. Immuntherapie 3(10): 1167-1184, 2011.
146 H. Watarai, E. Sekine-Kondo, T. Shigeura, Y. Motomura, T. Yasuda, R. Satoh, H. Yoshida, M. Kubo, H. Kawamoto, H. Koseki und M. Taniguchi: Entwicklung und Funktion natürlicher T-Killerzellen, die TH{{ 3}} und TH17--Zytokine. PLoS Biology 10(2): e1001255, 2012.
147 Taraban VY, Martin S, Attfield KE, Glennie MJ, Elliott T, Elewaut D, Van Calenbergh S, Linclau B und Al-Shamkhani A: Invariante NKT-Zellen fördern CD8 plus zytotoxische T-Zell-Antworten, indem sie die CD70-Expression auf dendritischen Zellen induzieren . J Immunol 180(7): 4615-4620, 2008.
148 Parietti V, Chifflot H, Sibilia J, Muller S und Monneaux F: Die Behandlung mit Rituximab überwindet die Reduktion regulatorischer iNKT-Zellen bei Patienten mit rheumatoider Arthritis. Clin Immunol 134(3): 331-339, 2010.
149 Ooi JH, Chen J und Cantorna MT: Vitamin-D-Regulation der Immunfunktion im Darm: Warum haben T-Zellen Vitamin-D-Rezeptoren? Mol Aspects Med 33(1): 77-82, 2012.
150 Yu S und Cantorna MT: Epigenetische Reduktion in iNKT-Zellen nach Vitamin-D-Mangel im Mutterleib bei Mäusen. J Immunol 186(3): 1384-1390, 2011.
151 Gordy LE, Bezbradica JS, Flyak AI, Spencer CT, Dunkle A, Sun J, Stanic AK, Boothby MR, He YW, Zhao Z, Van Kaer L und Joyce S: IL-15 reguliert die Homöostase und die Endreifung von NKT-Zellen. J Immunol 187(12): 6335-6345, 2011.
152 Ma LJ, Acero LF, Zal T und Schluns K: Die Trans-Präsentation von IL-15 durch intestinale Epithelzellen treibt die Entwicklung von CD8-IELs voran. J Immunol 183(2): 1044-1054, 2009.
153 Gao J, Ma X, Gu W, Fu M, An J, Xing Y, Gao T, Li W und Liu Y: Neuartige Funktionen muriner B1-Zellen: Aktive phagozytische und mikrobizide Fähigkeiten. Eur J Immunol 42(4): 982-992, 2012.
154 Qian L, Qian C, Chen Y, Bai Y, Bao Y, Lu L und Cao X: Regulatorische dendritische Zellen programmieren B-Zellen, um sich durch IFN- und CD40L in regulatorische CD19hiFc IIbhi-B-Zellen zu differenzieren. Blut 120(3): 581-591, 2012.
155 Kin NW, Chen Y, Stefanov EK, Gallo RL und Kearney JF: Cathelin-related antimicrobial Peptidedifferentiallyregt T- and B-cell function. Eur J Immunol 41(10): 3006-3016, 2011.
156 Wuerth K und Hancock RE: Neue Erkenntnisse zur Cathelicidin-Modulation der adaptiven Immunität. Eur J Immunol 41(10): 2817- 2819, 2011.
157 Chen S, Sims GP, Chen XX, Gu YY, Chen S und Lipsky PE: Modulatorische Effekte von 1,25-Dihydroxyvitamin D3 auf die menschliche B-Zell-Differenzierung. J Immunol 179: 1634-1647, 2007.
158 Geldmeyer-Hilt K, Heine G, Hartmann B, Baumgrass R, Radbruch A und Worm M: 1,25-Dihydroxyvitamin D3 beeinträchtigt die NF-kB-Aktivierung in humanen naiven B-Zellen. Biochem Biophys Res Commun 407(4): 699-702, 2011.
159 G. Galli, P. Pittoni, E. Tonti, C. Malzone, Y. Uematsu, M. Tortoli, D. Maione, G. Volpini, O. Finco, S. Nuti, S. Tavarini, P. Dellabona, R. Rappuoli, G. Casorati und S. Abrignani: Invariante NKT-Zellen erhalten spezifische B-Zell-Antworten und Gedächtnis. Proc Natl Acad Sci USA 104(10): 3984-3989, 2007.
160 Enoksson SL, Grasset EK, Hägglöf T, Mattsson N, Kaiser Y, Gabrielsson S, McGaha TL, Scheynius A, und Karlsson MC: Das entzündliche Zytokin IL-18 induziert selbstreaktive angeborene Antikörperantworten, die durch den natürlichen Killer T reguliert werden -Zellen. Proc Natl Acad Sci USA 108(51): E1399-1407, 2011.
161 Tonti E, Fedeli M, Napolitano A, Iannacone M, von Andrian UH, Guidotti LG, Abrignani S, Casorati G und Dellabona P: Follikulare Helfer-NKT-Zellen induzieren begrenzte B-Zell-Antworten und Keimzentrumsbildung in Abwesenheit von CD4( plus ) T-Zell-Hilfe. J Immunol 188(7): 3217-3222, 2012.
162 Wen X, Yang JQ, Kim PJ und Singh RR: Homöostatische Regulation von B-Zellen der Randzone durch invariante natürliche Killer-T-Zellen. PLoS One 6(10): e26536, 2011.
163 Yang JQ, Wen X, Kim PJ und Singh RR: Invariante NKT-Zellen hemmen autoreaktive B-Zellen auf kontakt- und CD1d-abhängige Weise. J Immunol 186(3): 1512-1520, 2011.
164 Bialecki E, Paget C, Fontaine J, Capron M, Trottein F und Faveeuw C: Role of marginal zone B-lymphocytes in invariant NKT cell activation. J Immunol 182(10): 6105-6113, 2009.
165 Bosma A, Abdel-Gadir A, Isenberg DA, Jury EC und Mauri C: Lipid-antigen presentation by CD1d plus B-cells is essential for the maintenance of invariante natural killer T-cells. Immunität 36(3): 477-490, 2012.
166 Sinha A, Hollingsworth KG, Ball S und Cheetham T: Die Verbesserung des Vitamin-D-Status von Erwachsenen mit Vitamin-D-Mangel ist mit einer verbesserten mitochondrialen oxidativen Funktion im Skelettmuskel verbunden. J Clin Endocrinol Metab 98(3): E509-513, 2013. 167 Rossi AE, Boncompagni S und Dirksen RT: Sarcoplasmic reticulum-mitochondrial symbiosis: Bi-directional signalling in skeletal muscle. Exerc Sport Sci Rev 37(1): 29-35, 2009.
168 Bergman P, Lindh AU, Björkhem-Bergman L und Lindh JD: Vitamin D und Infektionen der Atemwege: Eine systematische Überprüfung und Metaanalyse randomisierter kontrollierter Studien. PLoS One 8(6): e65835, 2013.
169 Bergman P, Norlin AC, Hansen S, Rekha RS, Agerberth B, Björkhem-Bergman L, Ekström L, Lindh JD, und Andersson J: Vitamin D3 Supplementation in Patients with Frequent Respiratory Tract Infections: A randomized and double-blind intervention study . BMJ Open 2(6): e001663, 2012.
170 Pfeffer PE und Hawrylowicz CM: Vitamin D und Lungenerkrankungen. Thorax 67(11): 1018-1020, 2012.
171 BF Décard, N. von Ahsen, T. Grunwald, F. Streit, A. Street, P. Niggemeier, V. Schottstedt, J. Riggert, R. Gold und A. Chan: Niedriges Vitamin D und erhöhte Immunreaktivität gegen das Epstein-Barr-Virus vor der ersten klinischen Manifestation von multiplen Sklerose. J Neurol Neurosurg Psychiatry 83(12): 1170-1173, 2012.
172 Mealy MA, Newsome S, Greenberg BM, Wingerchuk D, Calabresi P und Levy M: Niedrige Serum-Vitamin-D-Spiegel und wiederkehrende entzündliche Rückenmarkserkrankungen. Arch Neurol 69(3): 352-356, 2012.
173 Simon KC, Munger KL und Ascherio A: Vitamin D und multiple Sklerose: Epidemiologie, Immunologie und Genetik. Curr Opin Neurol 25(3): 246-251, 2012.
174 Smolders J, Schuurman KG, van Strien ME, Melief J, Hendrickx D, Hol EM, van Eden C, Luchetti S und Huitinga I: Expression von Vitamin-D-Rezeptor und metabolisierenden Enzymen in von Multipler Sklerose betroffenem Gehirngewebe. J Neuropathol Exp Neurol 72(2): 91-105, 2013.
175 Fragoso TS, Dantas AT, Marques CD, Rocha Junior LF, Melo JH, Costa AJ und Duarte AL: 25-Hydroxyvitamin D3-Spiegel bei Patienten mit systemischem Lupus erythematodes und deren Zusammenhang mit klinischen Parametern und Labortests. Rev Bras Reumatol 52(1): 60-65, 2012.
176 Eichhorn A, Lochner S und Belz GG: Vitamin D zur Vorbeugung von Krankheiten? Dtsch Med Wochenschr 137(17): 906-912, 2012. (auf Deutsch)
177 Woloszynska-Read A, Johnson CS und Trump DL: Vitamin D und Krebs: Klinische Aspekte. Best Practise Res Clin Endocrinol Metab 25(4): 605-615, 2011.
178 Penna-Martinez M, Ramos-Lopez E, Stern J, Kahles H, Hinsch N, Hansmann ML, Selkinski I, Grünwald F, Vorländer C, Bechstein WO, Zeuzem S, Holzer K und Badenhoop K: Impaired vitamin D activation and association mit CYP24A1-Haplotypen bei differenziertem Schilddrüsenkarzinom. Schilddrüse 22(7): 709-716, 2012.
179 Walentowicz-Sadlecka M, Grabiec M, Sadlecki P, Gotowska M, Walentowicz P, Krintus M, Mankowska-Cyl A und Sypniewska G: 25(OH)D3 bei Patienten mit Eierstockkrebs und seine Korrelation mit dem Überleben. Clin Biochem 45(18): 1568-1572, 2012. 180 Abou-Raya A, Abou-Raya S and Helmii M: The effect of vitamin D supplementation on entzündungs- und hämostatische Marker und Krankheitsaktivität bei Patienten mit systemischem Lupus erythematodes: Eine randomisierte placebokontrollierte Studie. J Rheumatol 40(3): 265-272, 2013.






